###学院近代物理实验
实验报告
实验项目:钠原子光谱
实验地点:
班 级:
姓 名:
座 号:
实验时间: 年 月 日
一、实验目的:
本实验通过对钠原子光谱的观察、拍摄与分析,加深对碱金属原子的外层电子与原子实相互作用以及自旋与轨道运动相互作用的了解,在分析光谱线系和测量波长的基础上,计算钠原子的价电子在不同轨道运动时的量子缺,绘制钠原子的部分能级图.
实验预习部分
二、实验仪器设备:
1.用一般的玻璃棱镜摄谱仪,可拍摄到可见光区的谱线;石英棱镜摄谱仪和光栅摄谱仪则可拍摄到紫外、可见、红外光区的全部谱线.
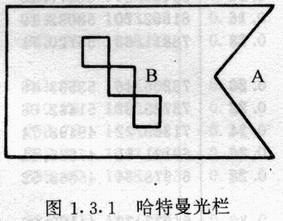
2.哈特曼光栏(见图 1.3.1)是摄谱仪的重要附件,利用光栏的A部分可以改变摄谱仪的狭缝高度;还可以利用哈特曼光栏B部分的三个小孔和固定底片盒, 并排拍摄铁谱和钠谱,以便测定钠谱线的波长.
3.利用光谱投影仪或比长仪和铁光谱标准图对比,可以辨认及测量出钠原子光谱各线系谱线的波长.
4.为了冲洗所拍摄的光谱底片,在暗房中备有整套的冲洗工具:定时钟、显影及定影药水等.
5.里德伯表(见表1.3.1).
三、实验原理:
在原子物理中,氢原子光谱的规律告诉我们:当原子在主量子数n2与n1的上下两能级间跃迁时, 它们的谱线波数可以用两光谱项之差表
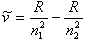
. ( 1.3.1)
式中R为里德伯常数 (109 677.58 cm-1 ).当n1= 2, n2= 3,4,5 ……,则为巴尔末线系.
对于只有一个价电子的碱金属原子(Li,Na,K ….)其价电子是在核和内层电子所组成的原子实的库仑场中运动, 和氢原子有点类似, 但是, 由于原子实的存在,价电子处在不同量子态时,或者按轨道模型的描述,处于不同的轨道时,它和原子实的相互作用是不同的.因为价电子处于不同轨道时,它们的轨道在原子实中贯穿的程度不同,所受到的作用不同;还有,价电子处于不同轨道时,引起原子实极化的程度也不同,这二者都要影响原子的能量.即使电子所处轨道的主量子数n相同而轨道量子数l不同,原子的能量也是不同的,因此原子的能量与价电子所处轨道的量子数n、l都有关.轨道贯穿和原子实极化都使原子的能量减 2
实验预习部分
少,量子数l越小,轨道进入原子实部分越多,原子实的极化也越显著,因而原子的能量减少得越多.与主量子数n相同的氢原子相比, 金属原子的能量要小,而且不同的轨道量子数l对应着不同的能量.l值越小,能量越小;l越大,越接近相应的氢原子的能级.
对于钠原子,我们可以用有效量子数n* 代替n,来统一描述原子实极化和轨道贯穿的总效果.若不考虑电子自旋和轨道运动的相互作用引起的能级分裂,可把光谱项表示为 Tn1 = R / (n*2) = R / (n ?C Δl)2 (1.3.2)
上式的Δl称为量子缺;而n* 不再是整数,由于Δl > 0,因此有效量子数n* 比主量子数n要小.理论计算和实验观测都表明,当n不很大时,量子缺的大小主要决定于l,而与n的关系很小,在本实验中近似认为它是一个与n无关的量.
由于由上能级跃迁到下能级时,发射光谱谱线的波数可用下式表示:

(1.3.3)
式中n2* 与n1* 分别为上、下能级的有效量子数,n、Δl与n’、Δl分别为上下能级的主量子数与量子缺,式(1.3.3)以两个光谱项之差的形式表达了钠原子某一谱线的波数值, l及l’分别为上、下能级所属轨道量子数.
如果令n’, l’固定, 而n依次改变(l的选择定则为l’ ?C l = ±1),则可得到一系列的值,从而构成一个光谱线系.在光谱学中通常用n’l’- nl这种符号表示线系, 当l=0, 1, 2, 3 …时,分别以 S, P, D, F …表示.钠原子光谱有四个线系:
主线系(P线系) 3S ─nP n=3,4,5,…
漫线系(D线系) 3P ─nD n=3,4,5,…
锐线系(S线系) 3P ─nS n=4,5,6,…
基线系(F线系) 3D ─nF n=4,5,6,…
在各线系中,式(1.3.3)中n’, l’是不变的, 第一项称为固定项,以An’l’表示; 第二项称为可变项,因此式可写成:

(1.3.4)
钠原子光谱具有碱金属原子光谱的典型特征 ,一般可以观测到四个光谱线系, 分析钠原子谱线时, 可以发现以下几点:
1.主线系和锐线系都分裂成双线结构.漫线系和基线系为三重结构 (要用分辨率较高的仪器方可分辨 ).对于不同的线系,这种分裂的大小和各线的强度比是不同的,但它们都是有规律的,这称为精细结构.这种精细结构可用电子自旋与轨道耦合而引起能级分裂来解释,本实验不准备作详细研究.
2.主线系在可见光区只有一对共振线??即钠黄线,其余都在紫外光区.由于自吸收的结果,所得到的钠黄线实际上是一对吸收谱线.主线系各对谱线的间隔向短波方向有规律地递减.
3
实验预习部分
3.锐线系的谱线除第一条在红外区,其余在可见光区,通常可测到3~4条谱线, 谱线较明锐、边缘较清晰,各双线都是等宽的.
4.漫线系的谱线除第一条在红外区, 其余亦在可见光区, 也可测到3~4条谱线, 但谱线稍弱,边缘漫散模糊.
5.基线系在红外区,谱线很弱,本实验不作研究.
用摄谱仪拍摄的光谱中,这些线系互相彼此穿插排列,根据强度、间隔和线型(精细结构),可以区分出属于同一线系的各条谱线,每个线系中的各条谱线的强度都是向短波方向很有规律地递减.
四、实验步骤:
1.拍摄钠原子光谱 用光谱纯碳棒做电极,上电极磨成圆锥型、下电极顶端钻一个直径为2~3 mm的小洞, 把纯 NaCl 结晶粉末放进小洞内,拍摄钠原子光谱.
为了使每条待测谱线都有感光合适、适于观测的像,可以利用哈特曼光栏分别拍摄几组不同的钠光谱及供对比的铁光谱.(NaCl粉末对摄谱仪有锈蚀作用, 实验时要注意保持仪器清洁.)
2.测量钠原子谱线的波数 底片冲洗风干后,在光谱投影仪下认谱.并在比长仪下测量谱线.用内插法测量钠原子谱线的锐线系各谱线波长.
各谱线波长测定后, 把波长换算成波数,即每一线系中相邻两谱线的波数差为

(1.3.5)
为了计算方便,令n - Δl = m+α,其中为m整数,α为正小数,式(1.3.4)可写成:

算出 (1.3.6) 后,可借助里德伯表直接查出m和α,代入n - Δl = m+α,已知n值, 即可求出Δl值.
3.求固定项

(1.3.7)
4.绘制能级图 计算出锐线系有关能级的光谱项值 (T3p,T5s, T6s, T7s……),以波数为单位,绘出钠原子的锐线系的能级图.为了比较起见,在同一能级图上画出主量子数相同的氢原子能级位置,氢原子能级的波数按下式计算:
T(n) = RH /n2 (其中RH=109 677.58 cm-1 )
*5.进一步实验 参照上述各步骤,观察并测量钠原子谱线的漫线系各谱线的波长,计算线系中相邻两谱线的波数差,找出Δl值和固定值,绘出能级图。
4
实验预习部分
六、实验数据处理:
5
实验预习部分
6
实验总结部分
七、实验结论与分析及思考题解答
1、对实验进行总结,写出结论:
2、思考题解答:
第二篇:氢原子光谱实验报告
氢原子光谱
摘 要:本实验用光栅光谱仪对氢原子光谱进行测量,测得了氢原子光谱巴尔末线系的波长,求出了里德伯常数。最后对本实验进行了讨论。
关键词:氢原子光谱,里德伯常数,巴尔末线系,光栅光谱仪
一.引言
光谱线系的规律与原子结构有内在的联系,因此,原子光谱是研究原子结构的一种重要方法。1885年巴尔末总结了人们对氢光谱测量的结果,发现了氢光谱的规律,提出了著名的巴尔末公式,氢光谱规律的发现为玻尔理论的建立提供了坚实的实验基础,对原子物理学和量子力学的发展起过重要作用。1932年尤里根据里德伯常数随原子核质量不同而变化的规律,对重氢赖曼线系进行摄谱分析,发现氢的同位素氘的存在。通过巴尔末公式求得的里德伯常数是物理学中少数几个最精确的常数之一,成为检验原子理论可靠性的标准和测量其他基本物理常数的依据。
二.实验目的
(1)熟悉光栅光谱仪的性能和用法;
(2)用光栅光谱仪测量氢原子光谱巴尔末系数的波长,求里德伯常数;
三.实验原理
氢原子光谱是最简单、最典型的原子光谱。用电激发氢放电管(氢灯)中的稀薄氢气(压力在102Pa左右),可得到线状氢原子光谱。瑞士物理学家巴尔末根据实验结果给出氢原子光谱在可见光区域的经验公式
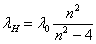 (1)
(1)
式中λH为氢原子谱线在真空中的波长。
λ0=364.57nm是一经验常数。
n取3,4,5等整数。
若用波数表示,则上式变为
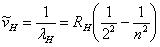 (2)
(2)
式中RH称为氢的里德伯常数。
根据玻尔理论,对氢和类氢原子的里德伯常数的计算,得
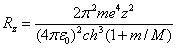 (3)
(3)
式中M为原子核质量,m为电子质量,e为电子电荷,c为光速,h为普朗克常数,ε0为真空介电常数,z为原子序数。
当M→∞时,由上式可得出相当于原子核不动时的里德伯常数(普适的里德伯常数)
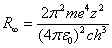 (4)
(4)
所以
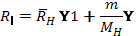 (5)
(5)
对于氢,有
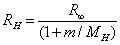 (6)
(6)
这里MH是氢原子核的质量。
由此可知,通过实验测得氢的巴尔末线系的前几条谱线的波长,借助(6)式可求得氢的里德伯常数。
里德伯常数R∞是重要的基本物理常数之一,对它的精密测量在科学上有重要意义,目前它的推荐值为R∞=10973731.568549(83)/m。
表1为氢的巴尔末线系的波长表。
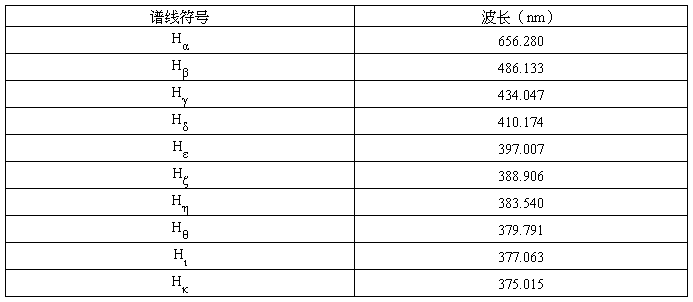
表1 氢的巴尔末线系波长
值得注意的是,计算RH和R时,应该用氢谱线在真空中的波长,而实验是在空气中进行的,所以应将空气中的波长转换成真空中的波长。即λ真空=λ空气+Δλ,氢巴尔末线系前6条谱线的修正值如表2所示。

表2 波长修正值
四. 实验仪器
 实验中用的仪器室WGD-3型组合式多功能光栅光谱仪,其主要由光栅单色仪、接收单元、扫描系统、电子放大器、A/D采集单元、计算机组成。其光学原理图如图1所示,入射狭缝、出射狭缝均为直狭缝,宽度范围0~2.5mm连续可调,光源发出的光束进入入射狭缝
实验中用的仪器室WGD-3型组合式多功能光栅光谱仪,其主要由光栅单色仪、接收单元、扫描系统、电子放大器、A/D采集单元、计算机组成。其光学原理图如图1所示,入射狭缝、出射狭缝均为直狭缝,宽度范围0~2.5mm连续可调,光源发出的光束进入入射狭缝 ,
, 位于反射式准光镜
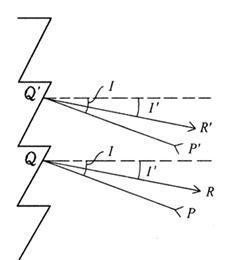
位于反射式准光镜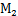 的焦面上,通过
的焦面上,通过 入射的光束经
入射的光束经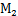 反射成平行光束投向平面光栅G上,衍射后的平行光束经物镜
反射成平行光束投向平面光栅G上,衍射后的平行光束经物镜 成像在
成像在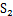 上和
上和 上,通过
上,通过 可以观察光的衍射情况,以便调节光栅;光通过
可以观察光的衍射情况,以便调节光栅;光通过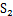 后用光电倍增管接收,送入计算机进行分析。
后用光电倍增管接收,送入计算机进行分析。
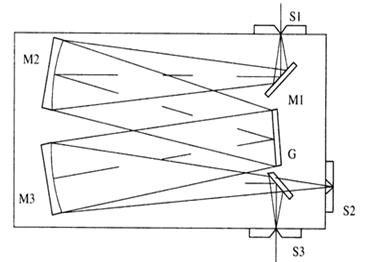
图1 光栅光谱仪光学原理图 图2 闪耀光栅示意图
在光栅光谱仪中常使用反射式闪耀光栅。如图2所示,锯齿形是光栅刻痕形状。现考虑相邻刻槽的相应点上反射的光线。PQ和P′Q′是以I角入射的光线。QR和Q′R′是以I′角衍射的两条光线。PQR和P′Q′R′两条光线之间的光程差是b(sinI+sinI′),其中b是相邻刻槽间的距离,称为光栅常数。当光程差满足光栅方程
b(sinI+sinI′)=kλ, k=0,±1,±2,…
时,光强有一极大值,或者说将出现一亮的光谱线。
对同一k,根据I、I′可以确定衍射光的波长λ,这就是光栅测量光谱的原理。闪耀光栅将同一波长的衍射光集中到某一特定的级k上。
为了对光谱扫描,将光栅安装在转盘上,转盘由电机驱动,转动转盘,可以改变入射角I,改变波长范围,实现较大波长范围的扫描,软件中的初始化工作,就是改变I的大小,改变测试波长范围。
五.实验内容
1. 接通电源前,检查接线是否正确,检查转化开关的位置。
2. 接通电箱电源,将电压调至500-900V.
3. 开启计算机,启动实验软件,选择合适光栅,选取测量范围400nm-700nm,测量步长0.5nm。
4. 打开放光管电源,将光源对准光谱仪入射狭缝。
5. 开始采样,得到四个峰,并读出对应的波长值。
六.实验数据处理与分析
对氢原子光谱进行测量,对曲线进行寻峰,读出波长如下表3,

表3,氢原子光谱的实验数据
利用表2中波长的修正值计算真空中氢原子的波长:
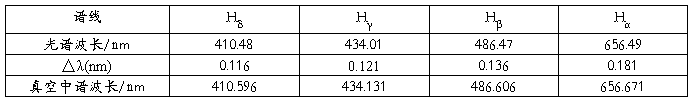
表4 氢谱线真空中的波长
利用公式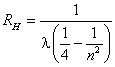 可以计算出里德伯常数,如下表5
可以计算出里德伯常数,如下表5
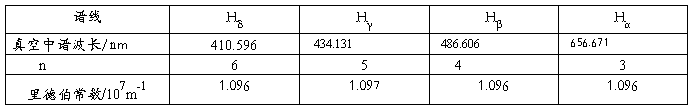
表5,氢谱线对应的里德伯常数
里德伯常数的平均值为R=(1.096+1.097+1.096+1.096)/4*107=1.096*107m-1
利用公式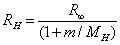 计算出普适里德伯常数,得出
计算出普适里德伯常数,得出
R=1.00054*1.096*107m-1=1.096*107m-1
而R推荐值是R∞=10973731.568549(83)/m,故相对误差为
=(1.097-1.096)/1.097=0.06%
七.实验反思
由于选用了一台新仪器,不太了解其操作,于是实验之初,犯了一些错误,比如,没有调节电压到适当值,没有把光对准狭缝等。
正式开始实验时,起初我们选用的是1号光栅,并没有在应该的波长位置出现峰值,在老师的提醒下,选用2号光栅尝试,但还是只测出了三个峰值,后又尝试了3号光栅和12号光栅效果同1号光栅。之后又调节了扫描间距重新尝试,最终得到了四个峰,并读出了它们对应的波长。
八.思考题
1、氢光谱巴尔末线系的极限波长是多少?
答:由公式 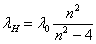 可以计算出极限波长,即n→∞时,
可以计算出极限波长,即n→∞时,
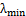 =
=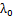 =364.57nm
=364.57nm
2、谱线计算值具有唯一的波长,但实测谱线有一定宽度,其主要原因是什么?
答:任何实测谱线都有一定的宽度,主要是由以下原因造成的:
(1)由海森伯不确定原理,?E?t>h,由于测量时间是有限的,故测得的能级有一定展宽。
(2)由于发生辐射跃迁的氢原子与探测器之间的相对运动而引入的展宽。
(3)由于实验仪器的灵敏度引入的展宽。
九. 参考文献
黄润生,近代物理实验(第二版),南京大学出版社
