蒸馏、分馏、精馏的联系与区别
u 实验证明,液体的蒸气压只与温度有关。即液体在一定温度下具有一定的蒸气压。当液态物质受热时蒸气压增大,待蒸气压大到与大气压或所给压力相等时液体沸腾,这时的温度称为液体的沸点。
蒸馏:
将液体加热至沸腾,使液体变为蒸气,然后使蒸气冷却再凝结为液体,这两个过程的联合操作称为蒸馏。
蒸馏是利用液体混合物中各组分挥发度的差别,从而实现其所含组分的分离。但是蒸馏时混合液体中各组分的沸点要相差30℃以上,才可以进行分离。当物质的沸点十分接近时,约相差20度,则无法使用简单蒸馏法,可改用分馏法。

(温度计水银球上限应和蒸馏头侧管的下限在同一水平线上)
分馏:
分馏是利用分馏柱将多次气化—冷凝过程在一次操作中完成的方法。因此,分馏实际上是多次蒸馏。它更适合于分离提纯沸点相差不大的液体有机混合物。
分馏的原理跟蒸馏基本相同,也是加热使混合液体汽化冷凝的连续操作过程,只在实验装置中添加一个分馏柱(工业上称为分馏塔盘)。在分馏柱内,当上升的蒸气与下降的冷凝液互相接触时,被加热的混合蒸气进入分馏柱,与内壁上已冷凝的回流液体发生对流而交换热量,使其中沸点较高的成分放热被液化,上升的蒸气部分冷凝放出热量使下降的冷凝液部分气化,两者之间发生了热量交换,其结果,上升蒸气中易挥发组分增加,而下降的冷凝液中高沸点组分增加,如此继续多次,就等于进行了多次的气液平衡,即达到了多次蒸馏的效果。这样靠近分馏柱顶部易挥发物质的组分比率高,而在烧瓶里高沸点组分的比率高。这样只要分馏柱足够高,就可将这种组分完全彻底分开。
工业上的精馏塔就相当于分馏柱。
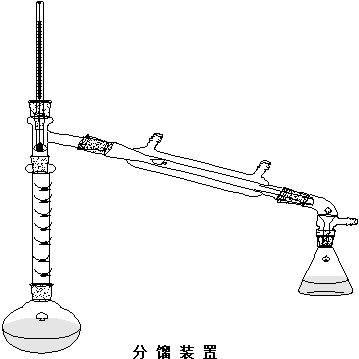
(控制好回流比,使上升的气流和下降液体充分进行热交换,使易挥发组分尽量上升,难挥发组分尽量下降,分馏效果更好。)
精馏:<精馏过程和分馏过程本质上是一样的,在有机,无机化学中一般说分馏,化工原理和物理化学叫精馏,工业上分离沸点较近的几种物质是用的精馏塔,实验室中叫分馏柱.原理都是道尔顿分压定律,拉乌尔定律.在计算理论版层数时,需要用到Gilliland关联图>
减压蒸馏:
液体的沸点是指它的蒸气压等于外界压力时的温度,因此液体的沸点是随外界压力的变化而变化的,如果借助于真空泵降低系统内压力,就可以降低液体的沸点,这便是减压蒸馏操作的理论依据。
减压蒸馏是分离和提纯有机化合物的常用方法之一。它特别适用于那些在常压蒸馏时未达沸点即已受热分解、氧化或聚合的物质
第二篇:普通蒸馏和分馏
普通蒸馏和分馏
目的
1. 了解普通蒸馏和分馏的原理以及分馏柱的作用。
2. 掌握普通蒸馏和分馏装置的安装和操作。
药品
丙酮 25mL
仪器
圆底烧瓶(100mL) 味格氏分馏柱(250mm) 直形冷凝管(200mm) 温度计(100℃) 直形冷凝管(200mm) 接液管(18×150mm) 锥形瓶(50及100mL) 量筒(10及25mL) 1个 1个 1支 1支 1支 1支 各1个 各1个
实 验 步 骤
在圆底烧瓶中,加入25mL丙酮和25mL水,并加入2粒沸石,安装蒸馏装置,按图2—6安装。再检查整套装置是否稳妥与严密。然后接通冷却水,开始加热(电热套加热时,电压由70V逐渐调至100V),当开始有馏出液管滴下时,调节火焰(或电压),使蒸馏速度每秒一滴,用量筒收集下列指定温度范围内的各馏分,并进行记录。
温度范围(℃) 体积(mL)
沸点~62 ——
63~72 ——
73~82 ——
83~95 ——
乘余物 ——
分馏操作同上,注意在蒸馏瓶上安装分馏柱[2、3][1](见图2-10)。
在同一张坐标纸上作分馏体积-温度曲线,并对蒸馏和分馏的分离效果进行比较。 注释
[1] 若升温太快,蒸气上升过多,柱中冷凝的液体将被上升的蒸气堵于柱中,此时分馏柱内会发生“液泛”或“窒息”现象。在此情况下破环了气液平衡,而且分馏不能继续进行。只有暂时降温,等柱内液体流回烧瓶中,再继续慢慢升温进行分馏。
[2]一定要严格控制好分馏速度为2~3秒一滴,才能保证良好的分离效果,因此,分馏
操作要比蒸馏操作更为细心。
[3]本实验使用味格氏分馏柱较方便,味格氏分馏管的中间,每隔一定距离向内伸出三根向下倾斜的刺状物,在柱中相交,每段刺状物间排列成螺旋状。故又称刺形分馏柱。
思 考 题
1. 分馏中,分馏柱起到什么作用?为什么某种分馏柱中要填加适当的填料?柱身为什么要用石棉布包裹?
2. 比较蒸馏和分馏在装置、操作上有哪些不同?通过实验数据比较两者的分离效果。
3. 分馏速度应如何控制?若升温太快,会产生什么现象?此时应如何操作?
