实验五 蔗糖的转化
【实验目的】
1. 测定蔗糖转化反应的速率常数和半衰期。
2. 了解旋光仪的构造、工作原理,掌握旋光仪的使用方法。
【基本要求】
1.了解在蔗糖反应的动力学方程式中,任何时刻t的蔗糖浓渡可以被反应体系在该时刻的选光度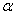 与反应终了时的选光度
与反应终了时的选光度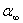 之差所替代的依据。
之差所替代的依据。
2 测定蔗糖转化率的速率常数的半衰期。
3 了解旋光仪的基本原理,掌握其实用方法。
【实验原理】
蔗糖转化反应为: C12H22O11 + H2O → C6H12O6 + C6H12O6
蔗糖 葡萄糖 果糖
为使水解反应加速,常以酸为催化剂,故反应在酸性介质中进行。由于反应中水是大量的,可以认为整个反应中水的浓度基本是恒定的。而H+是催化剂,其浓度也是固定的。所以,此反应可视为准一级反应。其动力学方程为
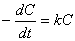 (1)
(1)
式中,k为反应速率常数;C为时间t时的反应物浓度。
将(1)式积分得: 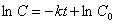 (2)
(2)
式中,C0为反应物的初始浓度。
当C=1/2C0时,t可用t1/2表示,即为反应的半衰期。由(2)式可得:
 (3)
(3)
蔗糖及水解产物均为旋光性物质。但它们的旋光能力不同,故可以利用体系在反应过程中旋光度的变化来衡量反应的进程。溶液的旋光度与溶液中所含旋光物质的种类、浓度、溶剂的性质、液层厚度、光源波长及温度等因素有关。
为了比较各种物质的旋光能力,引入比旋光度的概念。比旋光度可用下式表示:
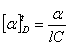 (4)
(4)
式中,t为实验温度(℃);D为光源波长;α为旋光度;l为液层厚度(m);C为浓度(kg·m-3)。
由(4)式可知,当其它条件不变时,旋光度α与浓度C成正比。即:
α=KC (5)
式中的K是一个与物质旋光能力、液层厚度、溶剂性质、光源波长、温度等因素有关的常数。
在蔗糖的水解反应中,反应物蔗糖是右旋性物质,其比旋光度[α]20D =66.6°。产物中葡萄糖也是右旋性物质,其比旋光度[α]20D=52.5°;而产物中的果糖则是左旋性物质,其比旋光度[α]20D=-91.9°。因此,随着水解反应的进行,右旋角不断减小,最后经过零点变成左旋。旋光度与浓度成正比,并且溶液的旋光度为各组成的旋光度之和。若反应时间为0,t,∞时溶液的旋光度分别用α0,αt,α∞表示。则:
α0=K反C0 (表示蔗糖未转化) (6)
α∞=K生C0 (表示蔗糖已完全转化) (7)
式(6)、(7)中的K反和K生分别为对应反应物与产物之比例常数。
αt =K反C +K生(C0-C) (8)
由(6)、(7)、(8)三式联立可以解得:
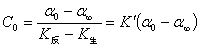 (9)
(9)
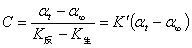 (10)
(10)
将(9)、(10)两式代入(2)式即得:
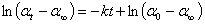 (11)
(11)
由(11)式可见,以ln(αt-α∞)对t作图为一直线,由该直线的斜率即可求得反应速率常数k。进而可求得半衰期t1/2。
根据阿累尼乌斯公式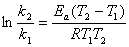 ,可求出蔗糖转化反应的活化能Ea。
,可求出蔗糖转化反应的活化能Ea。
【仪器试剂】
旋光仪1台;恒温旋光管1只;恒温槽1套;台称1台;停表1块;烧杯(100mL)1个;移液管(30mL)2只;带塞三角瓶(100mL)2只。
HCl溶液(4或2mol·dm-3);蔗糖(分析纯)。
【实验步骤】
1. 旋光仪零点的校正
洗净恒温旋光管,将管子一端的盖子旋紧,向管内注入蒸馏水,把玻璃片盖好,使管内无气泡(或小气泡)存在。再旋紧套盖,勿使漏水。用吸水纸擦净旋光管,再用擦镜纸将管两端的玻璃片擦净。放入旋光仪中盖上槽盖,打开光源,调节目镜使视野清晰,然后旋转检偏镜至观察到的三分视野最暗且暗度相等为止,记下检偏镜之旋转角α,重复操作三次,取其平均值,即为旋光仪的零点。
2. 蔗糖水解过程中αt的测定
用移液管取30mL蔗糖溶液置于100mL带塞三角瓶中。移取30mL2.5mol·dm-3HCl溶液于另一100mL带塞三角瓶中。取出两只三角瓶,将HCl迅速倒入蔗糖中,来回倒三次,使之充分混合。并且在加入HCl时开始记时,将混合液装满旋光管(操作同装蒸馏水相同)。装好擦净立刻置于旋光仪中,盖上槽盖。测量不同时间t时溶液的旋光度αt。测定时要迅速准确,当将三分视野暗度调节相同后,先记下时间,再读取旋光度。每隔一定时间,读取一次旋光度,开始时,可每3min读一次,30min后,每5min读一次。测定1h。
3. αt的测定:将步骤3剩余的混合液置于近60℃的水浴中,恒温30min以加速反应,然后冷却至实验温度,按上述操作,测定其旋光度,此值即为αt。
【注意事项】
? 装样品时,旋光管管盖旋至不漏液体即可,不要用力过猛,以免压碎玻璃片。
? 在测定α∞时,通过加热使反应速度加快转化完全。但加热温度不要超过60℃,加热过程要防止溶剂挥发,溶液浓度变化。
? 由于酸对仪器有腐蚀,操作时应特别注意,避免酸液滴漏到仪器上。实验结束后必须将旋光管洗净。
? 旋光仪中的钠光灯不宜长时间开启,测量间隔较长时应关闭几min,下一次测量前5min开启使光源稳定,以免损坏。
【数据处理】
1. 将实验数据记录于下表:
温度: ;盐酸浓度: ;α∞:

2. 以ln(αt-α∞)对t作图,由所得直线的斜率求出反应速率常数k。
3. 计算蔗糖转化反应的半衰期t1/2。
【实验讨论】
1. 测定旋光度有以下几种用途:(1)鉴定物质的纯度;(2)决定物质在溶液中的浓度或含量;(3)测定溶液的密度;(4)光学异构体的鉴别等。
2. 古根哈姆(Guggenheim)曾经推出了不需测定反应终了浓度(本实验中即为α∞)就能够计算一级反应速率常数k的方法,他的出发点是因为一级反应在时间t与t-Δt时反应的浓度c及c’可分别表示为:
c=c0e-kt
c0为起始浓度;
c’ =c0e-k(t+Δt)
由此得ln(c-c’)= - kt+ln[c0-(1- e-kt)],因此如果能在一定的时间间隔Δt测得一系列数据,则因为Δt为定值,所以ln(c-c’)对t作图,即可由直线的斜率求出k。
【实验成败的关键】
1 速率常数k与H+浓度有关,所以酸的浓度必须精确。
2 温度对K的影响不能忽视,为此实验过程应尽可能保持恒温。
3 蔗糖溶液的浓度可粗略配制,因为蔗糖溶液的浓度不影响速率常数,且我们是测旋光度来测量速率常数。
【思考题】
1. 实验中,为什么用蒸馏水来校正旋光仪的零点?在蔗糖转化反应过程中,所测的旋光度αt是否需要零点校正?为什么?
2. 蔗糖溶液为什么可粗略配制?这对结果有无影响?
3. 蔗糖的转化速率常数k与哪些因素有关?
4. 试分析本实验误差来源,怎样减少实验误差?
5. 该反应按一级反应进行的条件是什么?
6. 蔗糖水解用的蔗糖水溶液为什么必须现配?而不能久置再用?
第二篇:蔗糖转化实验
实验 2.7 蔗糖的转化 ¾¾ 一级反应
一、实验目的
1.测定蔗糖在酸催化作用下水解反应速率常数、半衰期和活化能。
2.掌握旋光仪的基本原理和使用方法。
3.掌握一级反应的动力学特征。
二、基本原理
蔗糖在水中转化为葡萄糖与果糖,其反应方程式为:
C12H22O11(蔗糖)+H2O = C6H12O6(葡萄糖)+ C6H12O6(果糖)
此反应是二级反应,在纯水中反应速率极慢,为使蔗糖水解反应加速,常以酸为催化剂。由于反应中水是大量的,可以近似认为整个反应过程中水的浓度是恒定的;而H+作为催化剂,其浓度也是固定的。因此,此反应可视为准一级反应,反应速率只与蔗糖浓度成正比。
根据反应动力学特征可知,测定反应的速率常数关键是在反应不同时间测定反应物的相应浓度。然而反应是在不断进行的,要快速分析出反应物的浓度是较困难的。但蔗糖及水解产物葡萄糖和果糖均为旋光性物质,而且它们的旋光能力不同,因此可以利用体系在反应过程中旋光度的变化来衡量反应的进程。溶液的旋光度与溶液中所含旋光物质的种类、浓度、样品管长度、光源波长及温度等因素有关。在其它条件固定时,旋光度α与反应物浓度有直线关系,即:
α = KC (2.7-1)
式中的比例常数K与物质的旋光能力、溶液性质、溶液浓度、样品管长度和温度等均有关。
物质的旋光能力用比旋光度来表示。在蔗糖的水解反应中,反应物蔗糖和产物中的葡萄糖都是右旋性物质,其比旋光度分别为66.6°和52.5°,但产物中的果糖是左旋性物质,其比旋光度为-91.9°。由于溶液的旋光度为各组成的旋光度之和,因此随着水解反应的进行,反应体系的右旋角度不断减小,最后经过零点变成左旋。当反应开始时(t=0)、经过一段时间t,以及蔗糖水解完全时(t→∞)溶液的旋光度分别用α0,αt,α∞表示。则:
α0 = K反C0 (2.7-2)
αt = K反Ct + K生(C0-Ct) (2.7-3)
α∞ = K生C∞ (2.7-4)
式中,K反 和K生 分别为反应物与生成物的比例常数,C0为反应物的最初浓度,C∞ 是生成物最终之浓度,Ct是时间为t 时蔗糖的浓度。由式(2.7-2)、(2.7-3)和(2.7-4)得:
 (2.7-5)
(2.7-5)
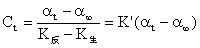 (2.7-6)
(2.7-6)
将式(2.7-5)和(2.7-6)代入一级反应的积分式:
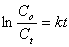 (2.7-7)
(2.7-7)
可得:
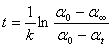 (2.7-8)
(2.7-8)
即:
 (2.7-9)
(2.7-9)
若以 ln(αt-α∞)对t作图,从直线的斜率即可求得反应速率常数k,进而可求得半衰期t1/2 = ln2/k。
测出不同温度下的速率常数,利用阿仑尼乌斯(Arrhenius)经验公式可计算出蔗糖水解反应的活化能(Ea):
 (2.7-10)
(2.7-10)
式中k1和k2分别为温度T1和T2时的速率常数。
三、仪器与试剂
仪器:旋光仪1台,恒温装置1套,100 mL磨口锥形瓶3只,25 mL移液管二支,100 mL量筒,停表1块,洗耳球1只,台称1台。
试剂:3 mol·dm-3 HCl,蔗糖(A.R.)。
四、实验步骤
1.仪器装置
旋光仪的构造、原理和使用方法详见本丛书第一分册仪器部分。
2.控制恒温水浴的温度恒定在(25 ± 0.1)oC,开启旋光仪预热。
3.旋光仪零点的校正
洗净旋光管,将管子一端的盖子旋紧,向管内注满蒸馏水,把玻璃片盖好,尽量使管内无气泡存在。再旋紧套盖,勿使漏水。管中如有气泡,可赶至胖肚部分。用吸水纸擦净旋光管,再用擦镜纸将管两端的玻璃片擦净。将旋光管放置到旋光仪中进行零点校正。记录旋光仪读数重复测量三次,平均值即为零点,用于校正仪器的系统误差。
3.反应过程中溶液旋光度的测定
在锥形瓶中,称取 10 g 的蔗糖溶于 50 mL 蒸馏水中,使蔗糖完全溶解,若溶液浑浊应过滤。用移液管各取蔗糖溶液和3 mol·dm-3 HCl溶液25 mL,分别置于 100 mL 的锥形瓶中,加盖后放入恒温水浴充分恒温至少 10 min后取出,将 HCl 溶液倒入蔗糖溶液中振荡,注意:当HCl溶液刚倒入蔗糖溶液中时开始记时,并立即倒回盛 HCl 溶液的瓶中再振荡,来回3 ~ 4次,使之均匀。其后立即用此混合反应液少许,洗旋光管 2 ~ 3次后,用反应混合液装满旋光管,旋上套盖,擦净管外的溶液后,尽快放入旋光仪中进行观察测量。要求在反应开始后2 ~ 3 min内测定第一个数据。其后,将盛混合反应液的旋光管放入已经预先恒温好的恒温水浴中,在反应开始15 min内每间隔1 min测量一次旋光度,以后测量的时间间隔可适当加长,一直测到旋光度由右旋变到左旋为止。每一次测量前,将旋光管从水浴中取出,用滤纸或毛巾擦净管外的溶液后,尽快放入旋光仪中进行观察测量。寻找到平衡点立即记下反应时间t,再读取旋光度αt。每测量一次旋光度后,迅速将旋光管放入恒温水浴中恒温,以尽可能使反应混合液保持恒定的温度。
4.α∞的测定
将上述剩余的蔗糖和HCl溶液的反应混合液置于 50 ~ 60 oC 水浴上温热 1.5小时左右,然后冷却至原实验温度,再测此溶液的旋光度,即为α∞值。
5.将恒温槽调节到另一温度,如35oC恒温,按上述实验步骤测定体系的旋光度随反应时间的关系。
五、结果与讨论
1.将反应过程中测得的旋光度αt和对应时间t列表,作出相应的αt~t图。
2.从αt~t曲线上,等间隔时间t取8个αt~t,通过计算,以ln(αt-α∞) ~ t作图,由直线的斜率求反应速率常数k,并由k值计算其半衰期t1/2。
3.根据两个不同温度下T1和T2测得的k1和k2,由Arrhenius公式(2.7-10)计算反应的表观活化能。
六、注意事项
1.测量αt要快而准,以减少实验温度波动时速率常数带来的误差。
2.旋光仪不要长时间开启,间隔超过20 min应该关闭,需要测定时提前5 min开启旋光仪。
3.装样品时,旋光管管盖旋至不漏液体即可,不要用力过猛,以免压碎玻璃片。实验结束时,应将旋光管洗净干燥,防止酸对旋光管得腐蚀。
4.在测定α∞时,通过加热使反应速度加快转化完全,但加热温度不要超过60oC,否则将产生副反应,颜色变黄。在H+催化下,蔗糖除了水解,由于蔗糖高温还有脱水反应,这会影响测量结果。另外,加热过程亦应避免溶液蒸发影响浓度,否则影响α∞测定的准确性。
七、思考题
1.实验中,我们用蒸馏水来校正旋光仪的零点,试问在蔗糖转化反应过程中所测的旋光度αt是否必须要进行零点校正?
2.蔗糖的水解速率常数与哪些因素有关?
3.配置蔗糖溶液时以托盘天平称量蔗糖并不够准确,这对测量结果是否有影响?
4.在测量蔗糖和HCl反应液时刻t对应的旋光度时,能否如同测纯水的旋光度那样,重复测三次后,取平均值?
5.在混合蔗糖溶液和盐酸溶液时,我们将盐酸加到蔗糖溶液里去了,可否将蔗糖溶液加到盐酸溶液中去?为什么?
6.本实验主要的误差因素是什么?如何减少实验误差?
八、拓展与应用
1.蔗糖在纯水中水解速率很慢,但在催化剂作用下会迅速加快,其反应速率大小不仅与催化剂种类有关而且与催化剂的浓度有关。
2.本实验除了用H+离子作催化剂外,也可用蔗糖酶催化。后者的催化效率更高,并且用量大大减少。
3.蔗糖酶的制备可采用如下方法:(1)在50 mL洁净的锥形瓶中,加入鲜酵母10 g,同时加入0.8 g醋酸钠,搅拌15 ~ 20 min,使之溶化;(2)再加入1.5 mL甲苯,用软木塞将瓶口塞住,摇荡10 min,置于37oC恒温水浴中,保温60 h。(3)取出后加入1.6 mL醋酸溶液(4 mol×dm-3)和5 mL蒸馏水,使其中pH为4.5左右,摇匀。(4)用离心机,以3000 r×min-1的转速离心30 min,取出后用滴管将中层澄清液移出,放置于冰柜中备用。
4.若要考虑 H+ 对反应速度的影响,可由:
k = k0 C
C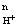
通过作图法求出酸催化速率常数( )和 H+ 的反应级数(n)。式中k0为
)和 H+ 的反应级数(n)。式中k0为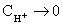 时的反应速率常数,k为蔗糖水解反应的表观速度常数。
时的反应速率常数,k为蔗糖水解反应的表观速度常数。
5.物质的旋光能力用比旋光度来度量,比旋光度用下式表示:
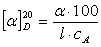
式中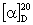 右上角的“20”表示实验时温度为20oC,D是指旋光仪所采用的钠灯光源D线的波长,即589 nm,α为测得的旋光度(°),l为样品管长度(dm),
右上角的“20”表示实验时温度为20oC,D是指旋光仪所采用的钠灯光源D线的波长,即589 nm,α为测得的旋光度(°),l为样品管长度(dm),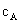 为浓度(g/100 mL)。
为浓度(g/100 mL)。
6.本实验在安排上,由于时间原因,采用测定两个温度下的反应速率常数来计算反应活化能。如果时间许可,最好测定6至8个温度下的速率常数,根据阿仑尼乌斯方程的积分形式:lnk = -Ea/RT + 常数 作lnk对1/T图,可得一条直线,从直线斜率求算反应活化能Ea,其结果更合理可靠些。
九、参考文献
1.刁国旺,阚锦晴,刘天晴编著,物理化学实验,北京:兵器工业出版社,1993。
2.Daniels F., Alberty R. A.,Williams J.W., Cornwell C. D., Bender P., Harriman J. E., Experimental Physical Chemistry, 6th Ed, New York: McGraw Hill Book Co Inc, 1962:193.
3.北京大学化学系物理化学教研室,物理化学实验(修订本),北京:北京大学出版社,1985。
4.http://151.fosu.edu.cn/hxsy/wulihuaxueshiyan/my%20web/zhetang%20z.htm.
5.http://jw.scuec.edu.cn/greatcourse/wulihuaxue/pp/content/canesugar/teaching%20materials. htm.
6.http://kcjs.yznu.cn/wlhx/Article.asp?id=667
