CNAS T0709化妆品中铅、砷的检测结果报告单
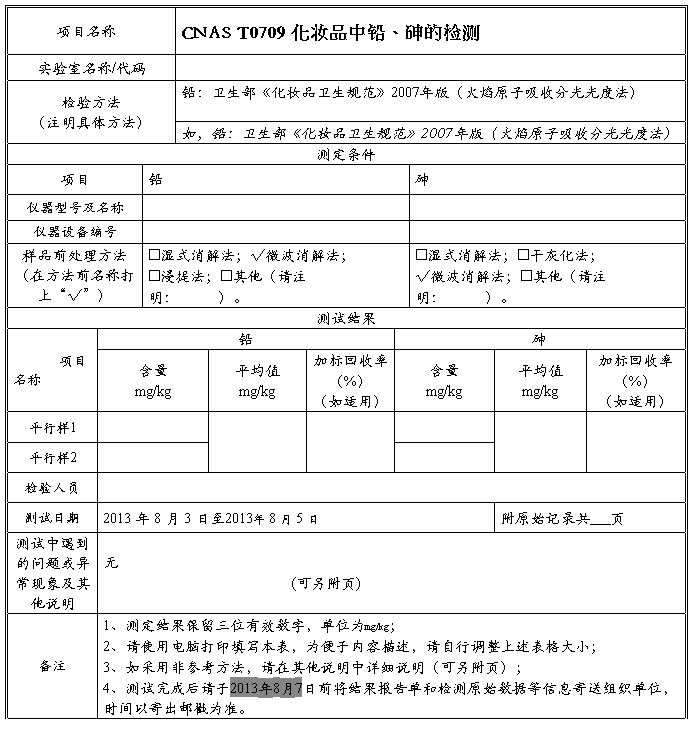
实验室负责人(签字): 签发日期:
(实验室盖章)
第二篇:CNAS T0426 抗生素微生物检定法测定药品含量 能力验证计划结果报告
CNAS T0354
CNAS T0426
抗生素微生物检定法测定药品含量
能力验证计划结果报告
中国合格评定国家认可委员会
上 海 市 食 品 药 品 检 验 所
二○一○年二月
组织机构:中国合格评定国家认可委员会
能力验证负责人:翟培军
联 系 人:何平
联系地址:北京市崇文区南花市大街8号
邮政编码:100062
联系电话:(010)67105287
传 真:(010)67105055
实施机构:上海市食品药品检验所
计划负责人:林 梅
联 系 人:杨美成
联系地址:上海市浦东新区张衡路1500号
邮政编码:201203
联系电话:(021)50798202/50798211
传 真:(021)50798211
统计专家:杨美成 唐海霞
技术专家:林 梅 钱维清 杨美成
- 2
目 录
一.前言................................................................4
二.本次计划的特点......................................................4
1.计划的目的和意义.....................................................4
2.参加实验室的范围.....................................................5
3.计划测试项目和要求...................................................6
4.样品情况描述.........................................................6
5.保密性要求...........................................................6
6. 日程安排.............................................................6
三.统计分析的设计及能力评价原则.........................................6
四.统计处理结果及能力评价...............................................7
1.检测结果统计量.......................................................7
2.检测结果情况综述.....................................................8
3.有问题结果及不满意结果实验室代码汇总..................................8
五.技术分析与建议......................................................8
1.参加实验室采用的检验方法等技术信息....................................8
2.技术分析.............................................................9
六. 附录.............................................................11
附录 A 实验室的检测结果和统计处理.....................................12
附录 B 样品制备和均匀性检验、稳定性情况...............................19
附录 C 相关文件(被测物品接受状态确认表和作业指导书).................24
附录 D 参考文献......................................................29
- 3
一.前言
本报告是对CNAS T0426《抗生素微生物检定法测定药品含量》能力验证计划结果的总结,由上海市食品药品检验所负责起草,中国合格评定国家认可委员会(CNAS)秘书处审核并批准发布。
CNAS T0426《抗生素微生物检定法测定药品含量》能力验证计划由CNAS组织,上海市食品药品检验所作为技术支持机构负责计划的协调及实施。
CNAS依据ISO/IEC导则43:1997的要求运作能力验证计划。
CNAS要求申请认可和获准认可的实验室必须通过参加能力验证活动(包括CNAS组织实施或承认的能力验证计划、实验室间比对和测量审核)证明其技术能力。只有在能力验证活动中表现满意,或对于不满意结果能证明已开展了有效纠正措施的实验室,CNAS方受理或予以认可;对于未按规定的频次和领域参加能力验证的获准认可实验室,CNAS将采取警告、暂停、撤销资格等处理措施。
对参加了CNAS组织及其承认的能力验证活动且有稳定满意表现的机构,在CNAS的各类评审中可适当根据情况简化相关项目的能力确认过程。
获CNAS认可的实验室,在参加能力验证中出现不满意结果时,CNAS要求其立即停止在相关项目的证书/报告中使用CNAS的认可标识,并按其体系文件规定程序实施有效的纠正措施。实验室只有将实施纠正措施的记录以及纠正措施有效性证明材料在规定的期限内报CNAS确认后,方可恢复使用认可标识。
如果实验室的结果虽为不满意,但仍符合认可项目依据标准所规定的判定要求,实验室可向CNAS提出,经CNAS确认后,可恢复使用认可标识,但实验室仍需采取相关改进措施;对于出现可疑结果的机构,CNAS建议其采取相应的自查措施。
二.本次计划的特点
1.计划的目的和意义
抗生素微生物检定法不仅在中国药典和中国兽药典等国家标准中有收载,在美国药典、英国药典、日本药典、欧洲药典等国外药品权威标准中也都有收载,是药品质量检测的常用分析方法。
本次能力验证计划的目的是为了评价参加实验室采用抗生素微生物检定法的技术水平和能力,促进参加实验室进一步提高检测技术和加强实验室管理,尤其是检测结果不好的实验室,更要寻找原因,采取措施,保证日常检测结果的准确、可靠。
- 4
2.参加实验室的范围
本次能力验证计划共有85个实验室报名参加,分布于26个省、直辖市、自治区。参加实验室主要为国家、省、地市等各级药品检验所,也有兽药饲料检验机构、药品生产企业的分析测试中心等,见表1。在这些实验室中,检测项目已通过CNAS认可的有42家,占参加实验室总数的49%。所有报名的实验室都报告了检测结果。
表1 实验室分布情况 省、自治区、直辖市 食品药品检兽药饲料检其他检验机
验机构 验机构 构 合计
北京市 上海市 重庆市 江苏省 广西壮族自治区 浙江省 广东省 吉林省 山东省 辽宁省 河北省 四川省 福建省 陕西省 黑龙江省 安徽省 青海省 山西省 内蒙古自治区 新疆维吾尔自治区 河南省 甘肃省 海南省 湖北省 贵州省 宁夏回族自治区 总计
- 5
3.计划测试项目和要求
3.1 本次能力验证计划采用抗生素微生物检定法测定琥乙红霉素含量,推荐的检测依据为中国药典20xx年版二部,要求实验室按照日常检测程序和方法进行检测。因结果报告的含量值是以无水物计算,故需同时检测水分。
3.2 本次能力验证计划在向每个参加实验室发送检测样品的同时,附有作业指导书、结果报告单、被测物品接受状态确认表。见附录C。
4.样品情况描述
4.1 本次能力验证计划向每个参加实验室提供2份白色粉末样品,分别标注为:“ 实验室代码-1”和“实验室代码-2”,每瓶装量约1.6g。本次能力验证计划的样品为分割水平设计的样品对,分别定义为A样和B样。A样是普通琥乙红霉素原料,B样是琥乙红霉素精制原料;1号样、2号样与A样、B样间的对应关系见附录A1检测结果和统计处理的第3页的注1。
4.2 本次能力验证计划样品在发放前已进行了均匀性检验,相关情况见附录B,结果表明样品的均匀性符合要求。本次能力验证计划结果报告中出现的不满意结果或离群值不是由样品的差异所致。
5.保密性要求
每个参加实验室被随机分配一个唯一性代码,为保证参加实验室秘密,报告中的参加实验室均以代码表示。
6. 日程安排
20xx年4月 邀请实验室参加20xx年能力验证计划并开始报名。
20xx年6月 向参加实验室发出能力验证样品。
20xx年7月 反馈结果。
20xx年8月 汇总实验室数据,专家审核及统计工作。
20xx年 9月~10 月 编写能力验证计划结果报告。
三.统计分析的设计及能力评价原则
本次能力验证计划统计分析采用稳健(Robust)技术处理,即采用稳健统计的中位值作为指定值,标准化四分位距(NIQR)为变动性度量值(目标标准偏差)计算各
- 6
实验室结果的Z比分数(Z值)。本次能力验证计划中测定样品为按分割水平设计的样品对,因此,对抗生素微生物检定法测得结果分别计算实验室间Z比分数(ZB)和实验室内Z比分数(ZW)。
对本次能力验证计划实验室的检测结果,按下式计算Z值:
Z=(x-X)/σ
式中:x - 实验室测试结果;
X - 指定值;
σ- 变动性度量值(目标标准偏差)。
本次能力验证计划涉及的统计量有结果数、中位值、标准化四分位距(NIQR )、稳健的变异系数(CV)、最小值、最大值和极差等。各统计量的意义及相关计算方法参见CNAS GL02:2006《能力验证结果的统计处理和能力评价指南》。
本次能力验证计划以Z比分数(包括实验室间Z比分数ZB和实验室内Z比分数ZW)评价实验室的结果,即:若∣Z∣≤2,检测结果为满意结果;若2<∣Z∣<3,检测结果为有问题;若∣Z∣≥3,检测结果为不满意结果或离群值。
为了清晰表示各实验室参加能力验证计划的结果,附录A中给予了Z比分数柱状图以及尤登图。从这两种图上,每一个实验室很容易将其结果与其他参加实验室进行比较,了解其结果在本次计划中所处的水平。
四.统计处理结果及能力评价
1.检测结果统计量
表2是检测结果统计量汇总。
- 7
表2 检测结果统计量汇总表 检测
项目 样品标识 结果数 中位值 (单位/mg)标准化四分位距
(单位/mg) 稳健变异系数(%)最大值 (单位/mg)最小值 (单位/mg) 极差
(单位/mg)
A样红霉素
含量 B样
2.检测结果情况综述
参加本次能力验证计划的实验室共85家。在Z比分数的统计中,有69家的结果为满意,有11家的结果有问题,5家的结果为不满意,各占总数的81.2%、12.9%和5.9%。
3.有问题结果及不满意结果实验室代码汇总
表3 有问题结果及不满意结果实验室代码汇总表
检测项目
红霉素
含量
结果情况 有问题结果 实验室代码 5、6、31、34、36、49、60、64、72、81、83 不满意结果、28、47、62、76
五.技术分析与建议
1.参加实验室采用的检验方法等技术信息
参加本次能力验证计划的85家实验室中除部分兽药监察所采用的检测方法为中国兽药典20xx年版二部外,均采用了作业指导书推荐的中国药典20xx年版二部琥乙红霉素项下规定的方法,采用抗生素微生物检定法(中国药典20xx年版二部附录Ⅺ
A)来测定琥乙红霉素的含量。经查阅中国药典20xx年版二部的抗生素微生物检定法与中国兽药典20xx年版二部的抗生素微生物检定法基本一致。但有部分实验室结果报告单检测方法项的填写不规范,如仅填写“管碟法”、“二剂量法”、“三剂量法”。
根据各参加实验室提交的记录对影响检验结果准确性的主要技术信息汇总、分析如下:
- 8
1)使用的培养基 85家实验室所用培养基共涉及14家厂商,从结果看不同生产商的培养基对本次能力验证结果无影响。
2)抗生素抑菌圈的测量器具 各参加实验室均采用了抗生素抑菌圈面积测定仪进行结果的测量、计算和统计,没有用游标卡尺测量后手动计算结果的实验室。从结果看不同生产商的测量器具对本次能力验证结果无影响。
3)琥乙红霉素供试品的水解条件 药典规定了室温放置16小时或40℃放置6小时的两个条件。有66家实验室采用了40℃放置6小时的条件;另有19家采用了室温放置16小时的条件,他们的代码为:1、5、7、8、22、23、27、28、35、42、49、50、51、57、58、61、66、71、83。将这两个方法分组,剔除离群值(Z>=3)后,进行t检验,得到t值分别为1.21和0.27,均小于临界值 tp(v)=1.99(p=0.95,v=80),表明这两个方法无显著性差异。实施方也做过两种水解条件的对比,证明药典提供的两个条件均能适用,对检验结果没有影响。
结果为“有问题”和“不满意”的实验室共有16家(见表3),其中采用40℃放置6小时的实验室为13家,采用室温放置6小时的为3家。
其中代码为49的实验室在室温放置时间达22小时,代码为71的实验室将两个样品分别各采取一个水解条件,这都属于对标准方法的偏离。
4)结果报告的平均值形式 85家实验室中有77家实验室按算术平均值报告结果值;另有8家实验室按加权平均值报告结果值,他们的代码是7、12、18、43、45、49、63、65。实施方将他们报告的加权平均值与按算术平均值计算的结果一一作了对比,两者差基本在0.0~±1.1u/mg之间,仅有一个样品两者之差为2.3u/mg。
在中国药典以及《中国药品检验标准操作规范》中均没有提及用加权平均值报告结果值。
2.技术分析
抗生素微生物检定法属于生物测定范畴,不确定因素较多,与一般理化分析比较更依赖于操作者的经验、熟练程度、甚至于手法和视力等。而这些信息是无法从反馈的有限信息中获得的,我们仅能从总体上进行技术分析,以供参考。
1)标准品的影响
除兽药监察系统内的一些实验室所用红霉素标准品来源为中国兽医药品监察所外,大多数实验室所用红霉素标准品均为来自中国药品生物制品检定所的批号为
- 9
130307——200716、纯度为938u/mg的红霉素标准品。但也有四家实验室(代码为4、5、25、81)没有遵守抗生素标准品新批号发布老批号自动作废的规定,使用了批号为130307-200215或3079312的过期作废标准品。这四家实验室中,代码为25的实验结果为不满意,代码为5、81的实验结果为有问题,仅代码为4的实验结果尚在满意范围内。抗生素类标准品易受保存温度、湿度、时间等影响发生降解而使其纯度发生变化,在抗生素药品的含量测定中,所用标准品的效期和保存条件是影响结果准确性的重要因素。
2)标准品和供试品的称量和稀释的影响
抗生素微生物检定法是根据量反应平行线原理设计的方法,要求标准品高、低剂量溶液的浓度与供试品高、低剂量溶液的浓度一致。建议应根据《中国药品检验标准操作规范》中抗生素微生物检定法中称量和稀释的要求进行,即:调节标准品和供试品的第一步稀释使浓溶液的浓度均为每1ml中含500单位,然后平行地在500单位/ml整数浓度的基础上用移液管各取相同的整数体积进一步稀释,最终制备成整数的高、低浓度供试液。但是本次能力验证计划中有部分实验室第一步稀释后所得标准品溶液和供试品溶液的单位浓度就不相同,接下来用移液管各取相同的整数体积作第
二、第三步的稀释,则其最终溶液的单位浓度也不相同,且该差异未在实验结果的统计计算予以消除,从而影响实验结果的准确性。
3)抑菌圈直径的影响
在抗生素微生物检定法中,要求二剂量法标准品溶液的高浓度所致的抑菌圈直径在18~22mm之间,如抑菌圈直径太小会增加实验误差;还要求高、低浓度所致抑菌圈直径也应有适当差距,这是因为方法统计学的可靠性测验中剂间必须有显著差异。故要求实验人员通过摸索适宜的加菌量,或选择适宜的高、低供试浓度得到理想的抑菌圈直径,这也是保证实验结果准确性的重要因素之一。
4)向小钢管滴加溶液所用工具和时间的影响
向小钢管滴加标准品和供试品溶液是抗生素微生物检定法关键的技术操作步骤之
一。一般要求用毛细滴管按SH→TH→TL→SL的顺序滴加至液面与小钢管口“平满”,影响因素有小钢管内径的均匀性、操作者对液面“平满”的判断、每碟滴加所用时间、操作者的视力、手式、经验等等。
根据反馈信息有部分实验室采用微量加样器滴加溶液以克服可能存在的小钢管内径不均匀问题及液面“平满”的判断问题。但也有实验室(代码为30)在结果报告单中记录了微量加样器枪头内有“挂壁”的现象,可能引入操作误差。
- 10
因在滴加溶液的同时小钢管内抗生素溶液已在不断向菌层培养基扩散,所以滴加时间应尽可能短。绝大多数实验室滴加溶液所用时间平均在每碟0.5~1分钟左右,但也有些实验室滴加时间过长,如代码为19、20的实验室的平均滴加时间为每碟3分钟左右,甚至个别实验室(代码为47)记录滴加12个碟子用了80分钟,平均每碟
6.7分钟。这将增加剂间、碟间的差异从而影响实验的结果。
由于离群值产生的原因多种多样,在此无法一一罗列,希望数据离群的实验室结合检测过程,找出离群的可能原因。
六. 附录
附录A . 实验室的检测结果和统计处理
A1 检测结果和统计处理
A2 Z比分数柱状图
A3 尤登图
附录B. 样品制备和均匀性检验、稳定性情况
B1 样品制备报告
B2 均匀性检验报告
B3 稳定性情况说明
附录C. 相关文件(被测物品接收状态确认表和作业指导书)
C1 被测物品接收状态确认表
C2 作业指导书
附录D. 参考文献
- 11
附录 A
实验室的检测结果和统计处理
- 12
附录A1 检测结果和统计处理 实验室代码
01 02 03 04 05 06 07 08 09 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34
抗生素微生物检定法测定
A样 769.0 768.3 769.2 749.8 759.0 753.4 751.5 769.4 775.5 760.6 769.2 744.5 752.5 765.8 756.6 747.3 776.2 776.7 772.9 777.9 772.2 773.9 769.1 776.2 721.4 767.6 762.6 746.0 768.6 768.8 749.6 763.0 757.6 782.5
B样 797.8 790.1 821.0 803.4 831.9 773.7 812.8 811.8 822.6 813.8 806.0 811.4 803.7 808.2 803.0 799.0 828.0 821.9 805.2 809.1 817.1 815.0 795.6 822.6 786.4 793.6 805.9 769.6 799.4 821.6 780.6 808.0 807.6 835.1
Si
1107.9 1102.0 1124.4 1098.3 1124.9 1079.8 1106.1 1118.1 1130.0 1113.3 1113.8 1100.2 1100.4 1113.0 1102.8 1093.4 1134.3 1130.4 1115.9 1122.2 1123.8 1123.5 1106.4 1130.5 1066.2 1103.9 1109.1 1071.7 1108.7 1124.6 1082.0 1110.9 1106.8 1122.7
Di20.4 15.4 36.6 37.9 51.5 14.4 43.3 30.0 33.3 37.6 26.0 47.3 36.2 30.0 32.8 36.6 36.6 32.0 22.8 22.1 31.7 29.1 18.7 32.8 46.0 18.4 30.6 16.7 21.8 37.3 21.9 31.8 35.4 6.9
ZBi-0.25 -0.70 1.02 -0.99 1.06 -2.40* -0.38 0.53 1.45 0.16 0.21 -0.84 -0.82 0.14 -0.64 -1.36 1.78 1.47 0.36 0.85 0.97 0.95 -0.36 1.48 -3.45§ -0.55 -0.16 -3.02§ -0.18 1.03 -2.23* -0.02 -0.34 2.50*
ZWi -1.00 -1.49 0.60 0.72 2.07* -1.59 1.26 -0.06 0.27 0.70 -0.45 1.65 0.56 -0.06 0.22 0.59 0.60 0.14 -0.76 -0.83 0.12 -0.15 -1.16 0.22 1.52 -1.20 0.01 -1.36 -0.86 0.67 -0.85 0.13 0.47 0.65
- 13
实验室代码
35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70
抗生素微生物检定法测定
A样 757.0 789.0 764.2 765.5 764.7 763.6 765.2 750.9 764.7 774.1 766.2 766.1 869.1 777.8 751.2 743.7 759.7 763.8 764.6 776.8 761.4 776.8 750.3 767.1 768.1 748.6 787.9 794.2 768.5 750.0 764.7 780.0 764.7 760.9 760.0 759.3
B样 819.2 798.7 814.8 812.2 815.9 811.8 802.0 819.6 815.4 810.0 814.9 815.5 867.6 809.4 781.0 811.8 812.5 804.5 807.8 827.0 808.4 794.6 797.7 787.1 799.0 784.9 814.9 709.4 818.0 779.8 808.3 824.1 806.2 798.1 799.2 798.0
-
Si
1116.5 1115.6 1117.7 1114.0 1108.2 1110.5 1117.3 1120.1 1118.0 1118.4 1228.0 1122.3 1083.4 1099.9 1111.7 1109.0 1111.9 1134.1 1110.0 1111.1 1094.6 1099.0 1108.1 1084.3 1133.4 1063.2 1121.8 1081.7 1112.3 1134.3 1110.8 1102.4 1102.5 1079.3 1124.0 1107.2
Di35.8 33.0 36.2 34.1 26.0 48.6 35.9 25.4 34.4 34.9 -1.1 22.3 21.1 48.2 37.3 28.8 30.5 35.5 33.2 12.6 33.5 14.1 21.8 25.7 19.1 -60.0 35.0 21.1 30.8 31.2 29.3 26.3 27.7 30.5 39.9 12.3
ZBi0.26 0.88 0.41 0.34 0.50 0.22 -0.23 -0.05 0.47 0.69 0.53 0.55 8.96§ 0.86 -2.12* -0.86 0.04 -0.17 0.05 1.76 -0.09 0.00 -1.27 -0.93 -0.23 -2.05* 1.70 -3.67§ 0.82 -2.25* 0.09 1.77 -0.03 -0.67 -0.66 -0.76
ZWi 1.32 -2.33* 0.51 0.24 0.56 0.35 -0.45 1.77 0.52 -0.51 0.38 0.43 -3.11§ -0.81 -0.93 1.73 0.67 -0.17 0.00 0.49 0.26 -1.77 0.29 -1.61 -0.86 -0.48 -1.13 -8.90§ 0.44 -0.93 0.03 0.06 -0.12 -0.42 -0.28 -0.31
14
实验室代码
71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 结果数 中位值 (单位/mg) 标准化IQR (单位/mg) 稳健CV(%) 极小值 (单位/mg) 极大值 (单位/mg) 范围 (单位/mg)
抗生素微生物检定法测定
A样 761.5 741.6 766.6 774.2 753.6 799.0 763.1 760.7 762.6 770.6 757.6 769.6 741.2 780.0 780.2 85 764.7 10.82 1.41 721.4 869.1 147.7
B样 804.7 784.8 823.0 791.6 794.7 765.4 806.0 814.6 802.4 817.3 830.8 811.0 789.9 801.1 800.6 85 807.8 12.53 1.55 709.4 867.6 158.2
Si
1094.8 1106.2 1109.5 1113.9 1106.6 1122.8 1123.2 1117.7 1082.7 1118.0 1117.8 1107.9 1102.0 1124.4 1098.3 85 1111.1 13.05 1.17 1063.2 1228.0 164.8
Di29.1 -23.8 30.3 38.1 28.1 33.0 51.8 29.3 34.4 14.9 14.4 20.4 15.4 36.6 37.9 85 30.55 10.17 33.29 -59.96 51.76 111.72
ZBi-0.28 -2.44* 0.99 -0.30 -1.25 -0.38 -0.12 0.21 -0.35 0.89 0.92 0.50 -2.18* 0.53 0.51
ZWi 0.00 0.00 0.92 -1.79 -0.15 -5.34§ -0.02 0.74 -0.24 0.24 2.09* -0.13 0.38 -1.54 -1.59
注:1、实验室代码为6n+1,6n+2,6n+3的1号样为A样,2号样为B样; 实验室代码为6n+4,6n+5,6n+6的1号样为B样,2号样为A样; n为0~14的整数。
2、标“§” 的为不满意结果; 标“ * ” 的为可疑结果。
- 15
附录A2 Z比分数柱状图
实验室间Z比分数(ZB)柱状图
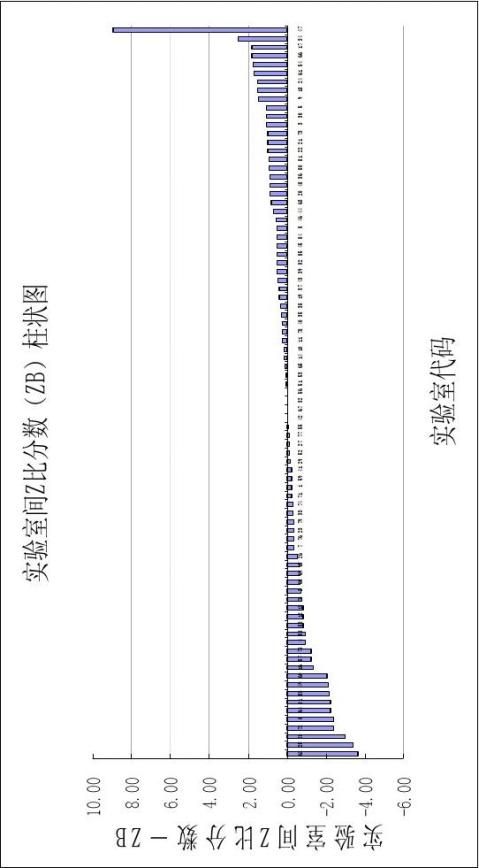
- 16
实验室内Z比分数(ZW)柱状图

- 17
附录A3 尤登图
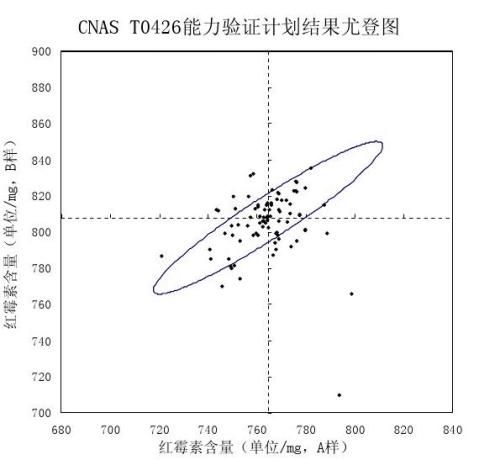
- 18
附录 B
样品制备和均匀性检验、稳定性情况
- 19
附录B1
样品制备报告
本次能力验证计划为分割水平对设计,2个样品分别定义为A样和B样。A样是普通琥乙红霉素原料,B样是琥乙红霉素精制原料。
在温度为20±2℃、相对湿度≤50%的环境下,将以上两种原料按预定的程序分两天分装到玻璃瓶,轧铝盖,各得140瓶,每瓶约1.6g。每个参加实验室按单盲分配表获得“A样”和“B样”各一瓶。
- 20
附录B2
均匀性检验报告
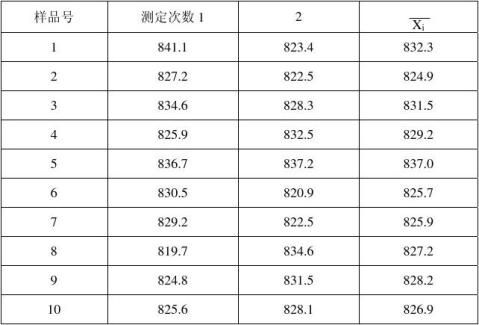
随机抽取A、B两种样品各10瓶,按作业指导书推荐的中国药典20xx年版二部方法,采用抗生素微生物检定法测定琥乙红霉素的含量,每瓶在重复性条件下测定2次。每组样品测定的顺序为:第一次:1,3,5,7,9,2,4,6,8,10;第二次:10,9,8,7,6,5,4,3,2,1。并分别用该瓶样品的水分值进行折干计算。采用单因子方差分析法对检验结果进行统计处理,结果表明样品的均匀性均满足要求,具体数据见后。
单因子方差分析:按照无水物计算各样品红霉素单位数据分别为:
样品A数据
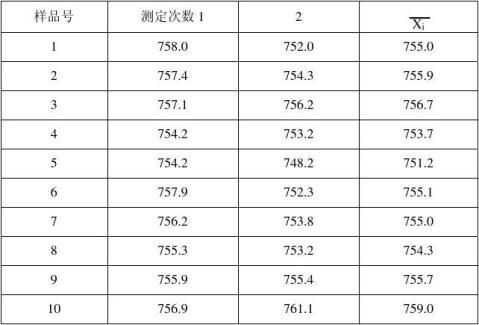
全部样品A的测试的总平均值
测定总次数N=20
样品间平方和
样品内平方和 Q1=∑ni(xi?x)2=7.2748E+01 i=1mx=∑xi/m=755.1 i=1Q2=∑∑(xij?xi)2=7.1420E+01
i=1j=1mni
自由度υ1=m?1=10-1=9
- 21
自由度υ2=N?m=20-10=10 Q1
统计量F=υ1
Q2=(7.2748E+01/9)/(7.1420E+01/10)=1.13
υ2
F临界值F0.05(9,10)=3.02,统计量F小于此值,这表明在0.05显著性水平时,样品A是均匀的。
样品B数据
全部样品B的测试的总平均值
测定总次数N=20
样品间平方和
样品内平方和 Q1=∑ni(xi?x)2=2.5271E+02 i=1mx=∑xi/m= 828.8 i=1Q2=∑∑(xij?xi)2=4.1454E+02
i=1j=1mni
自由度υ1=m?1=10-1=9
自由度υ2=N?m=20-10=10
Q1
统计量F=υ1
Q2=(2.5271E+02/9)/(4.1454E+02/10)=0.68
υ2
F临界值F0.05(9,10)=3.02,统计量F小于此值,这表明在0.05显著性水平时,样品B是均匀的。
- 22
附录B3
稳定性情况说明
查阅相关资料,琥乙红霉素稳定性良好,经加速试验考察3个月,各项指标无明显变化。本次能力验证从发送样品到回收结果报告仅有一个多月的时间,在这段时间内样品的稳定性能满足要求。
- 23
附录 C 相关文件(被测物品接受状态确认
表和作业指导书)
C1 被测物品接收状态确认表
C2 作业指导书
- 24
附录C1
被测物品接收状态确认表
编号:ZQ - 能力验证计划名称 CNAS T0426《抗生素微生物检定法测定药品含量》
组 织 机 构
发 送 机 构
电 话 / 传 真
发 送 日 期
发 送 状 态
接收实验室名称:
联系地址:
邮编:
联系电话/传真:
联系人: 接收人签名: 接收时间:
接收时,被测物品状态是否良好: 是 □ 否 □
如需要,对接收状态的详细说明:
注(此栏适用于传递被测物品的方式):
1. 请于 年 月 日前完成测试,并将被测物品于 年 月 日前传送至 (详细信息见CNAS“能力验证样品发送表”);
2. 传送被测物品时,请注意填写随附的能力验证样品发送表,并传真至指定机构
和上述实验室;
3. 注意计划的保密性,请勿向下一实验室通告本实验室的测试结果。
备注:请各实验室将填好的表格传真至指定机构。 中国合格评定国家认可委员会(CNAS) 上海市食品药品检验所 021-50798211(fax) 021-38839900-26712 20xx年6月18日 完好 □ 不完好 □ √联 系 人 杨美成 钱维清 运输单据号码 发送人签名 钱维清
- 25
附录C2
CNAS T0426《抗生素微生物检定法测定药品含量》
作业指导书
各参加实验室:
《CNAS T0426抗生素微生物检定法测定药品含量能力验证计划》是由上海市食品药品检验所负责实施的中国合格评定国家认可委员会(CNAS)的能力验证计划。本次能力验证计划中,贵实验室的代码为________。
本次能力验证计划的要求和相关信息如下:
1.样品
本次能力验证计划提供2份白色粉末样品(琥乙红霉素原料),采用玻璃瓶轧盖包装,每瓶装量约1.6g。贵实验室的样品编号分别为:“ -1”和“ -2”。样品请密封、在干燥处保存,样品打开后应尽快开展检测工作。
各实验室在收到样品时,应首先对样品是否完好、编号是否正确进行确认,同时将确认信息填写在《被测物品接收状态确认表》中以传真方式尽快返回实施机构。如收到的样品存在破损、污染等问题也请及时与实施机构联系更换事宜,并将样品寄回实施机构。
2.检测
本次能力验证计划要求实验室按照日常检测程序分别检测2份样品的含量。
推荐的检测方法为《中国药典》20xx年版二部,具体请按照“琥乙红霉素”项下的方法进行。提供的2份样品按分割水平设计,要求实验室在重复性条件下测试。
检测结果等相关信息请填写在附表1《CNAS T0426抗生素微生物检定法测定药品含量结果报告单》中,测试结果以每1mg的红霉素单位表示,并以无水物计算,结果保留至小数点后1位。
3.结果反馈
请各实验室于20xx年7月20日前,将《CNAS T0426抗生素微生物检定法测定药品含量结果报告单》原件及相关原始记录复印件邮寄到实施机构联系人(时间以当地邮戳为准)。逾期提交的结果将不列入本次计划统计。
4.保密
- 26
为对实验室的相关信息保密,本次能力验证计划为每个参加实验室提供一个代码,最终的结果报告中均使用该代码。
CNAS规定,在能力验证计划实施过程中,严禁参加实验室相互串通结果,一经发现CNAS将撤销相关项目的认可资格。
5.联系方式
参加本计划的实验室如有疑问,可与实施机构联系。联系方式如下:
实施机构:上海市食品药品检验所
地 址:上海市浦东新区张衡路1500号
邮 编:201203
联系电话:021-50798211 021-38839900-26712
传 真:021-50798211
联 系 人:杨美成 钱维清 陈祝康
E-mail: yangmeicheng@
- 27
附表1
《CNAS T0426抗生素微生物检定法测定药品含量》
结果报告单
实验室名称: 代码: 1
样品编号 红霉素含量 (按无水物计算,每1mg的红霉素单位)
-1 (1) (2) 平均值 检测方法 水解条件 对照品 (来源、批号)
培养基 (名称、厂商、批号、pH值)
试验菌 (名称、编号) 抑菌圈测量器具的品牌型号 水分(%)
所做碟数
-1:
-1(1)
-1(2)
-2
(1) (2) 平均值
温度: 放置时间:
-2:
-2(1) -2(2)
相关信息
小钢管滴加时间
(min) 参与统计碟数 可信限率
其他需要说明的情况(如有)
注:1)检测方法如上表中写不下可另附页;
2)测定结果均以效价单位计,保留到小数点后1位。
3)请于20xx年7月20日前,将结果报告单传真到实施机构。同时将该报告单原件及相关原始记录复印件邮寄到实施机构联系人(时间以当地邮戳为准)。
测试人员: 测试日期:
实验室负责人: (单位盖章)
-
28
附录 D 参考文献
1. CNAS-RL02∶2007能力验证规则
2. CNAS-GL02∶2006能力验证结果的统计处理和能力评价指南
3. CNAS-GL03∶2006能力验证样品均匀性和稳定性评价指南
- 29
