食醋中总酸量的测定
一、实验目标
1. 熟练掌握滴定管,容量瓶,移液管的使用方法和滴定操作技术;
2. 学会用传感器技术测定食醋中的总酸量;
3. 会组织中学生用传感器技术测定食醋中的总酸量教学过程。
二、实验原理
待测的食醋中醋酸及其他有机酸可换算为醋酸总量,都可以被标准的强碱NaOH溶液标定:C待测V待测=C标准V标准 。当溶液中的电解质含量恒定时,电导率亦恒定,当生成难电离物质时,电导率下降,pH传感器就是把电信号转化为化学信息来测定其中的总酸度的。
三、仪器与药品
仪器:pH传感器、数据采集器、液滴计数器、50mL酸式滴定管、电磁搅拌器、铁架台、250mL烧杯、移液管、容量瓶
药品:有色食醋原液、经标定的0.1mol/L NaOH溶液、去CO2的蒸馏水
四、实验操作过程
1.实验连接与操作
把pH传感器连接到数据采集器的3号端口上;
数据采集器速率设定为1/s;
采集数据的总数:5000;
用pH=4和pH=9的溶液进行标定;
再用pH=6的溶液验证标定结果,pH波动范围在6.70-7.00;
往酸式滴定管中注入有色食醋溶液;
再往烧杯中注入标定过的50mL NaOH溶液,把烧杯放于磁力搅拌器上,将洗干净的pH计插入到烧杯中。
如装置图所示:

在数据采集器上点击“通用”,打开右上角模板,找到SDMEM软盘,双击,找到实验模板化学酸碱中和,双击文件,稍等片刻,直到传感器的数据稳定下来。
开动磁力搅拌器,搅拌烧杯中的NaOH溶液。
打开光电门计数器,然后轻轻旋开酸式滴定管旋钮,使待测的食醋溶液一滴一滴地滴入烧杯中。
跟踪pH传感器测量数据的变化。
当pH传感器的数据刚开始变化,立即终止滴入食醋,并记录已消耗的食醋的体积。
再次滴入食醋,注意跟踪pH的变化,当数值接近滴定终点时滴入的食醋尽可能地慢。当波峰曲线出现平台时,停止滴加食醋溶液。平行测定3次。
2.数据处理
计算中和滴定过程中pH的变化量:pH初始值是多少,终值是多少,变化量是多少?
pH刚要开始改变的时候滴入的食醋的量是多少?把它与NaOH溶液完全被中和的时候消耗的食醋量作比较。
求算待测食醋中的醋酸含量:用每100mL食醋中含醋酸的质量来表示。
五、数据处理
1.pH-体积曲线图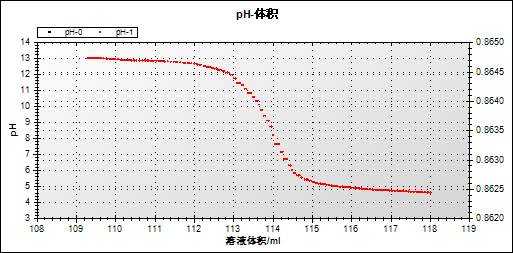
2.pH倒数图
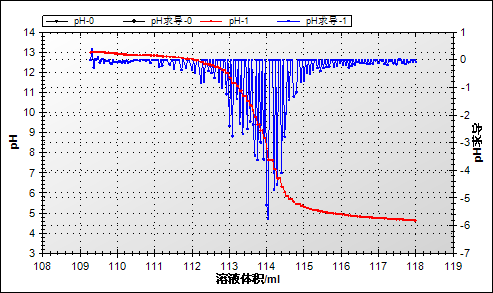
3.中和滴定过程中pH的变化量

4.中和滴定过程中醋酸用量
5. 求算待测食醋中的醋酸含量:用每100mL食醋中含醋酸的质量来表示。
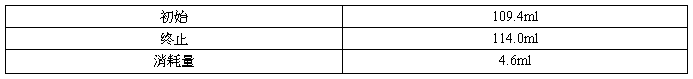
数据如下:
对pH-体积图中的最低点进行求导,得到到该点时消耗的食醋的体积约为4.6mL。已知NaOH溶液的浓度为0.1mol/L,NaOH溶液的体积为50mL。
由C待测V待测=C标准V标准 得
C待测 = C标准V标准 / V待测 =0.1mol/L*0.05L/ 0.0046 L=1.09 mol/L
故每100mL食醋中含醋酸的质量是6.54g/100mL
六、实验注意事项
1. 酸式滴定管的尖嘴要与计数器挡光孔垂直对齐,否则计数器不能感应液滴,无法正常计数。
2. 滴定速度的控制:在接近终点时,要注意放慢速度,以便观察到终点。
3. 酸碱的浓度差别不要太大,否则,实验将较难控制,结果误差较大。
4. 由于NaOH固体易吸收空气中的CO2和水分,不能直接配制碱标准溶液,而必须用标定法。
5. 注意食醋取后应立即将试剂瓶盖盖好,防止挥发。
七、实验反思
本次实验过程中,我们较好的完成了实验,但是在实验中还是有一些缺点值得下次改进。总结如下:
1.本次实验主要是学会用传感器技术测定食醋中的总酸量,作为未来的教师,我们不仅应该熟悉掌握传感器的使用及其原理,更应该掌握如何组织中学生使用传感器技术的教学过程。
2.作为一名新时代是教师,我们不能仅局限于传统的实验教学,而是应该积极关注行内动态,不断学习新知识,掌握新技能。
八、文献综述
1.传感器简介
传感器是一系列根据一定的物理化学原理制成的物理化学量的感应器具,它能把外界环境中的某个物理化学量的变化以电信号的方式输出,再经数据模拟装置转化成数据或图表的形式在数据采集器上显示并储存起来。中学化学教学中进行科学探究常用到的传感器有温度传感器、pH传感器、溶解氧传感器、电导率传感器、光传感器、压力传感器、色度传感器等。
传感器技术的特点:便携,实时,准确,综合,直观。[2]
2.实验背景
食醋的质量高低取决于其中所含醋酸量的多少。市场上销售的食醋中,既有无色的(白醋、兑制醋),又有有色的(香醋、陈醋、熏醋),它们的标牌上所标出的醋酸总含量各不相同,有的大于9g/100mL,有的大于6g/100mL,还有的标着大于等于4.5 g/100mL、4.2 g/100mL、3.5 g/100mL等等。
(1)食醋中的主要成分是醋酸,此外还含有少量的乳酸等有机酸,醋酸是弱酸,用pH试纸或酸度计测定食醋中的总酸量,总是要比实际浓度低,何因?
(2)如果用中和滴定的方法来测定食醋中的总酸量,那么如何选择指示剂?
(3)用中和滴定来测定白醋和兑制醋很好,但是测定米醋、果醋、熏醋等有色食醋的含酸量时,因其颜色比较深,能遮盖住指示剂的颜色,这样就无法看见指示剂的颜色变化,能否用蒸馏水冲稀食醋以减轻颜色的干扰,或者能否用活性炭对这类食醋作脱色处理以后滴定?加入活性炭对溶液的酸度是否有影响?
(4)克服上述不足,可以用一种称作pH传感器测定的方法来实现,该方法不怕待测物中的颜色干扰,测定既快又不用加指示剂。[1]
九、参考文献
[1]郑长龙主编.化学实验课程与教学论[M].北京:高等教育出版社,2009
[2]肖常磊,钱扬义主编.中学化学实验教学论[M].北京:化学工业出版社,2008
[3]钱扬义编著.手持技术在立刻试验中的应用研究[M].北京:高等教育出版社,2003
[4]钱扬义.手持技术在研究性学习中的应用及其心理学基础[M].北京:科学出版社,龙门书局,2006
[5]白涛等编著. 化学为什么是这样基于手持技术的数字化实验探索[M].北京:化学工业出版社,2011
第二篇:选修四学生实验报告册





(化学反应原理)班级:—————— 姓名:—————— 教师:——————
学生实验一 酸碱中和中和热测定
预习思考
◆实验目的
测定强酸和强碱反应的反应热,体验化学反应的热效应。
◆实验原理
1、中和反应原理:H+(aq) + OH-(aq)===H2O(l);△H=-57.3kJ/mol 中和热计算方法:(强酸和强碱反应) Q=mCΔt
(1)其中 Q为 ,m为 ,C为反应混合液的比热容, △t为 ; (2)因为m = V(酸)ρ(酸)+V(碱)ρ(碱),V(酸)=V(碱)=50mL,而酸的浓度是0.50 mol/L ,碱的浓度是0.55mol/L;且ρ(酸)=ρ(碱)=1 g/cm3、C=4.18 J/(g·℃),所以 ;?H??
0.418(t2?t1)
kJ/mol。
0.025
◆实验用品
大烧杯(500 mL)、小烧杯(100 mL)、温度计、量筒(50 mL)两个、泡沫塑料或纸条、 泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒、0.50 mol/L 盐酸、0.55 mol/L NaOH溶液(为了保证盐酸完全被氢氧化钠中和,采用)。
◆要点提示
1、酸和碱反应的实质是。
2、中和热实验所测得的数据若不是57.3 kJ/mol,则产生误差可能的原因有哪些?
一、记录与分析
实验时间: 年 月 日 第 节 同组成员:

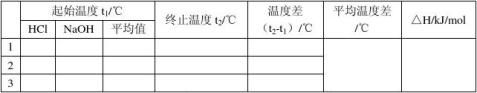
中和热测定数据表
四、问题讨论
1、中和热测定实验酸、碱混合时,为何要把量筒中的NaOH溶液一次倒入小烧杯而不能缓缓倒入?
2 大小烧杯放置时,为什么要两杯口相平?填充泡沫塑料的作用是什么?
3.实验中所用到的盐酸和氢氧化钠的物质的量比为何不是1:1,而是氢氧化钠过量?若盐酸过量行吗?
实验成绩:

学生实验二 酸碱中和滴定
预习思考
◆实验目的
1、练习使用pH计测量溶液的pH;探究酸碱中和反应过程中pH的变化特点;体会定量实验在化学研究中的作用。
◆实验原理
2、在酸碱中和反应中,使用一种的酸(或碱)溶液跟碱(或酸)溶液完全中和,测出二者的 ,再根据化学方程式中酸和碱的物质的量的比值,就可以计算出碱(或酸)溶液的浓度。 计算公式:c(NaOH)?
c(HCl)?V(HCl)c(NaOH)?V(NaOH)
或 c(HCl)?。
V(NaOH)V(HCl)
◆实验用品
1、0.1mol/L左右的盐酸、0.1mol/L左右的NaOH溶液、酚酞溶液、蒸馏水、pH计、酸式滴定管、碱式滴定管,烧杯、锥形瓶、滴定管夹、铁架台
◆要点提示
3、酸和碱反应的实质是。 4、酸碱中和滴定选用酚酞作指示剂,但其滴定终点的变色点并不是pH=7,这样对中和滴定终点的判断有没有影响?
5、滴定管和量筒读数时有什么区别?
二、记录与分析
实验时间: 年 月 日 第 节 同组成员:

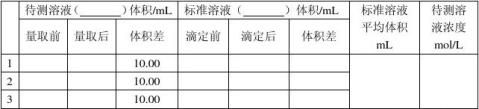
酸碱中和滴定数据表
四、问题讨论
3、酸碱中和滴定的关键是什么?
实验成绩: