电解水实验教学研究
摘要:
电解水实验是初中化学教学中的一个重要的实验,本实验从电极材料、电解液浓度和电压以及电极距进行分析,探索用简易装置在不同的条件下进行“电解水”实验时所产生的H2、O2对电解速度的影响。同时用正交试验法找到使氢、氧气体积比接近2:1的实验条件,找到最佳组合。
1 前言:
电解水实验是中学化学课本中一个非常重要的实验。该实验主要是验证水是由氢、氧两种元素组成的,实验的理论现象为:通电后,电极上出现气泡,一段时间后所收集到的氢、氧气体积比约为2:1。影响该实验的因素有以下几个:电解质种类、电解液浓度、电极材料、电极距、外加电压。通过探究的过程,利用正交实验法探究影响水电解实验的因素以及实验最佳条件。
2 实验原理:
水在通电情况下会发生水解,氢离子向负极移动,氢离子得负极电子而变成氢气,故阴极产物为氢气,而氢氧根离子向正极移动,氢氧根在水的参与下失去电子而得到氢离子和氧气,故阳极产物为氧气。其体积比为2:1,以此可以确定水的组成成分。纯水导电能力不强,电解速度慢,因此为改善这个问题,加快电解速度,可加入适量电解质来增强水的导电能力,本实验采用硫酸作为电解液,对电解液浓度,电压和电极矩三个因素进行分析比较,以便好中选优。
水在通电下总反应方程式为:2H2O 2H2↑+O2↑
2H2↑+O2↑
阴极:2H+ + 2е- ==H2↑ 阳极:4OH- _ 4е- ==2H2O+O2↑
3 仪器与试剂:
3.1仪器:
直流稳压电源、电极(铁钉、碳棒、保险丝)、饮料瓶、刻度试管(10ml)、导线、胶塞(一号)、1000ml烧杯、火柴、量筒、尺子、剪刀、秒表、酒精灯
3.2试剂: 蒸馏水、浓硫酸(98%)
4 实验部分:
(1)根据因素水平表,按正交表1 L9(34)进行实验。
(2)将饮料瓶剪成水槽状,按电极距要求打孔,装入电极,用蜡封好,检验是否密封完好。
(3)分别配置质量分数为5%、10%、15%的硫酸溶液,装入广口瓶中备用。
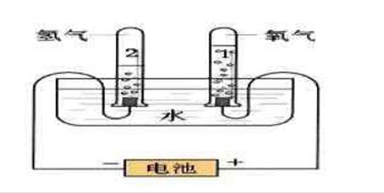
(4)按图7-1所示将饮料瓶与电极组装成简易的电解水装置。
(5)将直流稳压电源调节到所需电压,关闭。将正、负极与电极接好,打开开关并立刻计时,当负极收集的氢气为6ml时关闭开关,停止计时,读出正极收集的氧气的体积。
 图7-1:电解水简易装置图
图7-1:电解水简易装置图
表7-1 正交表1 L9(34)

表7-2 -1 反应体积比例评价标准

表7-2-2反应时间评价标准

5 结果与讨论:
5.1数据记录及处理
表7-3实验数据记录表

表7-4因素水平分析表

5.2实验结论
本文利用试验正交法探究不同的电极材料、电解液浓度、电压和电极距对实验效果的影响中,电极材料是最主要的影响因素,电极距是最次要影响因素,本实验达到最好效果的电极材料为保险丝,电解液浓度为15%的硫酸,电压为18v,电极距为4cm。
5.3 讨论
实验的理论现象为:通电后,电极上出现气泡,一段时间后所收集到的氢、氧气体积比约为2:1。但在一般情况下,氢气与氧气的体积比值一般大于2:1,原因有下面两种 :
1.氢气和氧气的溶解性的差别,氢气难溶于水,氧气不易溶于水(1L水30mL的氧气)所以一小部分氧气溶于水,比值大于2:1.
2.电极氧化消耗了一部分氧气,ρO2=1.429g/mL , ρH2=0.089g/mL
(其中氢,氧两种分子数比值:2:1;氢气,氧气的质量比值:1:8)
6 参考文献
[1] 刘怀乐.中学化学教学实证与求索[M].重庆:西南师范大学出版社.2002:
[2] 华彤文,陈景祖等. 普通化学原理(第三版)[M]. 北京:北京大学出版社.2005:
[3]中学化学教师手册编委会.中学化学教师手册[M]. 北京:科学普及出版社.1981:
[4] 王克勤,逯俊玲,左志军.酒精灯加热温度的测定研究[J].化学教学, 2003,(11):
[5] 《中学化学实验大全》《中学化学教法》《中学趣味实验》
第二篇:电解水实验的改进装置探讨
电解水实验的改进装置探讨
化学系本0802班 孙涓 王艳芳 李婧
指导教师:范建凤
电解水实验的改进装置探讨
摘要:为了验证水是由氢和氧两种元素组成的,由水的电解实验来探讨。但由于实验中气体的量比较少,现象不明显。且学生不易动手去做受到条件的限制。
关键词:电解水 改进装置
正文:
一 引言 随着中学化学实验的的普及和重要性探讨创新性实验变得十分重要,因此本次电解水实验讨论代用装置和改进变得十分有意义。
二 内容
1.实验原理
电解水装置的简单示意图如下
工作原理 由A和C两电极浸入含有Me+离子和X-离子组成溶液的电解池中,在两极的上端分别与直流电源的正、负两极接通时,直流电源便起着一个电子泵的作用;将电子压入C,又从A将电子抽回电源。由于溶液中并不存在自由电子,因此当通过电流时,在电极-溶液界面上就会发生某种或某些组分的氧化还原,使得在C处消耗电子,而在A处放出电子。这个过程就是氧化-还原反应。电极C就是通常所说的阴极(和电源负极相接),在它附近的离子或分子由于接受电子而被还原;而在阳极A处(与电源正极相接),由于离子或分子产生电子而氧化。总的电解池反应是两个电极半反应的总和。当电解进行时,离子不断向两极迁移,正离子(阳离子)向阴极迁移,负离子(阴离子)则向阳极迁移。

这种以金属盐水溶液为电解质进行提取或处理金属的电化冶金方法,简称电解,是一种将电能转变成化学能的过程。 由于水是弱电解质,故自由离子比较少,会使反应速率较慢,所以实验中加入少量的稀硫酸溶液。
阳极析氧 2H2O→O2+4H++4e
碱性溶液中 4OH-→O2+2H2O+4e
2.装置改进
方法一 使用医用5 ml注射器两个,5号电池碳棒两个,汽水瓶盖两个,500ml烧杯一个,低压电源,导线两根,木条,蜡烛一支。
电极制作如下图
(1)在木条相距4厘米间打两个小孔,大小使注射器针头刚好插入。
(2)将导线缠在碳棒两端,瓶盖的侧面孔使导线插入,上面的孔使碳棒插入,最后如图将导线和碳棒插出,为使铜丝不被电解,向瓶盖内滴蜡水将连接处密封起。

实验步骤
a) 将两个针管电极放入烧杯底部如下图
b) 拔去注射器的针头,按下图插入水中,套在碳棒上,当空气排尽后装上针头固定注射器。

c) 将导线和电极相连,接通电源后注射器内产生气泡,与负极相连的产生的是氢气先充满,与正极相连的产生的是氧气后充满。
d) 气体的检验如下图

方法二 使用两支小试管代替霍夫曼电解器的两个尖嘴管
a) 准备两支小试管,用铁丝两边弯曲用皮筋固定铁丝和试管,将铁丝挂在烧杯壁上,固定了试管如下图。
b)接通电源,收集气体,验纯同方法一
3.实验结果
酸性条件下(硫酸)
阴极H2(ml) 阳极O2(ml) 时间(s) 体积氢比氧
铅棒 4 1.9 40 〉2:1
碳棒 4 1.7 52 〉2:1
铜棒 4 0.0 150 0
因此在此条件下铅棒做电极最好
碱性条件下(氢氧化钠)
阴极H2(ml) 阳极O2(ml) 极距(cm) 时间(s) 体积氢比氧
铁棒 4 2.2 6 90 = 2:1
2.0 1 70 〈 2:1
碳棒 4 1.4 6 80 〉2:1
铜棒 4 1.8 6 50 〉2:1
因此在此条件下铁棒做电极最好并且极距越小越好
参考文献
· 傅祟说,冶金溶液热力学原理与计算,第2版,冶金工业出版社,北京,1989。
· 钟竹前等,湿法冶金过程,中南工业大学出版社,长沙,1988。
· 赵天从,重金属冶金学,冶金工业出版社,北京,1981。
