附件1:
医疗器械检验机构注册检验报告统一格式
封面
检 验 报 告
报告编号:××××
委 托 方
样品名称
型 号
检验类别 注册检验( )
注册补充检验( )
其他检验( )
国家食品药品监督管理局××医疗器械质量监督检验中心
封二
注意事项
一、报告无检测机构检验报告专用章或检验单位公章无效。
二、报告未经检测机构书面批准不得复制。
三、复制报告未重新加盖检测机构检验报告专用章或检验单位公章无效。
四、报告无批准人签字无效。
五、报告涂改无效。
六、对报告若有异议,应于收到报告之日起十五日内以书面方式向检验单位提出,逾期不予受理。
七、报告仅对来样负责。
地 址:
电 话:
传 真:
邮政编码:
首页
国家食品药品监督管理局××医疗器械质量监督检验中心
检验报告首页
报告编号: 共 页 第 页
批 准: 审 核: 检 验 :
职 务:
正文
国家食品药品监督管理局××医疗器械质量监督检验中心
检 验 报 告
报告编号: 样品编号: 共 页 第 页

正文
国家食品药品监督管理局××医疗器械质量监督检验中心
检 验 报 告
报告编号: 共 页 第 页

正文
国家食品药品监督管理局××医疗器械质量监督检验中心
检 验 报 告
报告编号: 共 页 第 页
照片页
国家食品药品监督管理局××医疗器械质量监督检验中心
检 验 报 告 照 片 页
报告编号: 共 页 第 页

第二篇:医疗器械注册产品标准格式

前 言
主要给出下列信息:
1、 说明与对应的国家标准、行业标准或国际标准的一致性程度;
2、 说明本标准编写格式符合GB/T 1.1的要求
3、 说明本标准与其它标准或前版标准的关系或代替情况(如有);
4、 必要时,说明本标准中的附录的性质。
5、 目前该产品尚无国家标准、行业标准,为规范产品的技术特性,确保产品的安全有效,特制订本注册产品标准,作为生产质量控制的依据。(此条款在无相应国家标准和行业标准时描述)
举例如下:
医用电气设备前言的描述
XXXXXXXXXXXXXXXXX是本公司生产的产品。根据《医疗器械监督管理条例》、《医疗器械标准管理办法》特制订本注册产品标准作为该产品生产、检验的质量依据。
本标准的内容遵循了国家及行业的有关XXXXXXXXXX的标准规定,标准主要技术参数的设定依据了XXXXX《XXXXXXXXXXXXX》和XXXXXXXXXX《XXXXXXXXXXX》等标准。安全要求符合GB 9706.1-2007《医用电器设备 第一部分: 安全通用要求》、XXXXXXXXXXXXXXXXXXXXXXX等标准;相关参数值的确定参考了XXXXXXXXX参数。本标准的格式符合GB/T 1.1-2009《标准化工作导则 第1部分:标准的结构和编写规则》的要求。
本标准的附录A为规范性附录。
本标准由XXXXXXXXXXXXX提出。
本标准起草单位:XXXXXXXXXXXXXXXXXXXXXXXX起草。
本标准主要起草人:XX、XXX。
本标准于XXXX年X月XXX日首次发布。
产品名称
1 范围
本注册标准适用于XXXX(产品名称)。
本注册标准规定了XXXX(产品名称)的产品分类(如有)、要求,试验方法,检验规则,标志、包装、运输、贮存等内容。
2 规范性引用文件
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。
引用标准顺序:国家标准、行业标准、国际标准。标准的排列原则:按标准编号由小到大排列。
举例如下:
GB/T 191-2008 包装储运图示标志
GB/T 10151-2008 医用诊断X射线设备 高压电缆插头、插座技术条件
GB 9706.1-2007 医用电气设备 第一部分:安全通用要求
GB 9706.11-1997 医用电气设备 第二部分:医用诊断X射线源组件和X射线管组件安全专用要求
GB 9706.12-1997 医用电气设备 第一部分:安全通用要求 三、并列标准 诊断X射线设备辐射防护通用要求
注:凡是有明确日期的标准必须标出日期,不得省略。
3 分类与命名
可包含以下内容:
a) 产品安全防护类型(适用时考虑)
b) 产品结构组成 :应明确所有组成,包括附件、选配件等
c) 产品规格型号划分依据及命名方法:规格型号可按下列规则划分(推荐使用):①按产品结构组成不同划分;②按产品基本参数或几何尺寸不同划分;③按产品功能不同划分
d) 各规格型号产品功能及基本参数(或几何尺寸)
举例如下:(适用于有源产品)
3.1安全防护类型
依据GB 9706.11-1997第5章,按防电击类型及防电击程度,X射线管组件应为由外部电源供电的I类、B型设备。
3.2 产品型号命名方法
仪器的型号标记由企业代号、产品类别号、产品设计序号组成。
XX — XX □□ □
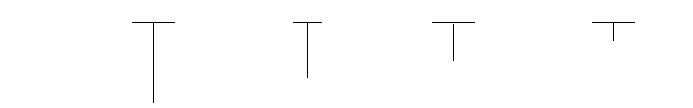
 产品功能代号(用A、C等表示,见表1)
产品功能代号(用A、C等表示,见表1)
 产品设计序号 (用两位数字表示,见表1)
产品设计序号 (用两位数字表示,见表1)
 产品类别号
产品类别号
 企业代号
企业代号
3.3 产品型号功能基本参数
本标准涉及的产品型号基本参数见表1(例)
表1 产品型号与选配表

举例如下:(适用于无源产品)
3.1 某球囊导管的产品型号示例
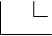 ZT - X 型
ZT - X 型
型式代号:I为四周扩张,II为双向扩张,III为单向扩张。
产品代号:ZT表示椎体(汉语拼音首字母缩写)。
3.2 分类
3.2.1 球囊导管按球囊扩张方式分为ZT-I型、ZT-II型、ZT-III型;ZT-I型为四周扩张,ZT-II型为双向扩张,ZT-III型为单向扩张。
3.3 组成
球囊导管主要由导管与导丝组成。
3.4 球囊导管的型式和基本性能参数
3.4.1 球囊导管的型式和基本性能参数(可用图和表)
4 要求
应提供安全性能及有效性能要求。其编写应考虑要求的合理性、有效性、安全性、适用性、导领性、完整性和协调性。(应充分考虑产品的使用要求和基本性能以及健康、安全、生理、环境保护因素)
1、安全性能要求
应注意选择适用下列标准:
GB 9706.1-2007 医用电气设备安全通用要求系列标准;
GB/T 16886-2003 医疗器械生物学评价系列标准;
GB 18278~GB 18280 医疗器械灭菌系列标准;
YY/T 0127 口腔材料生物评价系列标准;
及其它安全要求。
2、有效性能要求
应包括重要性能、一般性能指标及外观要求。有国家标准、行业标准的产品,其性能应符合上述标准的要求。没有国家标准、行业标准的产品,其性能应由产品制造商根据产品预期应用情况确定,并保持性能要求与说明书中明示的技术指标一致。
举例如下:(适用于无源产品)
4 要求
4.1 配置与基本尺寸
4.2 外观
4.3 物理性能
4.4 化学性能:其它性能按实际描述
4.4.1环氧乙烷残留量:产品采用环氧乙烷灭菌,其环氧乙烷残留量应不大于10ug/g。
4.5 生物性能
4.5.1 无菌:产品应无菌。
4.5.2 细胞毒性:皮肤反应不大于1级。
4.5.3 刺激性:皮肤无反应PⅡ为0.0~0.4。
4.5.4 致敏性:皮肤反应不大于1级。
举例如下:(适用于有源产品)
4.1 正常工作条件
a)环境温度范围:
b)相对湿度范围:
c)大气压力范围:
d)使用电源电压:
4.2 外观与结构
4.3 有效性能:
4.4环境试验要求:
产品应符合GB/T 14710-2009中气候环境试验I组(或II组),机械环境试验I组(或II组)的要求。产品的运输试验、电源电压适应能力试验应分别符合GB/T 14710-2009中第3章、第4章的要求。
4.5 安全要求:
应符合GB 9706.1-2007(GB4793.1-2007)等标准相关条款的要求。按照国食药监械[2008]314号文要求:医用电气设备的注册产品标准中,电气安全部分可不单独编制附录A,但须明确产品符合的电气安全国家标准或行业标准及产品主要安全特征,并按标准条款的顺序明确适用项。内容如下:
产品主要安全特征:
一、按防电击类型分类
二、按防电击的程度分类
三、按对进液的防护程度分类
四、按在与空气混合的易燃麻醉气或与氧或氧化亚氮混合的易燃麻醉气情况下使用时的安全程度分类
五、按运行模式分类
六、设备的额定电压和频率
七、设备的输入功率
八、设备是否具有对除颤放电效应防护的应用部分
九、设备是否具有信号输出或输入部分
十、永久性安装设备或非永久性安装设备
十一、电气绝缘图
具体写法可参照如下:
产品特征
仪器中的XXXXX属医用电气设备。
a)XXXXXX按防电击类型分类属于I类设备;选配的XXXXXXX为按防电击类型分类属于Ⅱ类设备。
b)XXXXXX按防电击的程度分类属于具有B型应用部分的设备;
c)XXXXXX按对进液防护程度分类属于IPX0设备;
d)XXXXXX按在与空气混合的易燃麻醉气或氧或氧化亚氮混合的易燃麻醉气情况下使用时的安全程度分类不属于AP型和APG型设备;
e)XXXXXX按运行模式分类属于间歇加载连续运行设备;
f)XXXXXX有信号输出和输入部分;;
g) XXXXXX不具有对除颤放电效应防护的应用部分;
h) 仪器的额定电压和频率:a.c.220V、50Hz
i) 仪器输入功率:KJ-1001A:260VA,KJ-1001C:120VA,KJ-1002:260VA;
j) 仪器属于非永久性安装、移动式设备;
k)电气绝缘图见附图。
附绝缘图
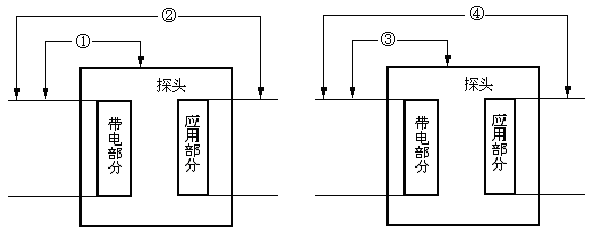
①带电部分与已保护接地的外壳之间:基本绝缘
②应用部分与带电部分之间:加强绝缘
③带电部分与未保护接地的外壳之间:辅助绝缘
④应用部分与带电部分之间:辅助绝缘
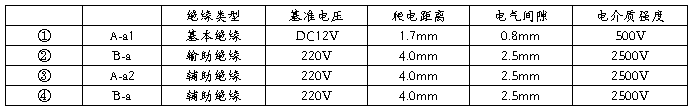
A.1.1.1 GB9706.1-2007适用项(见表A1)
表A1 GB 9706.1-2007条款
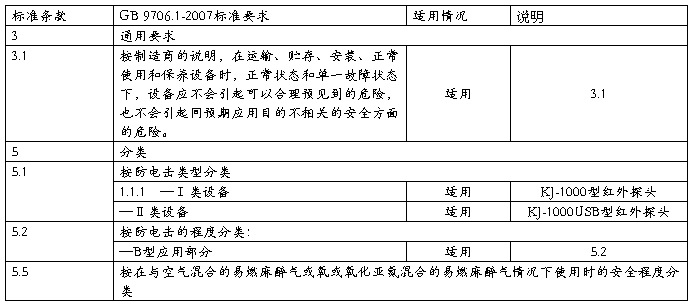
其他项目以此类推,应写明所有适用项。其他专用安全性行标国标附录按此形式提供。
5 试验方法
试验方法应与要求相对应。试验方法一般应采用已颁布的标准试验方法。如果没有现行的试验方法可采用时,规定的试验方法应具有可操作性和可再现性。试验中使用的测试仪器、设备、工具及标准样品等一般应有规定的精度等级。
举例如下:(适用于无源产品)
5 试验方法
5.1 基本尺寸:用通用量具测量
5.2 外观:在自然光线下用目力观察或仿使用操作进行检查应符合XXX的规定。
5.3 物理性能:根据实际性能制定试验方法
5.4 化学性能:(其它根据实际性能制定试验方法)
5.4.1 环氧乙烷残留量
按GB/T14233.1—2008环氧乙烷分析方法进行,应符合XXX的规定。
5.5 生物性能
5.5.1 无菌
按GB/T14233.2-2005中小型配件或实体器具的无菌试验方法进行,应符合XXX的规定。
5.5.2 细胞毒性
按GB/T14233.2—2005第8章规定的方法进行,应符合XXX的规定。
5.5.3 刺激性
按GB/T16886.10—2005第6章规定的方法进行,应符合XXX的规定。
5.5.4 致敏性
按GB/T16886.10—2005第7章规定的方法进行,应符合XXX的规定。
举例如下:(适用于有源产品)
5.1 试验条件(如有):例如环境条件、电源条件、仪表精度等
5.2 外观与结构试验
如: 以目力观察和手感检查,结果应符合XXX的要求。
5.3 性能试验
5.4 环境试验要求(此表仅供参考,应结合产品特点重新设置)
按GB/T 14710-2009规定的方法顺序及表2的要求进行试验。
表2环境试验表

5.5 安全试验
系统的安全要求验证应按照GB9706.1-2007(或者其他安全性通用要求)所有试验方法,试验结果应符合前面4.5要求。
6 检验规则
应给出下列信息:
1、产品出厂检验要求;检验内容包括项目、数量、判定规则;
(出厂检验是对正式生产的产品在交货时进行的最终检验,项目一般为非破坏性的、试验时间较短的的试验)
2、型式试验周期检查要求;检验内容包括条件、项目、数量、判定规则
(型式试验是对产品各项质量指标的全面检验,项目包括要求中的全部内容)
举例如下:(适用于有源产品)
6 检验规则
6.1 检验分类
产品检验分出厂检验和型式检验两种。
6.2 出厂检验
6.2.1 产品必须经制造厂质量部门检验合格后,并附有质量检验合格证方可出厂。
6.2.2 出厂检验为逐台检验,其检验项目为XXXXXX。
6.2.3 判定规则
检验结果若有一项不合格,则判产品不合格。
6.3 型式检验
6.3.1 有下列情形之一时,应进行型式检验:
a) 产品注册时;
b) 正式生产后,如结构、材料、工艺有较大改变,可能影响产品性能时;
c) 正常生产时,定期或积累一定产量后,应周期性进行一次性检验;
d) 产品停产一年以上,恢复生产时;
e) 出厂检验结果与上次型式检验有较大差异时;
f) 国家质量检查监督机构提出型式检验的要求时;
6.3.2 型式检验在出厂检验合格的产品中随机抽取1台,检验项目XX、XX、XX、XX。
6.3.3 判定规则
检验结果若有一项不合格,可从同批产品中加倍抽样对不合格项进行复检(电气安全要求除外),若仍不合格,则判该项型式检验不合格
举例如下:(适用于无源产品)
6 检验规则
6.1 检验分逐批检查(出厂检验) 和周期检验(型式检验)。
6 .2 逐批检验(出厂检验)
6.2.1 逐批检验按GB/T2828.1-2003的规定进行。
6.2.2 每一灭菌批的产品为一检查批。
6.2.3 抽样方案采用一次抽样,抽样方案的严格性从正常检查方案开始,其不合格分类、检查项目、接收质量限(AQL)和检查水平按表X的规定。
表X 逐批检查抽样方案
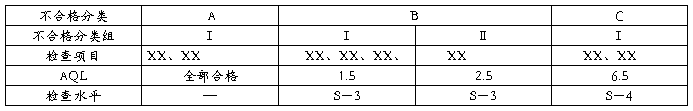
6.3 周期检验(型式检验)
6.3.1 在下列情况之一时,应进行周期检验:
a) 产品注册时;
b) 正常生产时每年一次;
c) 材料来源或配方、工艺改变时。
d) 国家监督管理部门要求时。
e) 停产一年以后再投产时。
6.3.2 周期检验项目为第4章的全部项目。
6.3.3 周期检验应从逐批检验合格的产品中随机抽取××支。
6.3.4 周期检验中若有一顶不合格则判该次周期检验不合格。
7 标志
7.1 标志:产品上应有下列标志
a) 制造厂单位名称、产品名称、规格型号;
b) 生产日期;
c) 产品编号;
d) 注册产品标准号;
e) 产品注册号。
7.2 合格证上应至少提供下列信息:
a) 制造厂名称;
b) 产品名称;
c) 检验员代号;
d) 检验日期;
7.3 产品单包装上应至少提供下列信息:
a) 制造厂名称和商标;
b) 厂址;
c) 产品名称、型式、规格;
d) 数量;
e) 注册产品标准号;
f) 产品注册号;
g) 出厂日期;
h) 产品编号、生产许可证号及生产批号。
7.4 运输标志应符合GB/T 191-2008和YY 0466的规定。
箱上的字样和标志应能保证不因历时较久而模糊不清。
8 使用说明书的编写应符合GB/T 9969-2008 《工业产品使用说明书 总则》和《医疗器械说明书、标签和包装标识管理规定》。
9 包装
举例如下:
XXXX(产品名称)应装在以泡沫塑料防护的包装箱中,箱内应有防潮、防震措施并附有全套附件、使用说明书及合格证。
10 运输
举例如下:
XXXX(产品名称)允许使用一般交通运输工具,但须防止运输过程中的剧烈冲击、震动及雨雪淋溅。也可按合同要求进行。
11 贮存
举例如下:
包装后的XXXX(产品名称)应贮存在相对湿度不大于80%、无腐蚀性气体、通风良好的室内。
———————————
编 制 说 明
一、与人体接触的材料是否已在临床上应用过,其安全性、可靠性是否得到证明:
1) 已应用于临床——大家公认的(输液器、心脏瓣膜);
2) 刚开始应用,未普及——(提供证明材料、在专业、行业、刊物上发表、临床单位应用其安全性、可靠性得到证明);
3) 新材料——必须进行生物学评价。
二、引用或参照的相关标准和资料:
引用文件的排列顺序:GB、YY、ISO、IEC标准等,并按标准的顺序号排列。
三、管理类别确定的依据:
1) 产品分类目录;
2) 产品分类规则。
四、产品概述及主要技术条款确定的依据:
(针对主要性能、使用性能、安全性能)
1) 产品概述(结构、工作原理、预期目的和用途);
2) 强制性标准执行情况的说明或者推荐性标准执行情况说明。
3) 风险分析与评价——结合对应的指标。
(器械审评科提供)
