20##届高三化学实验专题复习1
一、 萃取与分液
1.原理
(1)萃取
利用物质在互不相溶 的溶剂里 溶解度 的不同,用一种溶剂把物质从它与另一种溶剂所组成的溶液里提取出来的方法。
(2)分液
将 互不相溶 的液体分开的操作。
2.主要仪器: 铁架台 、 分液漏斗 、 烧杯 。
3.用四氯化碳萃取碘水中的碘
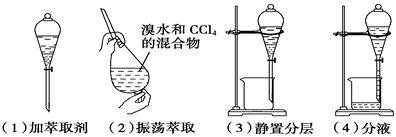
(1)加萃取剂
用量筒量取10 mL碘的饱和水溶液,倒入 分液漏斗 ,然后再注入4 mL四氯化碳,盖好玻璃塞,发现溶液分层。 四氯化碳 在下层。
(2)振荡萃取
用右手压住分液漏斗口部 ,左手握住活塞 部分,把分液漏斗倒转过来振荡,使两种液体充分接触;振荡后打开活塞,使漏斗内气体放出。
(3)静置分层
将分液漏斗放在铁架台上静置,液体分层。上层为水,无色;下层为 碘的四氯化碳溶液 ,显 紫 色。
(4)分液
待液体分层后,将分液漏斗上的塞子打开(或使塞上的凹槽 对准漏斗上的小孔),再将分液漏斗下面的活塞 拧开,使下层液体沿烧杯壁 流下。上层液体从分液漏斗上口倒出。
【思维拓展】分液漏斗中有苯和水两层无色液体,设计简单实验探究哪层液体为水层?
答案:向分液漏斗中加入一定量的水,哪层液体增加,该层液体即为水层。
4.结合用CCl4萃取碘水中的碘的实验,总结萃取剂选择应遵循的原则是什么?
答案 萃取剂选择的基本原则:
(1)溶质在萃取剂中的溶解度远大于 在原溶剂中的溶解度。
(2)萃取剂与原溶剂互不相溶 。
(3)萃取剂与原溶液中的溶质、溶剂互不反应 。
例题1:用CCl4从碘水中提取碘并进行分液,其实验步骤分为如下几步:
①把盛有溶液的分液漏斗放在铁架台的铁圈上
②把50mL碘水和15mLCCl4加入漏斗中,盖好玻璃塞
③检验漏斗是否漏水
④倒转漏斗用力振荡,并不时放气,最后关闭活塞,把漏斗放正
⑤旋开活塞,用烧杯接收溶液
⑥从分液漏斗上口倒出上层液体
⑦将漏斗上口的玻璃塞打开
⑧静置、分层 正确的操作顺序是:____________________________________
例题2、现有四氯化碳、苯和酒精哪种物质可以将溴单质(Br2)与水分离?原理?
向溴水中加入__________时,出现分层现象,但加入_________时不会出现分层。
向溴水中加入苯时,上层为________层,呈_________色,下层为______层,呈______色。
向溴水中加入四氯化碳时,上层为为________层,下层为_________层。
【讨 论】溴易溶于酒精,为什么不能用酒精将溴水中的溴萃取出来?
【配套练习】
1.下列混合物的分离和提纯方法中,主要是从溶解性的角度考虑的是( )
A.蒸发 B.蒸馏 C.过滤 D.萃取
2.在使用分液漏斗进行分液时,正确的操作是( )
A.上层液体经漏斗下方活塞放出
B.分离液体时,将漏斗拿在手上进行分离
C.分离液体时,分液漏斗上的小孔与大气相通时打开活塞
D.分液漏斗中盛装的是液体,振荡后不必扭开活塞把气体放出
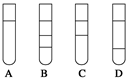 3.将体积比为1∶2的四氯化碳和碘水在试管中充分混合后静置。下列图示现象正确的是( )
3.将体积比为1∶2的四氯化碳和碘水在试管中充分混合后静置。下列图示现象正确的是( )
4.下列实验中用错试剂的是( )
A 用稀盐酸清洗做焰色反应的镍铬丝
B 用酒精萃取碘水中的碘
C 用稀硝酸洗去残留在试管壁上的铜
D 用碱石灰吸收氨气中的水蒸气
5.下列实验操作中错误的是( )
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.蒸馏时,应使温度计水银球靠近蒸烧瓶支管口
C.滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面
D.称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中
6.以下实验装置一般不用于分离物质的是( )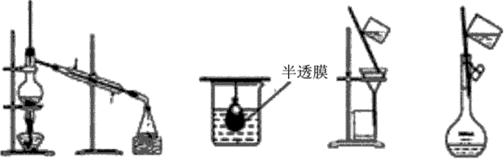
A、 B、 C、 D
7.海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验: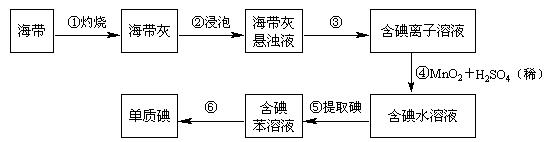
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法: 。
8.某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的硅酸盐质实验仪器有_______________(填代号,限填3项)。
A、试管 B、瓷坩埚 C、坩埚钳 D、铁三角架
E、泥三角 F、洒精灯 G、烧杯 H、墨筒
(2)第2步:Iˉ溶液的获取。操作是_________________________________________。
(3)第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用_________(填代号)。
A、浓硫酸 B、新制氯水 C、KMnO4溶液 D、H2O2
理由是__________________________________________________________________。
(4)第4步:碘单质的检验。操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘。
萃取与分液参考答案:1D 2C 3C 4B 5C 6D
7.(1)BDE (2)过滤 蒸馏
(3)2I-+MnO2+4H+=Mn2++I2+2H2O
(4)苯与水互不相溶;碘在苯中的溶解度比在水中大
(5)取少量提取碘后的水溶液于试管中,加入几滴淀粉试液;观察是否出现蓝色(如果变蓝,说明还是单质碘)
8.(1) B E F
(2)将灰烬转移到烧杯中,加适量蒸馏水,用玻棒充分搅拌,煮沸,过滤
(3) D (4)过氧化氢是绿色氧化剂,在氧化过程中不引进杂质、不产生污染(不会进一步氧化单质碘)
第二篇:连续液液萃取
方法3520C[1]
连续液液萃取
1.0适用范围
1.1本方法主要介绍了从液相样品中分离有机物的步骤。同时,本方法也介绍了第四章4.3节中所讲到的恰当的具有决定性步骤的萃取的预处理——浓缩技术。
1.2本方法适用于各种色谱分析预处理中不溶于水或微溶于水的有机物的分离或浓缩。
1.3方法3520使用密度稍大于样品的溶剂进行萃取,而连续萃取法使用密度略小于样品的溶剂进行萃取。化验品在使用仪器进行样品萃取前必须确认自动萃取仪器的有效性。
1.4本方法只限于专业化验员或在专业化验员的监督下使用。每位化验员必须具有出具可验收结果的能力。
2.0方法概述
2.1萃取样品的体积通常是1L,根据需要调整到特定的pH值(见表一),把样品放入连续液液萃取仪中用有机溶剂进行萃取。一般萃取时间18~24小时。
2.2萃取物经过干燥、浓缩(如有必要),使用合适的溶剂清洗并进行测定(溶剂根据需要选定,可参见表一)。
3.0方法干扰
3.1参见方法3500。
3.2在萃取条件下某些萃取物可能会分解。有机氯农药可能脱氯,邻苯二甲酸酯可能发生置换反应,酚类物质可能反应形成单宁酸盐。在方法3510中,这些反应随着pH的升高而加快,随着反应时间的缩短而减小。方法3510比方法3520更适合分析这几类化合物。然而,应用方法3520,在酸性环境条件下执行基础萃取方法时,可尽量回收酚类物质。
4.0仪器和材料
4.1连续液液萃取器:配备聚四氟乙烯或玻璃连接接头和无需润滑的旋塞(Kontes584200-0000,584500-0000,583250-0000,或同级品)
4.2干燥柱:为内径20 mm的硼硅酸耐热玻璃色谱柱,底部装有硼硅酸耐热玻璃棉,配备聚四氟乙烯活塞。
注意:烧结多孔玻璃盘难以清除高污染萃取物通过后形成的污染,应使用无釉料柱。可用小块硼硅酸耐热玻璃玻璃棉保留吸附剂。应先后用50mL丙酮、50mL洗脱溶剂对放入色谱柱的玻璃棉进行预清洗。
4.3 K-D(Kuderna-Danish)仪
4.3.1浓缩管:10mL刻度管(Kontes K-570050-1025或同级品),需配磨砂玻璃塞以防止提取物蒸发。
4.3.2蒸馏瓶:500mL(Kontes K-570001-500或同级品),用弹簧管、夹子或类似附件与浓缩管进行连接。
4.3.3斯奈德柱:三分球式(Kontes K-503000-0121或同级品)。
4.3.4斯奈德柱:二分球式(KontesK-569001-0219或同级品)。
4.3.5弹簧:½英寸(Kontes K-662750型或同级品)。
备注:在需要使用K-D蒸发浓缩器的浓缩程序中,推荐使用以下玻璃器皿回收溶剂。各州或当地政府管理挥发性有机物气体排放的法令中可能需要包括这些仪器。环境保护署推荐采用此类型的回收系统来执行排放减量项目。溶剂回收是遵守废弃物减量和防止污染的一项措施。
4.4溶剂蒸汽回收系统:(Kontes K-545000-1006或K-547300-0000型,A级玻璃6614-30或同级品)。
4.5沸腾片:用于溶剂萃取,约10/40目(材质为碳化硅或同级品)。
4.6恒温水槽:加热用,有同心环盖,能够控制温度(±5℃),水槽应该在通风橱内使用。
4.7小瓶:容量为2mL,配备聚四氟乙烯线型螺纹盖,或者卷曲的顶部。
4.8 pH试纸:pH测量范围包含萃取物pH。
4.9加热套:可变阻控制。
4.10注射器:体积5mL。
5.0试剂
5.1所有测试用到的化学药品均为化学纯,除非有特别说明,所有的试剂必须符合美国化学协会分析试剂委员会指定的规格。其它等级的试剂如果纯度足够高,使用时不会降低测试的准确度,则也可以使用。
5.2不含有机物的水:本方法中提到的水都是不含有机物的水,见本手册第一章的定义。
5.3氢氧化钠溶液,NaOH,10N:称取40g NaOH,用不含有机物的水溶解并稀释到100mL。此溶液用于在不显著改变样品体积(变化<1%)条件下调节样品pH值。也可配制成其他浓度。
5.4无水硫酸钠,Na2SO4,颗粒状:放在浅盘中在400℃下加热4小时干燥。也可以使用二氯甲烷预清洗,但同时必须进行空白实验,以确认硫酸钠中不存在干扰。
5.5 硫酸,H2SO4,体积比1/1:缓缓将50mL浓硫酸(比重1.84)加入到50mL不含有机物的水中。此溶液用于在不显著改变样品体积(变化<1%)条件下调节样品pH值。也可配制成其他浓度。
5.6萃取/交换溶剂:所有的溶剂都是农药等级或是同等级的试剂。
5.6.1 二氯甲烷,CH2Cl2,沸点39℃。
5.6.2 己烷,C6H14,沸点68.7℃。
5.6.3 2-丙醇,CH3CH(OH)CH3,沸点82.3℃。
5.6.4 环己烷,C6H12,沸点80.7℃。
5.6.5乙腈,CH3CN,沸点81.6℃。
6.0样品的收集、储存和处理
见《有机分析物》第4.1节的介绍说明。
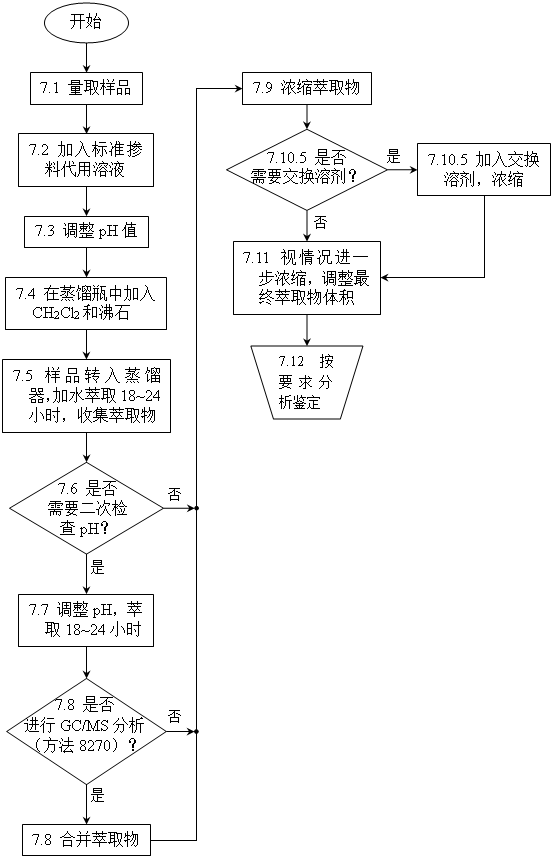
7.0操作程序
7.1用量筒量取大致1L的样品。如果样品总量不足,则在样品瓶外壁标出样品液面高度。如果样品浓度较高,可取少量样品用水稀释到1L再进行测定,或者更好的方法是使用一个小号样品瓶进行实验。
7.2 加入1.0mL标准掺料代用溶液并混合均匀(代用标准物质及基体溶液选择和配制详见方法3500)。
7.2.1 每个批次掺料样品,都需要加入1.0mL基体掺料标准溶液。
7.2.2 如果使用方法3640进行凝胶提纯,则标准掺料代用溶液用量应加倍,因为在凝胶渗透色谱法设备中,一半萃取物被放弃。
7.3 使用广泛pH试纸检查样品pH值,并视情况用1:1H2SO4(体积比)或10N NaOH调整到表1给出的值。可以使用更低浓度的H2SO4或NaOH,但须保证样品溶液体积不发生显著改变(~1%)。
7.4 在蒸馏瓶加入300~500mL二氯甲烷,并放入几块沸石。
7.5 定量将样品转入萃取装置,以少量二氯甲烷冲洗样品瓶,合并洗液。萃取18~24小时(可视情况加入不含有机物的水)。
7.6 萃取完成后,冷却萃取物。如果不需要二次萃取,则按照7.10~7.11节操作浓缩萃取物。
7.7 如果需要二次萃取,则按表1要求,在小心搅拌同时调整pH值。如果需要进行独立分析测试(参见7.8节),则将萃取装置与另一装有500mL二氯甲烷的蒸馏瓶连接,进行二次萃取,萃取18~24小时。
7.8 如果进行GC/MS分析(方法8270),可以根据情况将酸/中性萃取物与碱性萃取物合并测试,或者二者分开测试(如果实验目的是为了确定低浓度下是否存在酸/中性化合物与碱性化合物,就必须进行分开测试)。
7.9 如有必要,使用K-D浓缩器对萃取物进行浓缩(参见7.10.1~7.10.6小节)。
7.10 K-D浓缩技术
7.10.1 用4.3节提供的材料组装K-D浓缩器,将1个10mL的浓缩管接到500mL的蒸馏瓶上。
7.10.2遵照仪器生产商的指导,将溶剂蒸汽回收玻璃器皿(浓缩和收集装置,参见4.4节)与K-D仪器的斯奈德柱连接。
7.10.3将萃取物通过含有约10cm无水硫酸钠的干燥柱,将收集到的干燥萃取物加入至K-D浓缩器中,使用20~30mL二氯甲烷清洗萃取烧瓶及硫酸钠柱,合并洗液。
7.10.4 在蒸馏瓶中加入一两块干净沸石,接上三球的斯奈德柱,往斯奈德柱顶加入约1mL二氯甲烷湿润,将K-D装置放入热的恒温水槽中(温度应比溶剂的沸点高15~20℃),使浓缩管部分地浸入热水中,而蒸馏瓶的整个圆形底部则完全浸入在热的蒸汽中。按照需要调节仪器在竖直方向上的位置和水的温度,10-20分钟内完成浓缩。在适当的蒸馏速度下,斯奈德柱的球形部分会快速振动作响,但是腔内没有液体流动。当液体的体积明显达到1-2mL时,将K-D装置从水浴中取出,让液体冷却回流至少10分钟。
7.10.5 如果需要交换溶剂(参见表1),则快速移开斯奈德柱,加入约50mL交换溶剂和一块新的沸石,重新接上斯奈德柱。交换溶剂也可以在水浴加热时直接从斯奈德柱的顶部直接注入。然后按7.10.4所述,将萃取物浓缩。如果有必要,提高水浴的温度来维持合适的蒸馏。
7.10.6移开斯奈德柱,用1-2mL的二氯甲烷或交换溶剂冲洗烧瓶及其底部与浓缩器的接口,洗液并入浓缩管中。如果有硫的晶体析出,可按照方法3660进行净化。萃取物如果过多,可使用7.11节所述的技术进一步浓缩,否则使用最后一次使用的溶剂调节体积至10.0mL。
7.11 如果按表1所示,需要进行进一步浓缩,可使用微斯奈德柱技术(7.11.1)或氮气吹脱技术(7.12.2)调节萃取物至最终需要的体积。
7.11.1微斯奈德柱技术
在浓缩管中加入一两块干净的沸石,然后接上一个两球的微斯奈德柱,往柱的顶部加入约0.5mL二氯甲烷湿润,将K-D装置放入热的水浴槽中,使浓缩管部分地浸入热水中。调节仪器在竖直方向上的位置和水的温度,在5-10分钟内完成浓缩。在适当的蒸馏速度下,斯奈德柱的球形部分会快速振动作响,但是腔内无液体流动。当液体的体积达到0.5mL时,将K-D装置从水浴中取出,让液体回流冷却至少10分钟。移开斯奈德柱,用约0.2mL的二氯甲烷或交换溶剂冲洗烧瓶及其底部的接口,洗液并入浓缩管。最后利用溶剂将最终体积调节至表1中给出的数值。
7.11.2 氮气吹脱技术
7.11.2.1将浓缩管放入至约35℃的恒温水槽中,用清洁干燥(经活性炭柱过滤)的氮气流缓慢地吹拂,将溶液的体积挥发至所需要的体积。
注意:在活性炭管道与样品之间不可使用塑料管,否则可能会引入污染。
7.11.2.2在操作过程中,管的内壁必须使用合适的溶剂冲洗数次。在挥发过程中应正确放置试管,防止冷凝水进入样品中(例如,溶剂的液面应处于水槽表面以下)。在正常的操作条件下,萃取物不允许干透。
注意:当溶剂的体积减少至1mL之下时,半挥发性的分析物可能会损失掉。
7.12最终获得的萃取物可使用合适的有机分析方法(见本章4.3节)进行分析。如果萃取物不能立即进行进行分析,则应塞上塞子冷藏,若储藏时间超过2天,则应转移至有聚四氟乙烯线型螺纹盖或卷曲顶端的小瓶中,并作好标示。
8.0品质控制
8.1任何的空白实验、基体掺料或重复样品都应该同实际样品使用相同的分析程序。
8.2参考第一章相关的品质控制程序,萃取和样品的制备程序参照方法3500。
9.0方法性能
性能数据详见测试方法。
10.0参考资料
无。
表1 不同测试方法的萃取条件
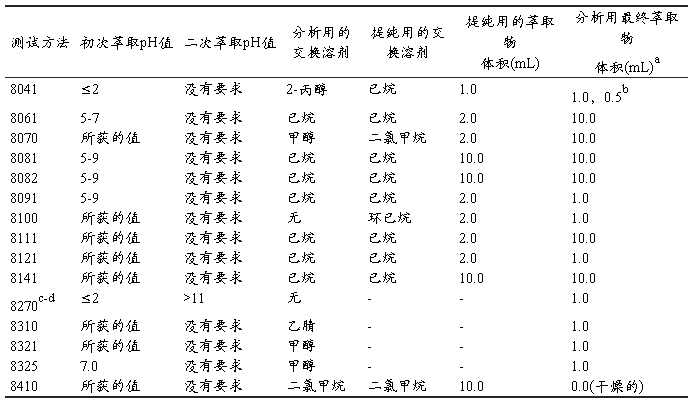
a 用于最终萃取体积为10.0mL的方法。为了达到更低的检测限,可以将体积减少至1.0mL。
b 酚类可以使用方法8041进行分析,将1.0mL 2-丙醇的萃取物利用气相色谱-火焰离子化检测器(GC/FID)技术检测。方法8041也包含一个供选择的酚类的衍生程序,此程序会产生0.5mL的已烷萃取物,利用气相色谱-电子捕获检测器(GC/ECD)技术检测。
c 气质联用技术的特点使得不需要提纯萃取物。如果需要提纯,请参照方法3600相关的程序作为指导。
d 按照不同pH控制萃取进程,可以更有效分离酸/中性成分,但不宜多次进行pH调整,否则可能导致某些分析物的损失。
[1] 1996年第3修订版
