中国石油大学(华东)现代远程教育
实验报告
课程名称:有机化学
实验名称:乙酸乙酯的合成
实验形式:在线模拟+现场实践
提交形式:在线提交

备注:该报告纳入考核,占总评成绩的10%。
第二篇:乙酸乙酯皂化反应实验报告
乙酸乙酯皂化反应速度常相数的测定
一、实验目的
1.通过电导法测定乙酸乙酯皂化反应速度常数。
2.求反应的活化能。
3.进一步理解二级反应的特点。
4.掌握电导仪的使用方法。
二、基本原理
乙酸乙酯的皂化反应是一个典型的二级反应:
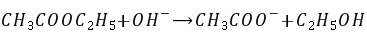 设在时间
设在时间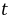 时生成浓度为
时生成浓度为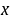 ,则该反应的动力学方程式为
,则该反应的动力学方程式为
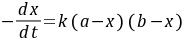 (8-1)
(8-1)
式中,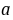 ,
,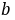 分别为乙酸乙酯和碱的起始浓度,k为反应速率常数,若a=b,则(8-1)式变为
分别为乙酸乙酯和碱的起始浓度,k为反应速率常数,若a=b,则(8-1)式变为
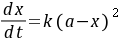 (8-2)
(8-2)
积分上式得: 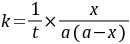 (8-3)
(8-3)
由实验测的不同t时的x值,则可根据式(8-3)计算出不同t时的k值。如果k值为常数,就可证明反应是二级的。通常是作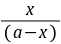 对t图,如果所的是直线,也可证明反应是二级反应,并可从直线的斜率求出k值。
对t图,如果所的是直线,也可证明反应是二级反应,并可从直线的斜率求出k值。
不同时间下生成物的浓度可用化学分析法测定,也可用物理化学分析法测定。本实验用电导法测定x值,测定的根据是:
(1)溶液中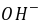 离子的电导率比离子(即
离子的电导率比离子(即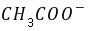 )的电导率要大很多。因此,随着反应的进行,
)的电导率要大很多。因此,随着反应的进行,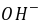 离子的浓度不断降低,溶液的电导率就随着下降。
离子的浓度不断降低,溶液的电导率就随着下降。
(2)在稀溶液中,每种强电解质的电导率与其浓度成正比,而且溶液的总电导率就等于组成溶液的电解质的电导率之和。
依据上述两点,对乙酸乙酯皂化反应来说,反映物和生成物只有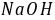 和
和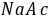 是强电解质,乙酸乙酯和乙醇不具有明显的导电性,它们的浓度变化不至于影响电导率的数值。如果是在稀溶液下进行反应,则
是强电解质,乙酸乙酯和乙醇不具有明显的导电性,它们的浓度变化不至于影响电导率的数值。如果是在稀溶液下进行反应,则
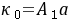
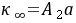
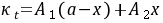 式中:
式中: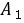 ,
,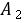 是与温度、溶剂、电解质
是与温度、溶剂、电解质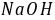 和
和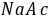 的性质有关的比例常数;
的性质有关的比例常数;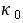 ,
,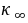 分别为反应开始和终了是溶液的总电导率;
分别为反应开始和终了是溶液的总电导率;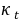 为时间t时溶液的总电导率。由此三式可以得到:
为时间t时溶液的总电导率。由此三式可以得到:
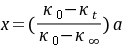 (8-4)
(8-4)
若乙酸乙酯与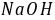 的起始浓度相等,将(8-4)式代入(8-3)式得:
的起始浓度相等,将(8-4)式代入(8-3)式得:
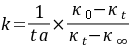 (8-5)
(8-5)
由上式变换为:
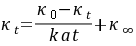 (8-6)
(8-6)
作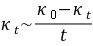 图,由直线的斜率可求k值,即
图,由直线的斜率可求k值,即
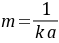 ,
, 由(8-3)式可知,本反应的半衰期为:
由(8-3)式可知,本反应的半衰期为:
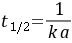 (8-7)
(8-7)
可见,两反应物起始浓度相同的二级反应,其半衰期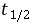 与起始浓度成反比,由(8-7)式可知,此处
与起始浓度成反比,由(8-7)式可知,此处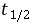 亦即作图所得直线之斜率。
亦即作图所得直线之斜率。
若由实验求得两个不同温度下的速度常数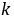 ,则可利用公式(8-8)计算出反应的活化能
,则可利用公式(8-8)计算出反应的活化能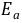 。
。
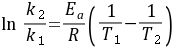 (8-8)
(8-8)
三、仪器和试剂

四、操作步骤
1.准确配制0.02 的
的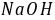 溶液和
溶液和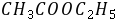 溶液。调节恒温槽温度至25℃,调试好电导仪。将电导池(如图8-1)及0.02
溶液。调节恒温槽温度至25℃,调试好电导仪。将电导池(如图8-1)及0.02 的
的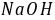 溶液和
溶液和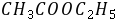 溶液浸入恒温槽中恒温待用。
溶液浸入恒温槽中恒温待用。
2.分别取适量0.01 的
的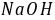 溶液和
溶液和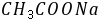 溶液注入干燥的比色管中,插入电极,溶液面必须浸没铂黑电极,置于恒温槽中恒温15分钟,待其恒温后测其电导,分别为
溶液注入干燥的比色管中,插入电极,溶液面必须浸没铂黑电极,置于恒温槽中恒温15分钟,待其恒温后测其电导,分别为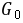 和
和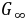 值,记下数据。
值,记下数据。
3.取20 0.02
0.02 的
的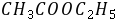 溶液和20
溶液和20 0.02
0.02 的
的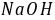 溶液,分别注入双叉管的两个叉管中(注意勿使二溶液混合),插入电极并置于恒温槽中恒温10分钟。然后摇动双叉管,使两种溶液均匀混合并导入装有电极一侧的叉管之中,同时开动停表,作为反应的起始时间。从计时开始,在第5、10、15、20、25、30、40、50、60分钟各测一次电导值。
溶液,分别注入双叉管的两个叉管中(注意勿使二溶液混合),插入电极并置于恒温槽中恒温10分钟。然后摇动双叉管,使两种溶液均匀混合并导入装有电极一侧的叉管之中,同时开动停表,作为反应的起始时间。从计时开始,在第5、10、15、20、25、30、40、50、60分钟各测一次电导值。
4.在30℃下按上述三步骤进行实验。
五、数据记录和处理
将测得数据记录于下表:
室温:18.6℃ 大气压:721.5 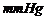
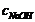 =0.01
=0.01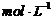
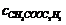 =0.02
=0.02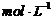
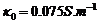

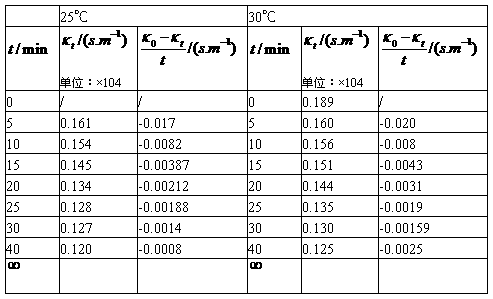
说明:其中温度为30℃时的实验数据为我小组所测,25℃时的数据是参考其他小组多得。
1.利用表中数据以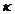 对
对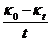 作图求两温度下的
作图求两温度下的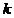 。
。
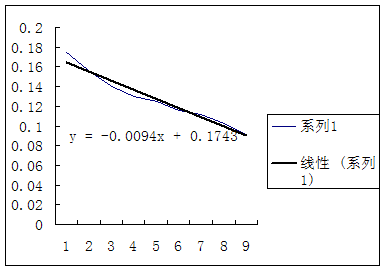
25℃时的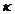 —
—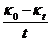 图
图
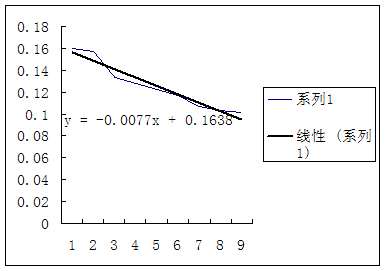
30℃时的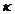 —
—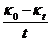 图
图
2.利用所作之图求两温度下的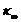 ,并与测量所得之
,并与测量所得之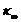 进行比较。
进行比较。
25℃:测量的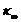 =0.1964
=0.1964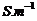 作图所得
作图所得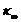 =0.1743
=0.1743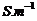
30℃:测量的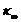 =0.1850
=0.1850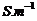 作图所得
作图所得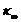 =0.1638
=0.1638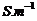
可以看出作图所求的两温度下的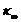 比测量值小一些,说明可能是测量时间太短,反应不完全所造成的,再就是可能数据处理存在着误差,使得结果偏小。
比测量值小一些,说明可能是测量时间太短,反应不完全所造成的,再就是可能数据处理存在着误差,使得结果偏小。
3.求此反应在25℃和35℃时的半衰期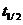 值。
值。
由图象法可以求出半衰期分别为:25℃: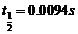 30℃:
30℃: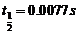
4.计算此反应的活化能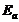 。
。
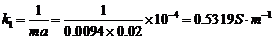
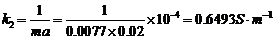
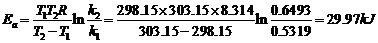
六、注意事项
1.注意每次测量之前都应该校正。
2.选择合适的量程,使得读取的数值在10~100之间。
3.进行实验时,溶液面必须浸没电极,实验完毕,一定要用蒸馏水把电极冲洗干净并放入去离子水中。
七、思考题
1.为什么以0.01 的
的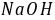 溶液和0.01
溶液和0.01 的
的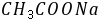 溶液测得的电导,就可以认为是
溶液测得的电导,就可以认为是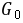 和
和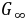 。
。
答:因为它们是强电解质,在稀溶液中,每种强电解质的电导率与其浓度成正比,而且溶液的总电导率就等于组成溶液的电解质的电导率之和。
2.为什么本实验要在恒温条件下进行?而且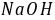 溶液和
溶液和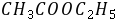 溶液在混合前还要预先恒温?
溶液在混合前还要预先恒温?
答:不同温度条件下所得速率常数不一样。保证温度的均一性,使得所测速率常数更加准确。
3.如何从实验结果来验证乙酸乙酯皂化反应为二级反应?
答: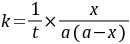 (8-3)
(8-3)
由实验测的不同t时的x值,则可根据式(8-3)计算出不同t时的k值。如果k值为常数,就可证明反应是二级的。通常是作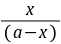 对t图,如果所的是直线,也可证明反应是二级反应,并可从直线的斜率求出k值。
对t图,如果所的是直线,也可证明反应是二级反应,并可从直线的斜率求出k值。
