生理学实验手册
EXPERIMENT MANUAL FOR PHYSIOLOGY
专业及班级:
学 号:
姓 名:
组 别:
天津医科大学临床医学院生理学实验室
实验一 标本制备及BL-410生物机能实验系统的使用
Experiment 1 Preparation of specimens and the use of BL-410 biological function of experimental system
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【实验目的】
掌握制备坐骨神经-腓肠肌标本的操作技术,为此后有关的神经肌肉实验打下基础;熟悉BL-410生物机能实验系统的使用。
【实验原理】
蛙或两栖类动物的一些基本生命活动及生理功能与温血动物近似,而且其离体组织需要的生活条件非常简单,易于控制和掌握。因此在生理学实验中,坐骨神经-腓肠肌标本是研究神经肌肉生理最常用的对象,经常用来研究神经肌肉的兴奋性、刺激与反应的规律、肌肉收缩的特点、兴奋性的周期性变化等。
【实验器材和药品】
蛙类手术器械一套(金属探针1根,粗剪刀、眼科剪刀各1把,圆头镊子、眼科镊子各1把,玻璃分针2根),蛙板和玻璃板各1块,培养皿,滴管,废物缸、锌铜弓,丝线,棉花;任氏液。
【实验对象】
蟾蜍或蛙。
【实验方法和步骤】
1.破坏脑和脊髓(常用的有三种方法)
(1) 俯式捣毁法:是最常用的方法。以左手持蟾蜍,将其腹面朝向手心,前肢夹在食指和中指之间固定,后肢夹在无名指和小指之间固定,并用拇指按压蟾蜍头部使之下俯30~40度角;然后右手持金属探针沿蟾蜍头部的中线下划,可触及一凹陷处即为枕骨大孔。将探针从枕骨大孔垂直刺入1~1.5mm,再向前刺入颅腔,左右搅动(可感觉到探针与颅骨壁的碰击),破坏脑组织;再将探针退回至进针处,但不拔出而是转向后方刺入椎管,破坏脊髓。
(2) 仰式捣毁法:将蟾蜍仰卧于蛙板上,拉开下颌,右手持探针在颅底两眼之间向前下刺入颅腔,用探针在颅腔内向四周捣毁脑组织,然后将探针退至粘膜下,针尖向后平行刺入椎管内以破坏脊髓。
(3) 横断脊柱后捣毁法:左手持蟾蜍,右手持粗剪刀,在两腋窝稍下横断脊柱,然后在脊柱呈白色的脊髓断面处,向上插入探针破坏脑,再向下插入探针破坏脊髓。
以上方法破坏脑和脊髓成功后,蟾蜍出现四肢(尤其是后肢)瘫软,并常有尿失禁现象。
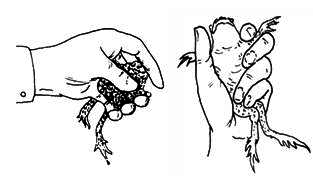
Schematics for handing of toad
2.剪去躯干上部及内脏 用粗剪刀在两侧腋部稍下(或在骶髂关节以上1.5 ~ 2cm处)剪断脊柱,用左手握住蟾蜍后肢,拇指按压骶骨,使蟾蜍头部及内脏自然下垂;避开腰骶神经丛后,右手用粗剪刀沿脊柱两侧剪开腹壁,在耻骨联合处将躯干上部及内脏剪掉,弃入废物缸内。
3.剥皮 左手持大镊子夹住脊柱断端 (小心勿伤神经),右手捏住脊柱断端的皮肤边缘,逐步向下剥去全部后肢皮肤。将剥好的标本放置在盛有任氏液的培养皿中,或置于洁净的玻璃板上,滴加任氏液备用。然后洗手并清洗用过的手术器械。
4.分离左右腿 用圆头镊子夹住脊柱并提起,避开坐骨神经,用粗剪刀剪去向上突出的骶骨,沿脊柱正中线将脊柱从上向下分成两半,再从耻骨联合中央剪开(注意:剪开时应避免剪刀走“S”形,以保证坐骨神经的完整),将已分离的两腿浸入任氏液备用。亦可在游离大腿部位的坐骨神经后再分离两腿。
5.游离坐骨神经 取蟾蜍腿一条,用玻璃分针在大腿背面内侧沿坐骨神经沟(股二头肌与半膜肌之间)分离肌肉,暴露坐骨神经。向上将梨状肌及其附近的结缔组织剪断,然后用玻璃分针沿脊柱自上而下轻柔游离坐骨神经腹腔部(坐骨神经呈亮白色束状),用眼科剪刀剪断神经的所有分支,在近脊柱处穿线结扎,从脊柱根部将坐骨神经剪断。也可以不结扎、不剪断神经,而保留一小块与神经相连的脊柱(约0.5cm×0.5cm左右),供握持神经用。
6.游离股骨 将游离的坐骨神经轻轻搭在腓肠肌上,切断膝关节周围的大腿部肌肉,把股骨刮干净,然后剪去股骨小头并保留余下的股骨(约1~1.5cm),以便在固定神经肌肉标本时使用。
7.完成标本 用眼科镊子(或小剪刀)在跟健下方穿一洞,向上游离腓肠肌至膝关节处。穿线结扎腓肠肌跟健,左手提线,在结扎线远端剪断跟健。将膝关节以下的小腿其余部分全部剪去。以上过程应注意避免损伤神经,并随时滴加任氏液。至此即完成一个坐骨神经-腓肠肌标本的制备。
8.检查标本的兴奋性:用被任氏液浸湿的锌铜弓接触坐骨神经,如腓肠肌迅速收缩,则表示标本的兴奋性良好,可供有关神经肌肉生理实验用。
【实验要求与注意事项】
1.熟悉蟾蜍手术器械的使用方法,了解蟾蜍腿部的局部解剖及坐骨神经的走行。
2.避免损伤蟾蜍背部的腺体(尤其是眼后的大腺体),防止其分泌物溅入眼内或污染标本。
3.勿剪破蟾蜍内脏,并及时清洗手及用过的器械;已剥去皮肤的组织应避免接触蟾蜍皮肤或其他不洁物;以防标本被污染。
4.游离神经、肌肉时不可过度牵拉,应避免用手指、金属器械接触或夹持标本的神经肌肉部分,更不能用自来水冲洗标本。
5.制备过程中应经常向标本上滴任氏液,防止神经因干燥而失去正常兴奋性。标本制成后须放在任氏液中浸泡数分钟,使标本兴奋性稳定。
6.移动制备好的标本时,先将游离的神经搭在腓肠肌上,再用双手分别提拿跟键和股骨断端,防止神经受力过重。
【写出下列器械的用途】
1. 粗剪刀(scissors)
2.手术剪(surgical scissors)
3.眼科剪(ophthalmic scissors)
4.手术镊(surgical forceps)
5.眼科镊(ophthalmic forceps)
6.探针(metal probe)
7.玻璃分针(glass disselting tool)
8.锌铜弓(bimetal electrode)
9.蛙钉(frog nail)
10.双极电极(stimulating electrode)
【BL-410生物机能实验系统的使用】
1. BL-410生物机能实验系统是生理学实验中常用到生物信号记录仪器,其工作的基本原理是:首先将原始的生物机能信号进行放大、滤波等处理,然后对处理的信号通过模数转换进行数字化并将数字化后的 信号传输到计算机内部,计算机通过生物机能实验系统专用的软件对接收到的信号进行实时处理,并进行生物机能信号的波形显示和存储。
2. BL-410生物机能实验系统有多种配件,其中,生理实验中常用到的换能器有 和 。前者的原理是将生物张力信号转换成电信号输出;后者的原理是将压力的变化转化成电阻的变化产生信号输出。
3. 软件的启动,只需双击Windows操作系统桌面上的“
”图标即可启动BL-NewCentury程序。
【实验结果】
用铅笔画出蟾蜍坐骨神经-腓肠肌标本的示意图。
要求:(1)形象、美观。
(2)各个部位比例合适。
(3)标注出各个部位的名称。
【回答下列问题】
1. 损毁脑和脊髓后的蟾蜍有何表现?若破坏脊髓不彻底,蟾蜍的四肢会有什么表现?为什么?
2. 为什么在本实验中应经常给标本滴加任氏液?
实验二 刺激频率与肌肉收缩的关系
Experiment 2 The relationship between Stimulation frequency and muscle contraction
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【实验目的】
观察有效电刺激频率与肌肉反应形式的关系
【实验原理】
单收缩:当给肌肉一个阈上剌激时,肌肉即发生一次收缩反应,称为单收缩。单收缩的全过程可分为潜伏期、收缩期和舒张期。蟾蜍腓肠肌的单收缩约历时0.12秒,若给肌肉两个以上有效剌激,且使每两个剌激的间隔时间大于该肌肉单收缩的总时程,则肌肉将出现一连串各自分离的单收缩。
复合收缩:若增加刺激频率,使每两个剌激的间隔时间小于该肌肉单收缩的总时程,则引起肌肉的收缩可以总和起来,出现连续的收缩,称为复合收缩。包括不完全强直收缩和完全强直收缩。不完全强直收缩:剌激间隔短于单收缩时程而长于收缩期,即新的收缩发生于前次收缩的舒张期,肌肉的收缩反应可以融合,出现持续的锯齿状收缩曲线。完全强直收缩:继续增加剌激频率,使剌激间隔短于收缩期,每次新的收缩都产生于前次收缩的收缩期中,肌肉的收缩反应完全融合而出现一持续的收缩曲线。强直收缩产生的肌张力要比单收缩强3~4倍。
【实验对象】
蟾蜍或蛙
【实验器材和药品】
BL-410生物机能实验系统、张力换能器、刺激电极、蛙类手术器械、铁支架、培养皿、滴管、任氏液等
【实验方法】
1、制备坐骨神经腓肠肌标本,在任氏液中浸泡10min左右,使其兴奋性较稳定。
2、仪器标本连接
(1)将张力换能器固定在铁支架上,肌肉标本的股骨固定于激动器上,腓肠肌跟腱的结扎线连于张力换能器的受力片上,连线应松紧适宜,并与桌面垂直,张力换能器的输入端接BL-410系统的1通道插孔。
(2)把坐骨神经轻轻提起,放在刺激电极上。
(3)BL-410系统操作
◆ 依次选定“实验项目”→“肌肉神经实验”→“刺激频率与反应的关系 ”。
◆ 在弹出的“设置刺激频率与反应关系实验参数”对话框中选择“现代实验”或“经典实验”。若选定“经典实验”,系统将按照设置输出三组不同的刺激;若选定“现代实验”,系统以初始频率为基础,按频率阶梯数值递增刺激频率。观察收缩形式的变化。
【注意事项】
1. 每两次刺激之间必须让标本休息15秒。
2. 经常给标本滴加任氏液以维持兴奋性于良好状态。
3. 张力换能器有标志的面朝上,防止出现负张力.
【实验结果及分析】
1. 打印或画出实验所记录的结果
要求:(1)用铅笔画图
(2)标记处图形所对应的刺激频率和刺激强度
2. 根据所得实验结果,讨论分析不同刺激频率对肌肉收缩的影响机制。
【回答下列问题】
1. 不同的肌肉,引起完全强直收缩的刺激频率是否相同?为什么?
2. 同一块肌肉,其单收缩、复合收缩和强直收缩的高度是否相同?为什么?
实验三期前收缩和代偿间歇
Experiment 3 premature systole and compensatory pause
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【实验目的】
学习心脏活动曲线的描记方法,通过观察在心脏活动的不同时期给予刺激,以验证心肌兴奋性的周期性变化。
【实验原理】
心肌在经历一次兴奋后,其兴奋性会发生一系列周期性的变化。心脏的兴奋性的变化分为一下几个时期:有效不应期、相对不应期和超常期。心肌兴奋后的兴奋性变化特点是其有效不应期特别长,约相当于心动周期的整个收缩期和舒张早期。在此期间,任何强大的刺激均不能使之产生动作电位,不能发生兴奋和收缩。如果在心脏的有限不应期之后,给予心室一次人为的或起自窦房结以外的阈上刺激,便可以在正常节律性兴奋到达心室之前,引起一次扩布性的兴奋和收缩,由于该兴奋和收缩发生在正常节律性兴奋之前,称为“期前收缩”。期前兴奋也是一次心脏兴奋,也有自己的有效不应期,当紧接在期前收缩后的一次正常的节律性兴奋到达时,心肌常常正好处于期前收缩的有效不应期,因而不能引起心室的兴奋和收缩,此时心室停留舒张状态。直至下一次正常节律性兴奋到达时,才恢复正常的节律性收缩。这种期前收缩后出现的一次时间较长的舒张期,称为“代偿间歇”。
【实验对象】
蟾蜍或蛙
【实验器材和药品】
BL-410生物机能实验系统、张力换能器、刺激电极、蛙类手术器械、蛙板、蛙心夹、铁架台、双凹夹、线、小烧杯、滴管、任氏液等
【实验方法】
1、暴露心脏,在心舒期用蛙心夹夹住心尖约1毫米。
2、将蛙心夹上的连线连至张力传感器,刺激电极与心脏相接触。
【注意事项】
用蛙心夹夹住心尖时应当避免刺破心脏。
实验过程中,要经常用任氏液保持心脏的湿润。
每刺激一次心室后,要让心脏恢复2-3次正常搏动后,再行下一次刺激。
在刺激心脏之前,先用刺激电极刺激腹部肌肉以检查电刺激是否有效。
【实验操作过程】
1. 心脏的兴奋性的变化分为以下几个时期: 、 和
。
2. 心脏兴奋后的兴奋性变化特点是其有效不应期特别 ,约相当于心动周期的整个收缩期和 。
3. 期前收缩:
4. 代偿间歇:
5简要写出蟾蜍心脏暴露步骤:
【实验结果及分析】
1、剪贴记录曲线,做好标记,并分析解释实验结果。
2、根据实验结果分析心机兴奋性的周期性变化产生的原因。
实验四 ABO血型的鉴定
Experiment 4 Identification of ABO blood group
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【实验目的】
(1) 学习ABO血型的鉴定方法,观察红细胞凝集现象。
(2) 掌握ABO血型鉴定的原理。
【实验原理】
血型就是红细胞膜上特异抗原的类型。在ABO血型系统中,红细胞膜上抗原分A和B两种抗原,而血清抗体分抗A和抗B两种抗体。A抗原加抗A抗体或B抗原加抗B抗体,则产生凝集现象。用已知的凝集素即抗体,通过凝集反应的发生与否,判断红细胞膜上的凝集原的类型。在ABO血型系统,根据红细胞膜上是否含A、B抗原而分为A、B、AB、O四型。
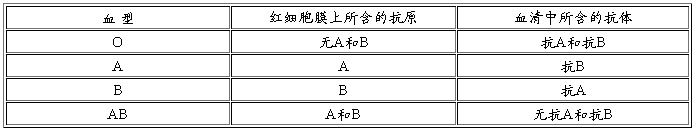
抗A、抗B血型鉴定试剂为基因工程技术生产的单克隆抗体。抗A血型鉴定试剂含抗A凝集原单克隆抗体(相当于抗A凝集素),为蓝色;抗B血型鉴定试剂含抗B凝集原单克隆抗体(相当于抗B凝集素),呈黄色。
【实验对象】
人【实验药品好器材】
75%酒精棉球、抗A、抗B血型鉴定试剂、一次性采血针、消毒棉球、消毒牙签、双凹玻片
【实验步骤】
(1)取一块清洁双凹玻片,将双凹玻片两端分别标上“A”和“B”,并在相应的小凹中加入A型(含抗B凝集原)或B型(含抗A凝集原)标准血清一滴。
(2)用75%酒精棉球消毒采血部位(耳垂或指尖),用消毒采血针刺破皮肤,用消毒牙签蘸血一滴放入A型血清内并混匀;用另一牙签蘸取血液同法放入B型血清中混匀。
(3)静置10~15min后用肉眼观察有无凝集现象。如肉眼看不清楚,可置于显微镜下观察。A侧发生凝集,则血型为B型;B侧发生凝集,则血型为A型;若两侧发生凝集,则血型为AB型;若两侧均未发生凝集,则为O型。
【注意事项】
(1)取血部位应严格消毒。
(2)牙签取血切勿过多或过少,以免影响结果判断。
(3)混匀时应分别用两支牙签,并注意防止两种血型鉴定试剂相互污染。
【实验结果及分析】
1. 画出ABO血型鉴定示意图。
2. 根据实验结果,判定受试者的血型;并讨论受试者在临床输血时能给什么血型的病人输血?能接受什么血型供血者的血液?
【回答下列问题】
1. 在运用本实验方法鉴定血型时,应注意哪些问题?
2. 经血型鉴定后,若是同型血,是否可直接输血?为什么?
实验五 人体动脉血压的测定
Experiment 5 Determination of human arterial blood pressure 同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【实验目的】
(1)学习袖带法测定动脉血压的原理和方法。
(2)测定人体肱动脉的收缩压和舒张压。
【实验原理】
血液在血管内流动和水在平整光滑的河道内流动一样,通常是没有声音的,但当血液或水通过狭窄的管道形成涡流时,则可发出声音,测量人体血压的血压计就是根据这个原理设计的。
目前临床上测量血压均采用间接测量法,最常用的方法是袖带法,所用的血压计由气球、袖带和检压计三部分组成。袖带的橡皮囊二管分别与气球和检压计相连,三者形成一个密闭的管道系统。检压计有水银柱式和弹簧式两种。
测量血压时先用气球向缠缚于上臂的袖带内充气加压,压力经软组织作用于肱动脉。当所加压力高于心收缩压力时,完全阻断了肱动脉的血流,此时在肱动脉的远端(袖带下)听不到声音,也触不到肱动脉的脉搏。由气球慢慢向外放气,袖带内的压力即随之下降,当袖带内的压力等于或稍低于心缩压时,随着心缩射血,血液即可冲开被阻断的血管形成涡流,用听诊器便开始听到搏动的声音,此时检压计所指示的压力值即相当于收缩压。继续缓慢放气,使袖带内压力逐渐降低,当袖带内压力低于心收缩压,但高于心舒张压这一段时间内,心脏每收缩一次,均可听到一次声音。当袖带压力降低到等于或稍低于舒张压时,血流复又畅通,伴随心跳所发出的声音便突然变弱或消失,此时检压计所指示的压力值即相当于舒张压。
用间接法测得的血压为一近似值,其精确程度与测量技术有一定关系。在测量时,缠缚袖带要平展,使上臂、心脏和水银检压计的零点(或弹簧检压计),尽量保持在同一水平上,并且放气不要过快,否则将出现较大的误差。
【实验对象】
人
【实验器材】
血压计、听诊器
【实验方法和步骤】
1、熟悉血压计的结构 血压计有两种,即水银柱式和表头式。常用的是汞柱式血压计。前者比较精确,后者方便携带。两种血压计均由检压计、袖带和橡皮气球三部分组成。汞柱式血压计的检压计是一个标有0~40 kPa(0~300 mmHg)(1mmHg=0.133kPa,1kPa=7.5mmHg)刻度的玻璃管,上端与大气相通,下端与水银贮槽相通。袖带是一个外包布套的长方形橡皮囊,借橡皮管分别和检压计的水银槽及橡皮球相通。橡皮球是一个带有螺丝帽的球状橡皮囊,供充气和放气之用。测压前须检查检压部分是否准确,袖带内橡皮囊与大气相通时,水银柱液面是否在零刻度线。袖带是否漏气。
表头式血压计的检压部分是以压力推动指针在表盘上旋转,此种血压计的特点是携带方便,但易失灵,须经常用水银检压计校正。
近年来又有一种新型的电子血压计在临床上应用。
听诊器有耳件、胸件和导管组成。
2、听诊法测量动脉血压
(1).受试者脱去右臂衣袖,取坐位,全身放松,右肘关节轻度弯曲,置于实验桌上,使上臂中心部与心脏位置同高。
(2).打开血压计,松开血压计橡皮球的螺旋阀,将袖带展评,排尽空气,再旋紧螺旋阀。
(3).将袖带平整、松紧适宜地缠绕于右上臂,袖带下缘至少位于肘关节上2cm处,开启水银槽开关。
(4).将听诊器两耳器塞入外耳道,务必使耳器弯曲方向与外耳道一致。
(5).在肘窝内侧先用手触及肱动脉搏动所在位置,再将听诊器胸不留缝隙地轻轻贴在上面。
(6).测量收缩压:挤压橡皮球将空气打入袖带内,使血压表上水银柱逐渐上升到听诊器听不到脉搏音为止,再继续打气使水银柱再升2.7~4.0kPa(20~30mmHg)。随即慢慢松开气球螺丝帽,徐徐放气,在观察水银柱缓缓下降的同时仔细听诊,在听到“咚”的第一声清晰而短促脉搏音时,血压表上所示水银柱高度即代表收缩压。
(7).测量舒张压:继续缓慢放气,血管声音会有一系列的变化,先依次增强,后又逐渐减弱,最后完全消失。在声音变调或消失的一瞬间,水银柱的刻度即代表舒张压。
(8).血压记录常以收缩压/舒张压kPa表示,如收缩压、舒张压分别为14.70kPa(110mmHg)和9.33kPa(70mmHg),记为14.70/9.33 kPa(110/70mmHg)。
(9).列表记录你所测同学的血压。
【注意事项】
(1)室内必须保持安静,以利听诊。
(2)袖带应缚于肘关节以上至少2cm,探头置于肱动脉搏动处,切不可插入袖带下测量。袖带的缠绕不宜过松或过紧,以可插入一指头为易。
(3)动脉血压通常可测2次,但必须间隔3~5min。重复测定前,必须使袖带内的压力降到零位。一般取两次较为接近的数值为准。
(4)测压部位的位置应与心脏同高。
(5)如血压超出正常范围,应让受试者休息10min后再测。
(6)左右肱动脉可有0.7~1.3 kPa(5~10mmHg)的压力差,测量时固定在一侧上臂不得随意更换。
【实验结果】
记录你所测同学的血压。

【回答下列问题】
何谓收缩压和舒张压?试说明收缩压和舒张压测定的原理。
实验六 家兔手术实验基本操作
(含录像)
Experiment 6 Basic operation of experimental surgery in rabbits
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【实验目的】
学习哺乳类动物实验的技术方法,为了进一步提高实验的基本技能奠定基础。
【实验器材和药品】
哺乳类动物手术器械一套,兔手术台,25%氨基甲酸乙脂,生理盐水,大、小烧杯,20ml注射器注射器,气管插管,缝合丝线,兔固定器,婴儿磅秤等。
【实验步骤】
1.称量体重,按Kg体重计
2.麻醉并且固定动物.
①麻醉剂量:1g∕Kg。
②麻醉方法:沿兔耳缘经脉远端缓慢注射。
③固定动物:仰卧位固定于兔手术台上。
3.兔颈部手术:
①剪毛:用弯剪子剪颈部手术部位的毛
②从颈部正中切开皮肤,钝性分离颈部皮肤、皮下组织、肌肉。
③分离气管,气管下穿线后行气管插管术。
④分离颈部血管和神经。
⑤行左侧颈总动脉插管术。
【写出下列器械的用途】
1. 蚊式止血钳(mosquito forceps)
2. 直止血钳(hemostatic forceps)
3. 动脉夹(artery clip)
4. 气管插管(tracheal cannula)
5. 组织钳(tissue forceps)
【实验操作过程】
1、家兔的捉拿
一手抓住 皮肤,另一手 ,使家兔呈
姿势(Fig . 2),切忌提拿双耳。
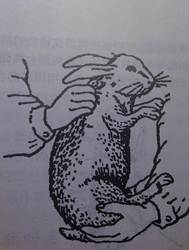
Fig . 2 Schematics for handing of rabbit
2、家兔体重的称量
称量家兔的体重所用的实验器材是 ,家兔的体重通常以
单位计量。
3、家兔的固定
按照实验要求,家兔常用兔盒固定(Fig . 3)或兔手术台固定。兔盒固定适用于 、 或观察耳部血管变化等,兔手术台固定适用于观察 、呼吸和进行 、胸、腹部手术。

Fig . 3 Schematics for Fixing of rabbit
4、家兔的麻醉
为了使动物在手术或实验中减少疼痛,保持安静,以利于实验顺利进行,在施行手术前必须对动物进行麻醉。麻醉家兔常用的麻醉药是
,俗称 ,英文 ,其常用浓度为: ,麻醉的理论参考给药剂量是 g/kg。
选用该药麻醉家兔,给药部位通常为 。将家兔固定在兔盒内,拔去耳外缘的毛,用手指弹动或轻柔兔耳,使静脉充盈。用左手的拇指和 捏住兔耳尖, 垫入兔耳注射处的下面,右手持注射器,从耳尖附近将针头刺入血管。如见到针头确在血管内,即以手指使针头和兔耳固定,将药液推入。如推注时有阻力,且兔耳局部变白,表明针头 。在推注该药的时候应注意速度不宜过快,更不能过量给药,判断家兔是否达到实验所要求的麻醉深度,可以通过 和
两个指标来判断。
5、本组所用家兔的体重为 kg,实验所用氨基甲酸乙酯的浓度为
,理论参考给药剂量为 ml/kg,在20ml注射器中所取的该药的体积为 ml。
6、在进行家兔颈部手术前必须剪毛,剪毛用 或 ,
不可用组织剪及眼科剪。剪毛范围应大于切口长度。为避免剪伤皮肤,,可一手 ,另一手 。剪下的毛应及时放入盛水的搪瓷碗中浸湿,以免到处飞扬。
7、在手术过程中,应注意避免损伤血管,如有出血要及时止血。组织渗血可用 压迫止血;较大血管出血,应用 夹住出血点及其周围少许组织,结扎止血。干纱布只用于吸血和压迫止血,不可用来揩擦组织,以免组织损伤和刚形成的血凝块脱落。
8、在分离神经和血管时,应掌握 、 的原则。
9、在哺乳动物急性实验中,为保证呼吸道通畅,一般均需做气管插管术。在进行家兔的气管插管术时,应于 下方 cm处作一
形切口,然后向下推入气管插管,用事先在气管后方穿好的棉线在切口稍下方做一结扎,再将结扎线固定于“T”形气管插管一侧分支处,以防插管脱落。
【回答下列问题】
如何辨别迷走神经、交感神经和减压神经?
实验七 呼吸运动的调节
Experiment 7 Regulation of respiration
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【目的和原理】
本实验的目的在于学习呼吸运动的记录方法。观察神经体液因素对呼吸运动的影响。
【实验器材和药品】
哺乳类动物手术器械一套,兔手术台,BL-410生物机能实验系统,张力传感器,刺激电极,球胆两个(分别装入CO2和N2)25%氨基甲酸乙酯,3%乳酸。
【实验步骤】
1. 麻醉并固定动物。
2. 沿颈部正中切开皮肤,分离气管并接入气管插管。
3. 分离双侧迷走神经并穿线备用。
4. 胸部手术:
上腹部剑突下正中切开皮肤,游离剑突(沿剑突轮廓剪开周围组织)剪断剑突上方的骨性组织,使剑突可呈900折叠即可。此为记录膈肌运动的方法。
5. BL-410系统的应用:
①进入本次实验项目。
②连接张力传感器于游离的剑突上,且使连线垂直绷紧(注意松紧度应使曲线位于通道的中间为宜)
③参数: G(增幅)—5~10mv T(滤波)— DC
F(频率)—30Hz
④刺激方式与强度: 连续单 50v以内
【观察项目】
1. 描记正常呼吸曲线,认清曲线与呼吸运动的关系。
2. 增加吸入气中CO2的浓度。将装有CO2的球胆管口对准气管插管侧管(二者有一定距离)并将球胆的夹子逐渐松开,使CO2气流不宜过急地随吸气进入气管。此时观察高浓度CO2对呼吸运动的影响。夹闭CO2球胆管,观察呼吸恢复的过程。
3. 缺氧:吸入纯氮气。
4. 增大无效腔。把50cm长的橡皮管连接在侧管上,家兔通过这根长管进行呼吸,观察经一段时间后呼吸运动有何变化,呼吸发生明显变化后即去掉橡皮管,使其恢复正常。
5. 血中酸性物质增多时的效应。用5ml注射器,由耳缘静脉较快地注入3%的乳酸2ml,观察此时呼吸运动的变化过程。
6. 迷走神经在呼吸运动中的作用。描记一段对照呼吸曲线,先切断一侧迷走神经,观察呼吸运动有何变化,再切断另一侧迷走神经,观察呼吸运动有何变化。然后以不同袭击强度刺激一侧迷走神经的向中端,再观察呼吸运动的变化。
【实验操作过程】
1、本组所取家兔的体重为: kg。
2、化学因素对呼吸运动的调节也是一种反射性调节,这里的化学因素是指动脉血、组织液或脑脊液中的 、 和 。
3、参与呼吸运动调节的化学感受器因其所在部位的不同,分为
和 。
4、 是调节呼吸运动的最重要的生理性化学因素。
5、在一定范围内,吸入气中CO2分压增加时,会引起呼吸 。
6、血液CO2升高对呼吸的刺激主要通过刺激 化学感受器。
7、呼吸基本节律产生于 。
8、切断家兔颈部双侧迷走神经后,呼吸将 。
【实验结果及分析】
1、实验结果:
将观察到的实验现象填入下表中:
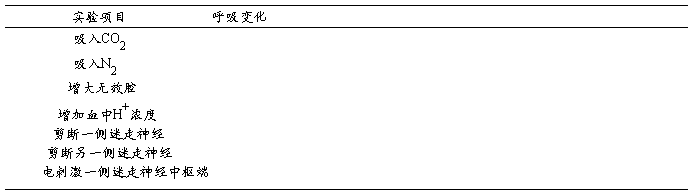
2、分析讨论实验结果:
【回答下列问题】
迷走神经在节律性呼吸运动中起何作用?
实验八 胃肠运动的观察
Experiment 8 Observation of gastrointestinal motility
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【目的和原理】
观察正常情况下,在体胃和小肠的运动形式,并分析神经、体液因素对其活动的影响
【实验对象】
家兔
【实验器材和药品】
哺乳动物手术器械一套、兔手术台、兔盒、刺激电极、20ml、1ml注射器各一个、25%氨基甲酸乙酯、乙酰胆碱(1:100000)、肾上腺素(1:100000)、阿托品注射液
【实验步骤和观察项目】
一、手术操作
(一)麻醉、固定 将家兔以25%氨基甲酸乙酯(4ml/kg)静脉注射,背位固定于兔手术台上。
(二)气管插管 颈部正中切口,气管插管。
(三)暴露胃肠 腹部正中切开腹壁(注意不要损伤腹腔内器官和血管),暴露胃和肠。
(四)分离神经 在膈下食管前方找出迷走神经前支,分离了并穿线备用。用温生理盐水湿润的纱布将肠管推向右侧,在左侧肾上腺上方找出内脏大神经,分离并穿线备用。
二、观察项目
(一)观察正常情况下,胃和小肠的运动,包括胃、小肠的紧张性、蠕动频率和小肠的分节运动频率。
(二)将迷走神经套上保护电极,用适宜的频率和强度的连续方波刺激膈下迷走神经,观察胃、小肠运动的变化。若反应不很明显,可增大刺激强度并反复刺激直至反应明显。
(三)将保护电极套在内脏大神经上,用适宜的频率、强度电刺激内脏大神经、观察胃、肠运动的变化。
(四)直接在胃和小肠表面上滴上数滴1:100000乙酰胆碱,观察胃肠运动的变化。待出现反应后,及时用新鲜的生理盐水冲洗干净。
(五)直接在胃和小肠表面上滴上数滴1:100000肾上腺素,观察胃肠运动的变化。出现反应后立即用新鲜的生理盐水冲洗干净。
(六)在电刺激膈下迷走神经出现明显胃肠运动变化的基础上,从兔耳缘静脉注射阿托品0.5~1.0mg(一般注射0.5mg),观察胃擦胃肠运动的变化。
(七)用刺激电极直接置于胃和小肠的表面,以中等频率和强度刺激之,观察其运动的变化。
【实验操作过程】
1、本组所取家兔的体重为: kg。
2、消化道主要由多层平滑肌组成,可以产生多种形式的运动,在消化道的不同部位运动形式有所差别,但运动的基本形式是 。
3、沿腹部正中线,自剑突向后打开腹腔,暴露胃肠,以备观察。在膈下食管的末端找出 ,分离穿线备用。用温生理盐水湿润的纱布将肠管推向右侧,在左侧腹后壁肾上腺的上方找出并分离 ,
穿线备用。
4、小肠的运动形式有 、 和 。
【实验结果及分析】
1、将观察到的胃和小肠的运动变化填入下表:
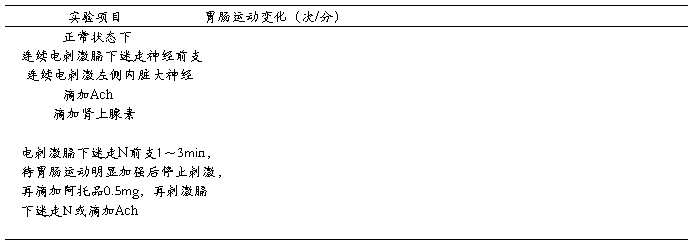
2、结果分析讨论:
实验九 动脉血压的调节
Experiment 9 Regulation of Arterial blood pressure
同组人姓名(the name of the students in the same group)
。
日期(date): 年 月 日
【实验目的】
学习哺乳动物动脉血压的直接测量方法,观察神经和体液因素对血压的调节作用。
【实验原理】
心脏受交感神经和副交感神经支配。心交感神经兴奋,其末梢释放去甲肾上腺素,作用于心肌细胞的β1受体,使心跳加强加快,传导加速,从而使心输出量增加,动脉血压升高。支配心脏的副交感神经为迷走神经,兴奋时其末梢释放乙酰胆碱,作用于心肌细胞的M受体,使心率减慢,心脏收缩力减弱,传导速度减慢,从而使心输出量减少,动脉血压下降。
支配血管的自主神经绝大多数属于交感缩血管神经,兴奋时其末梢释放去甲肾上腺素,作用于血管平滑肌的α受体,使血管收缩,外周阻力增加,动脉血压升高。同时由于容量血管收缩,促使静脉回流,心输出量亦增加。
心血管活动除受神经调节外,还受体液因素的调节,其中最重要的为肾上腺素和去甲肾上腺素。肾上腺素对α受体与β受体均有激活作用,使心跳加快,收缩力加强,传导加快,心输出量增加。它对血管的作用取决于两种受体中哪一种占优势。去甲肾上腺素主要激活α受体,对β受体作用很小,因而使外周阻力增加,动脉血压增加。其对心脏的作用远较肾上腺素为弱。静脉内注入去甲肾上腺素时,血压升高,启动减压反射,可反射性地引起心跳减慢。
【实验对象】
家兔
【实验器材和药品】
BL-410生物机能实验系统、哺乳类动物手术器械、婴儿秤、兔手术台、压力传感器、保护电极、刺激电极、铁架台、双凹夹、气管插管、动脉夹、三通、动脉插管、注射器(1ml、5ml、20ml)、丝线、纱布、25%氨基甲酸乙酯、1000U/ml肝素、生理盐水、1:10000肾上腺素溶液、1:10000去甲肾上腺素溶液、1:10000乙酰胆碱。
【实验步骤】
1.动物麻醉固定 称重后,耳缘静脉缓慢注入25%氨基甲酸乙酯(4ml/kg)
2.气管插管
3.分离颈部神经和血管
4.导入动脉插管
5.记录血压 启动BL-410生物机能实验系统进入测量状态。小心打开动脉夹,即可见血液冲入动脉插管。检查检压系统,确保无漏水及气泡存在。记录动脉血压曲线。
6.观察项目
(1)观察正常血压曲线。
(2)牵拉一侧颈总动脉,观察血压的变化。
(3)用动脉夹夹闭右侧颈总动脉15s,观察血压的变化。
(4)结扎并剪断右侧迷走神经,电刺激其外周端,观察血压的变化。
(5)由耳缘静脉注入1:10000去甲肾上腺素0.3ml,观察血压的变化。
(6)由耳缘静脉注入1:10000乙酰胆碱0.2ml,观察血压的变化。
(7)由耳缘静脉注入1:10000肾上腺素0.3ml,观察血压的变化。
【实验操作过程】
1、本组所取家兔的体重为: kg。
2、心脏受 神经和 神经支配。
3、本实验中用到的能够通过其直接测定血压的BL-410生物机能实验系统器件是 。实验前,应预先将其加压至 mmHg。
4、本实验中,手术操作的关键步骤就是进行动脉插管。在插管前应在动脉球中加入 ,以防止血液凝结;在左侧颈总动脉 端结扎,在结扎线下方 cm处用 夹住动脉的 端。用眼科剪在尽可能靠远心端结扎处剪一斜口,然后将动脉插管向 方向插入血管,用已穿好的另一丝线在插入血管的插管尖的细颈部分将血管扎紧,以防插管滑落。
5、实验中所用去甲肾上腺素的浓度为 、肾上腺素的浓度为
、乙酰胆碱的浓度为 。
6、实验中参数设置:G: ,T: ,F: ;刺激方式:
;刺激强度: 。
【实验结果及分析】
1、将实验结果填入下表:
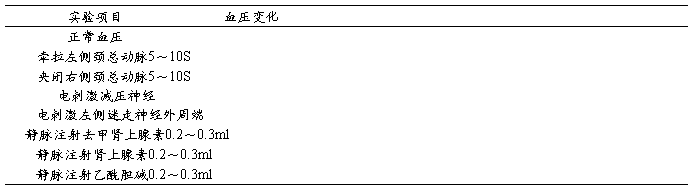
2、结果分析讨论:
【回答下列问题】
1、肾上腺素和去甲肾上腺素的作用有何不同?为什么?
2、动脉血压是如何形成的?
