附件1:
20##年度内部审计工作实施计划
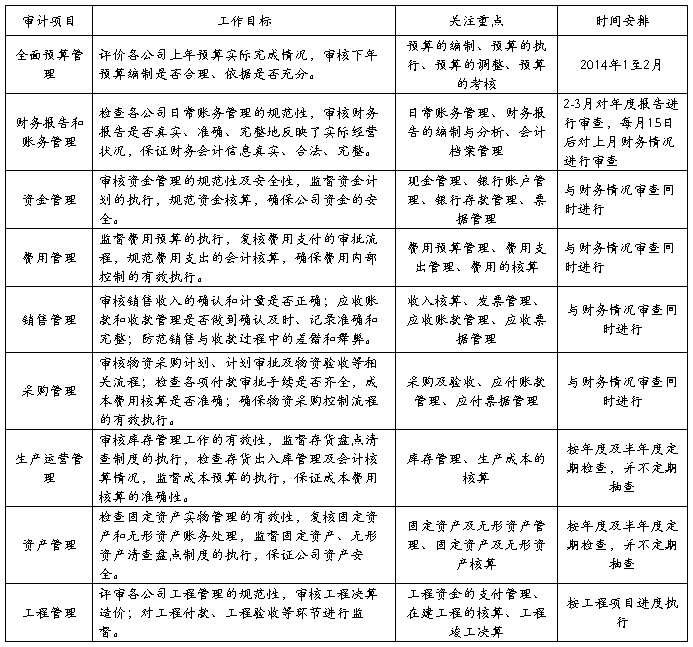
为了进一步发挥审计的监督与服务职能,促进集团各子公司提升管理效益,结合集团经营计划,特制定20##年度内部审计工作实施计划。
第二篇:20xx年度自检实施计划1
20##自检计计划
目 的:制订公司GMP自检计划,明确自检组织形式、自检对象和频率、检查对象、检查内容。
范 围:适用于本公司内部GMP自检工作。
责 任:GMP办公室、质量管理负责人、生产管理负责人及个部门负责人对实施本规定负责。
内 容:
1.自检概述:GMP自检是指制药企业内部对药品生产实施GMP的检查,是企业执行GMP中一项重要的质量活动。实质上也是对企业完善生产质量管理体系的自我检查,通过GMP自检,发现企业执行GMP时存在缺陷项目,并通过实施纠正和预防措施来进一步提高GMP执行的持续性、符合性、有效性或通过自检进行持续改进。
GMP自检作为《药品生产质量管理规范》中规定的条款之一。是企业内部管理的一种重要的管理手段,自检的目的是检查和评价企业在生产和质量管理的方面是否符合《药品生产质量管理规范》的要求。
通过内部自检建立起自我改进的管理机制,是促使各个职能部门能更有效执行GMP的重要手段。保证制药企业的生产质量管理体系能够持续地保持有效性,并不断改进和完善。
2.自检目的
2.1是公司的质量管理现状符合国家有关规范的要求;
2.2作为一种重要的管理手段和自我改进的机制,及时发现管理中存在的问题,预防和纠正企业管理缺陷:
2.3为管理层的决策提供事实依据;
2.4为获取公正的管理信息;
2.5指出公司的风险性;
2.6指出需要进行质量改进的可行性。
3.自检的依据
3.1国家有关法律、法规,如《药品管理法》、《药品生产质量管理规范》(20##年版)等;
3.2国家药品标准,如《中国药典》(2010版)等;
3.3公司内部有关生产质量管理要求,如公司GMP文件等。
4.自检的方式
4.1常规检查:指按照GMP规定条款进行的全面检查。
4.2追踪检查(再评估或再检查):被检查部门未履行或不正确履行GMP的某些规定,并已接受过公司GMP自检小组下发的“药品GMP自检整改通知单”,自检小组应对其进行追踪检查,监督整改措施落实情况。
4.3特殊检查:在接到投诉或回收怀疑其有质量问题的产品后,或者在接到药品监督部门通知检查时,应进行特殊检查。
五、自检的时机和频率
一般情况下每月进行一次内部自检并确保每半年完成全部内容,但在下列情况下,按GMP要求进行全面自检:
? 生产方法和操作有明显改变时
? 更换关键人员、厂房、设备时
5.自检范围
自检的范围一般取决于公司管理体系所涉及的部门、区域、内容、活动、产品及服务;自检的范围原则上应包括公司所涉及执行GMP的所有部门、区域、产品。本次自检范围包括:
? 机构与人员
? 厂房、设施与设备
? 物料与产品
? 确认与验证
? 文件管理
? 生产管理
? 质量管理、质量控制及保证
? 委托生产与检验
? 产品发运与召回
6.自检组织及其职责
自检工作是公司执行GMP规范的一项重要工作,需要公司内部各部门人员的参与和配合,公司管理层重视,自检管理部门协调组织得力,自检人员认真负责,才能保证自检工作的顺利开展。
7.组织机构:
由GMP办公室任组长、质量负责人任副组长,各部门负责任组员的GMP自检小组,组织实施各项自检工作。
8.自检的实施:自检按下列程序进行:
? 召开一次简短的首次会议(对本次自检作出必要的说明);
? 进行现场检查(客观描述检查中发现的缺陷项目,并让受检查部门负责人签字确认);
? 确定不合格项并编写不合格报告;
? 汇总分析自检结果;
? 召开末次会议,宣布自检结果;
? 编写自检报告;
? 纠正措施的跟踪确认。
9.20##年自检计划

