重庆XX中药制药有限责任公司
 检验记录(首页)
检验记录(首页)

【性状】
呈球形或扁球形。表面棕红色至暗中色,干瘪,缩皱,果肉常紧贴于种子上。果肉气微,味微酸。
结论:□符合规定 □不符合规定
重庆XX中药制药有限责任公司
 检验记录(附页)
检验记录(附页)
 检品批号:1501001
检品批号:1501001
【鉴 别】 照《中国药典》20##年版□一部附录Ⅵ B□二部附录Ⅴ B薄层色谱法检验。
供试品溶液的制备:
取粉末1g,加环己烷10ml,超声处理30分钟,滤过,滤液蒸干,残渣加甲醇2ml使溶解,离心,取上清液蒸干,残渣加环己烷1ml使溶解,作为供试品溶液。
□标准品□对照品□对照药材溶液的制备:
取南五味子对照药材1g,同法制成对照药材溶液。
取安五脂素对照品,加环己烷制成每1ml含2mg的溶液,作为对照品溶液。
结果:供试品色谱中,在与□标准品□对照品□对照药材色谱相应的位置上,显 颜色的□荧光斑点□斑点。
结论:□符合规定 □不符合规定
 重庆XX中药制药有限责任公司
重庆XX中药制药有限责任公司
薄层色谱检验记录

检品编号:15010011
检品名称:南五味子
日期:2015.01.17
室温:15℃
相对湿度:66%
薄层板:硅胶G板
展开剂:
三氯甲烷-丙酮(60:1)
显色剂:
①磷钼酸
②
备注:
样品 点样量(微升)
1 供试品 2ul
2 对照药材 2ul
3 对照品 2ul
4
重庆XX中药制药有限责任公司
 检验记录
检验记录
 检品编号:1501001
检品编号:1501001
【杂质】 中国药典20##年版一部附录IX A,依法检查。
天平型号:YP-B1003 编号: ZGB0005
1# 2#
样 品 重W1 (g):
挑选出的杂质重量W2 (g):

计算公式:
⑴
⑵
平均值:
标准规定:不得过1.0%
结论:□符合规定 □不符合规定
 重庆XX中药制药有限责任公司
重庆XX中药制药有限责任公司
检验记录(附页)
 检品编号:1501001
检品编号:1501001
【水分】 中国药典20##年版一部附录IX H第一法,依法检查。
天平型号:FZ604A 编号:ZGB01-017
干燥箱型号:101-1A 编号:ZGB01-008 干燥温度:105℃
1号 2号
称量瓶恒重W1 (g)
一 次(g):
二 次(g):
样 品 重W2 (g):
样加瓶重W3五小时(g)
再一小时(g):

计算公式:
⑴
⑵
平均值:
标准规定:不得过12.0%
结论:□符合规定 □不符合规定
重庆XX中药制药有限责任公司
 检验记录(附页)
检验记录(附页)
 检品批号:1501001
检品批号:1501001
灰分 照《中国药典》20##年版一部附录Ⅸ K□总灰分□酸不溶性灰分测定法检查
天平型号:FZ604A 编号:ZGB01-017
仪器型号:SX2-2.5-10A 编号:ZGB01-009
温度:550℃
实验结果:
坩埚瓶恒重W1 : 1# 2#
一 次(g)
二 次(g)
样 品 重W2: (g)
样品+坩埚恒重W3:
一 次(g)
二 次(g)
计算公式:灰分% = 
①
②
平均值:
标准规定:不得过6.0%
结论:□符合规定 □不符合规定
 重庆XX中药制药有限责任公司 检验记录(附页)
重庆XX中药制药有限责任公司 检验记录(附页)
 检品批号:1501001
检品批号:1501001
【含量测定】 《中国药典》20##年版□一部ⅥD□二部附录ⅤD高效液相色谱法
色谱条件与系统适用性试验:
仪器型号:LC210 编号:ZGB01-010
天平型号:FZ604A 编号:ZGB01-017
柱温:35℃ 检测器:□紫外
检测波长:254 nm 流动相:四氢呋喃-水(38:62) 流速:3 ml/min
供试品溶液的配制:
取粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,称定重量,超声处理(功率250W,频率40kHz)30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
□对照品□标准品溶液的配制:
取五味子脂甲对照品适量,精密称定,加甲醇制成每1ml含40ug的溶液,即得。
精密量取供试品溶液 10 μl与对照品溶液 10 μl,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算,
重庆XX中药制药有限责任公司
 检验记录(附页)
检验记录(附页)
 检品批号:1501001
检品批号:1501001
计算:
f值计算公式: F=C/A

样品计算公式:

示例:
标准规定:不得少于0.20%
结论:□符合规定 □不符合规定
第二篇:北五味子与南五味子的色谱鉴别
北五味子与南五味子的色谱鉴别
Schisandra chinensis and South Schisandra Chromatographic
identification
北五味子与南五味子的色谱鉴别
摘要
目的:通过色谱分析的方法,探讨北五味子与南五味子的差别。方法:利用薄层色谱 (TLC)、高效液相色谱(HPLC)及气象色谱-质谱法(GC-MS)定性等手段,对两药进行鉴别。结果:经TLC、HPLC及GC-MS色谱分析表明,北五味子含有五味子乙素,南五味子则不含这种物质;并且北五味子与南五味子种子中挥发油的种类、成分相差很大。结论:南五味子所含成分及药性,与北五味子存在显著差异,认为不可替代北五味子药用。两种药材应分开入药。
关键词:北五味子,南五味子,高效液相色普,薄层色谱,气象色谱-质谱
Schisandra chinensis and South Schisandra Chromatographic identification
Abstract
Objective: Searching for the difference Schisandra chinensis and South Schisandra by Chromatographic analysis. Methods: To identify the two drugs by TLC ,HPLC and GC-MS chromatographic approach. Results: To show that Schisandra chinensis contains Schisandrin, South schisandra without the substance by TLC ,HPLC and GC-MS chromatographic analysis. Conclusion: South Schisandra contains ingredients and there was a significant difference in Schisandra, South Schisandra medicinal that can not replaceSchisandra chinensis. Two kinds of medicinal herbs should be separated.
Key words: Schisandra, Kadsurasinensis,HPLC,TLC,GC-MS
前言
五味子为常用中药,始载于《神农本草经》,列为上品[1]。其性温,味酸、甘,归肺、心、肾经,具有收敛,固涩,益气生津,补肾宁心功能。用于久咳虚喘,遗精遗尿,久泄,盗汗等滑脱、开泄或津伤之虚证[2]。《中国药典》20xx年版一部收载的五味子品种为木兰科植物五味子[Schisandra chinensis( Tnrcz.) Bill.]的干燥成熟果实( 晒干或蒸后晒干),商品习称“北五味子”。由于历史与地方用药习惯等因素,全国有10余种混淆品作五味子药用。而目前市场出现较多的则是同科植物华中五味子( S.sphenanthera Rehd.et Wils.)的干燥成熟果实。商品习称“南五味子”,其中挥发油具有镇咳作用[3.4]。五味子甲素和乙素是北五味子的主要有效成分[5]。目前, 一些中成药中五味子甲素和乙素的含量测定方法有较多报道[6-9],但南五味子中不含五味子甲素。五味子种子中挥发性成分约占种子的1.6 %[10],北五味子与南五味子种子中挥发油的种类、成分相差很大。北五味子作为五味子正品,主产于东北及华北各省,畅销全国并出口。南五味子主产于河南、陕西、甘肃、湖北、四川、云南等中南部各省,畅销全国。鉴于该两者在药材品性上差异较大,南五味子虽也被收入某些地方药材标准使用,但在临床疗效上却远不及北五味子。认为不可替代北五味子药用。为此,本文试从药材的薄层色谱(TLC)、高效液相色谱(HPLC)及气象色谱-质谱(GC-MS)特征等方面对两者做了比较试验,用于区分两种药材效果明显,为以后更好的利用和研究南、北五味子做参考。
1 材料与方法
1.1 实验材料
仪器: Agilent HP1100高效液相色谱仪BX41型Olympus生物显微镜、GC-MS联用仪。
试药: 供试品五味子(北五味子)、华中五味子(南五味子)、对照药材五味子(为北五味子)、 对照品五味子甲素、五味子乙素。
化学试剂:均为分析纯。水为纯净水、薄层板为硅胶GF254板。
1.2 方法
TLC 鉴别,HPLC 鉴别,GC-MS分析
2 结果
2.1 TLC鉴别
取上述两种供试品粉末各0,5 g,分别加三氯甲烷20mL,加热回流30min,过滤,滤液蒸干,残渣加三氯甲烷1 mL使之溶解,作为供试品溶液S1、S2; 另取五味子对照药材粉末1 g,同法制成对照药材溶液R1; 再取五味子甲素、五味子乙素[11-13]对照品各适量,分别加三氯甲烷制成每1 mL含1 mg的溶液,作为对照品溶液R2、R3。按照《中国药典》20xx年版一部TLC法(附录VI B) 实验,吸取上述5种溶液各10μL,分别点于同一硅胶GF254 薄层板上,以石油醚( 30 -60℃)-甲酸乙酯-甲酸( 15∶5∶1) 的上层溶液为展开剂,展开,取出,晾干,置紫外光灯( 254 nm) 下检视。结果北五味子色谱中,在与对照药材[14]及对
照品色谱相应位置上显现相同颜色的斑点; 而南五味子色谱中,在与对照药材及对照品色谱相应位置上显然缺少五味子乙素这个主斑点及其他副斑点。所缺少的斑点大多位于该色谱的中上部,即显示南五味子缺乏油性物质,这恰与其干瘪的药材性状相符合。
图1 北五味子与南五味子TLC 图谱
S1.北五味子S2.南五味子R1.五味子对照药材R2.五味子甲素R3.五味子乙素
2.2 HPLC鉴别
2.2.1 色谱条件
色谱柱Hypersil ODS 柱( 4.6 mm×250 mm×5 m) ,流动相甲醇-水(72∶28 );流速1.0 mL/min; 检测波长254 nm,理论板数按五味子乙素峰计算不小于6000( 五味子乙素保留时间22.2 min) 。
2.2.2供试品溶液与对照品溶液制备
取北五味子与南五味子粉末各1.0 g,分别加75%甲醇50 mL,浸泡2 h,超声处理30 min,离心,分取上清液,用微孔滤膜( 0.45 μm) 滤过,取续滤液作为供试品溶液备用。另取五味子乙素对照品适量,加甲醇制成每1 mL 含0.1 mg 的溶液,作为对照品溶液。
2.2.3 测定与结果
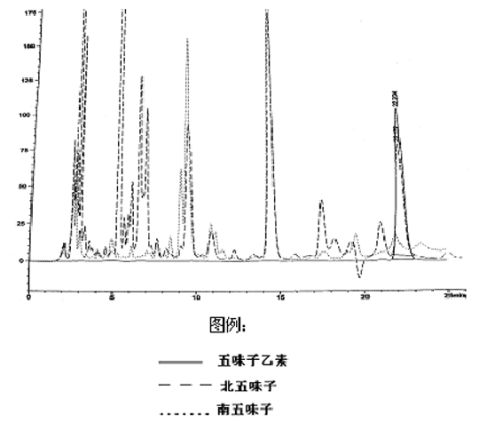
北五味子HPLC 色谱中,出现与对照品峰保留时间相同的一个目标峰( 五味子乙素) ,而南五味子HPLC 色谱中则无此目标峰出现。
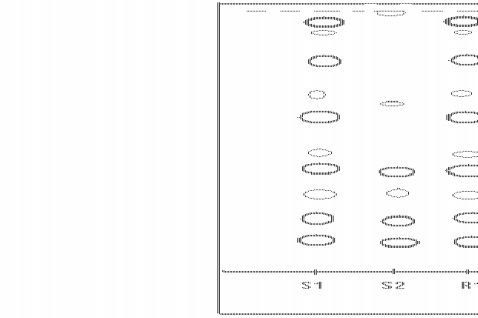
图2 北五味子与南五味子HPLC重叠图谱
2.3 南五味子与北五味子的GC-MS分析
2.3.1北五味子
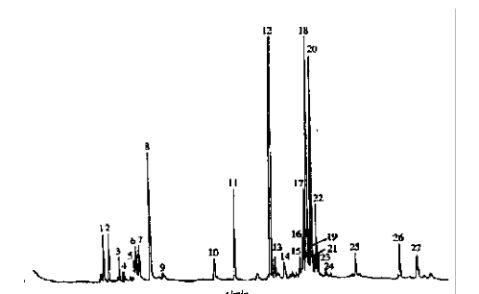
图3 北五味子种子挥发油GC-MS总离子流图

30min内分离出44个峰,鉴定了其中27个组分,占挥发油总量的95.13%。北五味子种子挥发油[15.16]的主要成分为烯, α-金合欢烯、α-荜澄茄油烯等。
2.3.2南五味子
表4 南五味子种子中挥发油化学成分及相对含量

南五味子出30个峰, 经质谱分析, 对每个色谱峰的化合物给出特定的MS峰,经计算机库贮存信息检索, 初步鉴定出22种化合物,占挥发油总量的68.05%。其中, 质量分数较高的有α-檀香烯(10.65%) 、榄香烯(6.48%) 、β-雪松烯(11.49%)、γ-杜松萜烯(10.87%)2-(4a,8-二甲基-1,2,3,4,4a,5,6,7-八氢萘-2) -1-丙烯醇(5.42% )和2种未检出的化合物峰22( 16. 79%) 、峰27( 10. 07%) 。从检出的化合物结构可以看出, 南五味子种子挥发油成分主要为倍半萜类( 包括萜烃及含氧衍生物-醇、醚、酮等) 化合物。
3 小结与讨论
GC-MS分析表明北五味子与南五味子种子中挥发油的种类与含量有很大差异,两者并不一样,也不能被相互代替。TLC及HPLC色谱分析表明富含五味子甲素、五味子乙素等油性物质,这与五味子功能中除收敛固涩外,还具有益气生津,补肾宁心的滋养濡润作用相吻合。而南五味子粒小干瘪,皮肉干枯而欠油性,色谱分析证明其不含五味子乙素等一些亲脂性成分,显微鉴别也印证果皮中少有油细胞。然而干瘪少油的南五味子,皮薄则显籽多。种子气香、味辛辣而微苦,从药性理论讲,辛香性走窜散发,恰与五味子的收敛补润功能相背离。因此,认为南五味子不可替代北五味子药用。两种药材应分开入药。区分两种五味子的鉴别要点在于: 北五味子果大肉厚色红润,而南五味子粒小干瘪籽无光(泽)。但需要指出的是,对于未成熟抢青采收的北五味子,干燥后也显干枯少油状,此时只需剥开看其种子有否光泽即可判断。必要时配合采取显微或色谱方法以及增加含量测定项目以鉴定其真伪优劣。鉴于地区习用和资源利用关系,南五味子虽不能等同北五味子入药,但仍具有一定药用价值。可根据其气味特性另辟药用。对其药理药效尚待深入探究。
参考文献
[1] 李时珍(明)本草纲目.北京:人民卫生出版社,1975:1238-1241。
[2] 国家药典委员会编1中华人民共和国药典(一部)北京:化学工业出版社,2005:44,169。
[3] Xiao P G. Modern Chinese Materia Medica ( 新编中药志)[M] . Beijing : Chemical
Industry Press , 2002.
[4] Zheng H Z. Modern Study and Application of Chinese Materia Medica (中药现代研究与应用) [M ] . Beijing: Xueyuan Press ,1999.
[5] 孙玉雯,刘汉清.五味子及其制剂中主要化学成分的提取和测定方法研究进展[J]。时珍国医国药,2004,15(6):368-369。
[6] 刘霞,杨远明,蔡敏芝,等。HPLC测定肝平胶囊中五味子甲素含量[J]。中成药,2004, 26(7):601- 602。
[7] 杜英峰,袁志芳 张兰桐,等.RP-H PLC法测定五味子及维肝福泰片中五味子甲素和五味子乙素的含量[J]。中草药,2004,35(5):519- 521
[8] 杜英峰,袁志芳,王春英,等。高效液相色谱法同时测定护肝片中五味子甲素和五味子乙素的含量[J] 。药物分析杂志,2004,24(4):397-399。
[9] 刘刚,王驰,薛克昌,等HPLC法测定五味子酊中五味子甲素和五味子乙素含量[J]。解放军药学学
报,2004,20(2):112-114。
[10] 朱有昌主编。东北药用植物。哈尔滨:黑龙江科技出版社,1989:4291。
[11] 阴健,肖培根,郭力弓,等。《中药现代研究与临床应用》.北京:学苑出版社,1995149。
[12] 王宝琴。《中成药质量标准与标准物质研究》。 北京:医学科技出版社,1994∶168。
[13] 中华人民共和国药典委员会。《中国药典》,1部。广东科技出版社,化学工业出版社, 1995∶502。
[14] 康廷国。中成药薄层色谱鉴别。北京:人民卫生出版社,1995∶197。
[15] Wan g Y, Wang J F, Cui Y H, et al . Analysis of the essential oil from the seeds of Schisandra chinensis by GC-MS [J] .Chin P harm J (中国药学杂志) , 2001, 36( 2) : 91.
[16] Li X N, Cui H, Song Y Q, et al. Analysis of the essential oil of S chisandra chinensis
(Turcz.) Baill . with GC/ MS [ J] .Acta Pharm Sin (药学学报) , 2001, 36( 3) : 215-219.
