二元合金平衡相图测定实验指导书
一、实验目的
熟悉用热分析法测定金属与合金的临界点,并根据临界点画出二元合金相图。
二、实验原理
相图是一种表示合金状态随温度、成分而变化的图形,又称状态图或平衡图。根据相图可以确定合金的浇注温度,进行热处理的可能性,形成各种组织的条件等。
到目前为止,几乎所有的相图都是通过实验测定出来的。金属及合金的状态发生变化将引起其性质发生变化,例如液体金属结晶或固态相变时将会产生热效应,合金相变时其电阻、体积、磁性等物理性质亦会发生变化。金属及合金发生相变时(包括液体结晶和固态相变)引起其某种性质变化所对应的温度称为临界温度,又称临界点。因此可以通过测定金属及合金的性质来求出其临界点。把这些临界点标注在以温度为纵坐标、成分为横坐标的图上,然后把各个相同意义的临界点连接成线,就构成了完整的相图。可见,相图的建立过程就是金属与合金临界点的测定过程。
测定金属与合金临界点的方法很多,如热分析法、热膨胀法、电阻测定法、显微分析法、磁性测定法、 X 射线分析法等,但其中最常用、最基本的方法是热分析法。
热分析法是通过测量、记录金属或合金在缓慢加热或冷却过程中温度随时间的变化来确定其临界点。测定时将金属自高温缓慢地冷却,在冷却过程中每隔相等时间测量、记录一次温度,由此得到温度与时间的关系曲线,称为冷却曲线。
金属或合金在缓冷过程中,当没有发生相变时,温度随时间增加而均匀地降低;一旦发生了某种转变,则由于有热效应产生,冷却曲线上就会出现转折,该转折点所对应的温度就是所求的临界点。因此,测出冷却曲线就可很容易地确定相变临界点。图 3-1 就是根据测定的一组冷却曲线建立相图的实例。

图1 Pb-Sb 二元相图的测定
热分析法简便易行,对于测定由液态转变为固态时的临界点,效果较为明显。但对固态溶解度变化因相变潜热小,难用热分析法测定,需用其它方法。
三、实验设备与温度测量
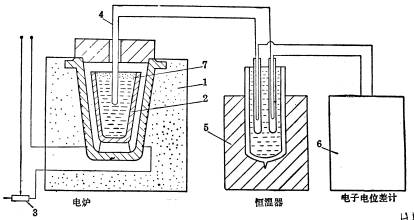 热分析用实验设备和装置如图 3-2 所示。由图可见,测温装置主要是由热电偶和电位差计组成。
热分析用实验设备和装置如图 3-2 所示。由图可见,测温装置主要是由热电偶和电位差计组成。
图2 热分析实验装置简图
1- 坩埚电炉 ( 3 ~ 5kw ); 2- 陶瓷坩锅( 30 或 50ml ); 3- 变阻器; 4- 热电偶; 5- 恒温器;
6- 电位差计(或长图自动平衡记录仪); 7- 覆盖剂(木炭粉或石墨粉)
热电偶是由两种不同金属丝所组成,这两种金属丝一端被焊接在一起形成热接点,而未焊接的一端是冷接点(又称自由端),用导线连接在电位差计上。若将热接点加热,则电路中就会产生热电势,它的数值可由电位差计测定。热接点的温度愈高,热电势就愈大,电位差计指针所指的数值也就愈大。
在两端相联的热电偶中所产生的热电势,可由下式决定:
 ( 3-1 )
( 3-1 )
式中, E ( t 1 ) 为热接点的热电势,其数值由热接点的温度 t 1 而定。 E ( t 0 ) 为冷接点的热电势,其数值由冷接点的温度 t 0 而定。
当 t 0 为常数,例如 0 ℃时, E ( t 1 , t 0 )= E ( t 1 ) 。这时,热电势可直接由热接点的温度(即加热温度)来决定。当冷接点不是 0 ℃(即 t' 0 )。而增加为 t 0 时,由( 3-1 )式可知,因冷接点温度的改变,热电偶所产生的热电势也发生改变。因而,必须对冷接点的温度进行修正。修正可按下式进行,即:
 ( 3-2 )
( 3-2 )
( 3-2 )式的实际应用如图 3-3 所示。
例如,设 t' 0 =60 ℃, t 0 =0 ℃,已测知 t 1 温度时热电偶中所产生的热电势 E ( t 1,60 ° ) =31mV, 求 E ( t 1,0 ° ) 。此时,若应用图 3-3 所示的热电偶特性曲线,必须先求出冷接点温度 t 0 =0 ℃时的热电势数值。
E ( t 1,0 ° ) = E ( t 1,60 ° ) + E (60 ° ,0 ° ) , 由图 3-3 可查出 E (60 ° ,0 ° ) =4.03mV 。
∴ E ( t 1,0 ° ) =31+4.03=35.03mV
根据图 3-3 中所示曲线, 36.03mV 的热电势相当于热接点的温度为 441 ℃。
热电偶有很多类型。
此外,热电偶接长图自动平衡记录仪也是目前常用的测温装置,但需配合使用数据放大器或调整仪器内部上限及下限锰铜丝制电阻值。使用该仪器可在记录纸上自动画出冷却曲线。
除热电偶电位差计测温装置外,也可利用水银温度计直接测温;但水银温度计本身受温度影响较大,测温不准确,且易于因预热不当、骤冷骤热而破裂,造成事故。水银温度计最高使用温度为 550 ℃,因此,对较高熔点金属加纯锑等不能使用。
随着科学技术的发展,目前已开始用微处理机来测定冷却曲线,更为简便、可靠。
本实验用合金选Pb-Sn 二元合金系。合金系成分参考下表 。

四、实验步骤
1 .预先配好所选合金系中的七种金属与合金,分别放在陶瓷坩埚中。试验时,各组将合金放在坩埚电炉中加热,待合金熔化后,将热电偶连同保护瓷套管插入金属液中,热电偶的工作端应处于金属液中部,不要靠近坩埚壁、坩埚底或金属液面。热电偶的自由端可以直接接到电位差计上,但此时应考虑自由端温度补偿,接线时要注意电极的正负。
2 .加热升温至金属与合金熔点以上 100 ℃左右,然后关闭电源。为防止金属氧化,应在熔化的金属液面上覆盖一层木炭粉或石墨粉。
3 .当合金开始冷却时,若用人工测温,则需每隔 1min 记录一次电位差计的读数,在临界点附近,可以每隔半分钟作一次记录。
4 .根据所得数据,作出冷却曲线(以热电势—时间或温度—时间为坐标),根据冷却曲线找出临界点。若测得的数值为毫伏数,则应换算成所对应的温度。换算时应考虑自由端的温度及热电偶的误差(各热电偶均有校正表)。根据各组所测得的临界点,建立铅—锡二元合金相图。
五、实验报告要求
1 .每组将本所选定的合金在冷却过程中热电势随时间的变化数据记录于表中。
2 .根据上表记录的数据,用方格纸绘出所测合金的冷却曲
线,并注明合金成分,标注出临界点。
3 .根据各种成分合金的临界点,按比例作出 Pb-Sn 合金相图。
4 .对实验结果进行分析和总结。
第二篇:二元气液平衡数据测定_实验指导书
化工专业实验报告
实验名称:二元气液平衡数据的测定
实验人员:
同组人:
实验地点:
实验时间:
班级:
学号:
指导教师:
实验成绩:
二元气液平衡数据的测定
一、 实验目的
1. 测定苯—正庚烷二元体系在常压下的气液平衡数据
2. 通过实验了平衡釜的结构,掌握气液平衡数据的测定方法和技能
3. 应用Wilson方程关联实验数据
二、 实验原理
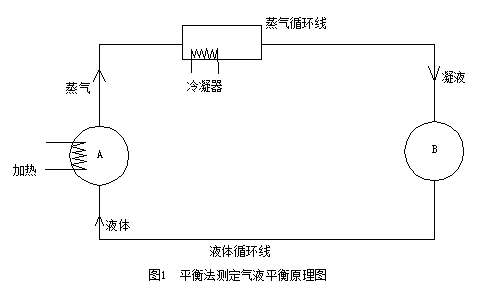
与循环法测定气液平衡数据的平衡釜基本原理相同,如下图所示,体系达到平衡时,两个容器的组成不随时间变化,这时从A和B 两容器中取样分析,可得到一组平衡数据。
当达到平衡时,除了两相的压力和温度分别相等外,每一组分的化学位也相等,即逸度相等,其热力学基本关系为:
fiL=fiV……………………………………….(1)
φipyi=γifi0xi
常压下,气相可视为理想气体,再忽略压力对液体逸度的影响,fi=pi0从而得出低压下气液平衡关系为:
pyi=γipi0xi…………………………………(2)
式中,p——体系压力(总压);
pi0——纯组分I在平衡温度下饱和蒸汽压,可用安托尼(Antoine)公式计算;
xi、yi——分别为组分I在液相和气相中的摩尔分率;
γi——组分i的活度系数。
由实验测得等压下气液平衡数据,则可用
 ………………………………..(3)
………………………………..(3)
计算出不同组成下的活度系数。
本实验中活度系数和组成关系采用Wilson方程关联。Wilson方程为:
lnγ1=-ln
 ………(4)
………(4)
lnγ2=-ln ………(5)
………(5)
Wilson方程二元配偶参数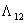 和
和 采用非线形最小二乘法,由二元气液平衡数据回归而得。
采用非线形最小二乘法,由二元气液平衡数据回归而得。
目标函数选为气相组成误差的平方和,即
F= (y1实-y1计)2j+(y2实-y2计)2j…………………………………(6)
(y1实-y1计)2j+(y2实-y2计)2j…………………………………(6)
三、实验装置和试剂
1. 平衡釜一台(平衡釜的选择原则:易于建立平衡、样品用量少、平衡温度测定准确、气相中不夹带液滴、液相不返混及不易暴沸等。本实验采用气液双循环的小平衡釜,其结构如图2所示)
2. 阿贝折射仪一台
3. 超级恒温槽一台
4. 50-100十分之一的标准温度计一支、0-50十分之一的标准温度计一支
5. 所用试剂(苯、正庚烷)为优级品。
6. 1ml注射器十支、5ml注射器三支。

四、实验步骤
1. 开启超级恒温槽,调温度至测定折射率所需温度25℃或30℃
2. 测温套管中倒入甘油,将标准温度计插入套管中,并在其露出部分中间固定一支温度计,对温度进行校正
3. 查整个系统的气密性,以保证实验装置具有良好的气密性,将气压球与三通管连接好,与大气相通,用手压瘪气压球,然后开启气压球所连小阀直通系统,抽气使设备处于负压状态,U型管压力计的液面升起,在一定值下停止。注意操作不能过快,以免将U型管液体抽入系统。关闭气压球所连小阀,停10分钟,U型管内液体位差不下降为合格。开启气压球所连小阀[j1] ,使系统直通大气。
4. 于实验测定的是常压下的气液平衡数据,读取当天实验室的大气压值。
5. 平衡釜内加入一定浓度的苯—正庚烷混合液约20—30毫升,打开冷却水,安放好加热器,接通电源。开始时加热电流给到0.1A加热,5分钟后给到0.2A,再等5分钟后慢慢调到0.25A左右即可,以平衡釜内液体能沸腾为准。冷凝回流液控制在每秒2—3滴,稳定回流15分钟左右,以建立平衡状态。
6. 到平衡后,需要记录下两个温度计的读数,并用微量注射器分别取两相样品2毫升,用阿贝折射仪测定其折射率,并在本实验给定的苯的组成—折射率曲线上确定样品的组成。关掉电源,拿下加热器,釜液停止沸腾。
7. 注射器从釜中取出2~5毫升的混合液,然后加入同量的一种纯物质,重新加热建立平衡。加入那种物质,可以依据你上一次的平衡温度而定,以免实验点分布不均。本实验是降温操作,取出的混和液5毫升,加入苯7毫升,实验重复5次。
8. 实验完毕,关掉电源和水源,处理实验数据。
五、实验数据处理及结论
(一)实验条件及给定数据
①实验条件
实验温度:25.5℃ 大气压:101.19Kpa
②纯组分在常压下的沸点
苯:80.4 ℃ 正庚烷:98.4℃
③水银温度计检定结果
表1:水银温度计显示值及修正值对应表(实验给定)

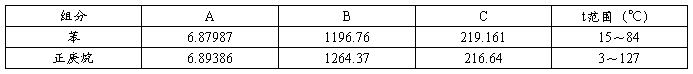
④苯和正庚烷纯物料的Antoine常数
表2:纯物料的安托尼常数
(二)苯—正庚烷混合液气液平衡数据的测定实验原始数据
表3 苯—正庚烷混合液测定实验沸点温度,以及气(苯含量)液平衡组成
(三)平衡温度计算
平衡温度的计算方法如下:
t实际=t主+t修正+t校正值
t修正:通过精查温度计的修正值得到,见表1
t校正值:t校正值=kn(t主-ts)
k——水银在玻璃中间的膨胀系数取0.00016;
n——露出部分的温度系数取60
t主——在介质中的温度;
ts——露出水银柱的平均温度(即辅助温度计的读数)
平衡温度计算结果见表4
表4 苯—正庚烷混合液测定实验实际温度计算结果
表4注:表中修正温度由主温度在表1所给温度修正值在三次样条插值而得,最终实际温度计算结果保留一位小数,是因为主温度测定的精度决定的。
附:修正水银温度计时所用三次样条插值程序(用matlab编写)
t0=[87.8 84.0 82.4 81.3]
x=[50 55 60 65 70 75 80 85 90 95 100]
y=[0.01 0.07 0.10 0.12 0.09 0.05 0.08 0.07 0.07 0.09 0.08]
yy=spline(x,y,t0)
ts=[26.0 26.0 25.0 25.0 25.0];
tj=0.00016 * 60 .*(t0-ts);
t=t0+tx+tj
运行结果:
t = 88.49 84.65 83.05 81.94
(四) 苯和正庚烷纯组分在本实验不同温度下的饱和蒸汽压的计算
由Antoine(安托尼)公式:
lgPi0=Ai – Bi/(Ci+t)
式中:
t—温度,℃(即计算所得的实际温度) P0—饱和蒸汽压,mmHg
所以可得到:
Pi0=10(Ai-Bi/(Ci+t))
纯物料的Antoine常数见表2
纯组分饱和蒸汽计算结果见表5
表5:纯组分饱和蒸汽在实验温度下计算结果
(五)用非线形最小二乘法回归配偶参数Λ12、Λ21并求液相组成
①活度系数和组成关系采用Wilson方程关联
lnγ1=-ln

lnγ2=-ln
目标函数选为气相组成误差的平方和,即
F= (y1实-y1计)2j+(y2实-y2计)2j
(y1实-y1计)2j+(y2实-y2计)2j
用非线性最小二乘法拟合:matlab拟合程序见下
主程序:
bb0=[1,1]
[bb,resnorm]=lsqnonlin('qiye',bb0)
子程序:
function F=qiye(bb)
x1=0.01*[37.2 55.2 65.2 74.8];
x2=1-x1;
y1=0.01*[52.0 67.2 75.2 81.8];
y2=1-y1;
Pa0 =[976.962 872.390 831.487 804.001];
Pb0 =[562.536 498.125 473.079 456.299];
for i=1:4
F(i)=y1(i)-Pa0(i)*x1(i)/760*exp(-log(x1(i)+bb(1)*x2(i))+x2(i)*(bb(1)/(x1(i)+bb(1)*x2(i))-bb(2)/(x2(i)+bb(2)*x1(i))))
end
for i=5:8
j=i-4
F(i)=y2(j)-Pb0(j)*x2(j)/760*exp(-log(x2(j)+bb(2)*x1(j))+x1(j)*(bb(2)/(x2(j)+bb(2)*x1(j))-bb(1)/(x1(j)+bb(1)*x2(j))))
End
拟合结果为:
bb = 1.0361 0.7112
resnorm = 6.2948e-004
也就是:
Λ12= 1.0361
Λ21= 0.7112
resnorm= 6.2948e-004
(六)求气相组成:
由matlab算出y实测-y计算程序如下:
bb =[1.0361 0.7112];
x1=0.01*[37.2 55.2 65.2 74.8];
x2=1-x1;
y1=0.01*[52.0 67.2 75.2 81.8];
y2=1-y1;
Pa0 =[976.962 872.390 831.487 804.001];
Pb0 =[562.536 498.125 473.079 456.299];
for i=1:4
F(i)=y1(i)-Pa0(i)*x1(i)/760*exp(-log(x1(i)+bb(1)*x2(i))+x2(i)*(bb(1)/(x1(i)+bb(1)*x2(i))-bb(2)/(x2(i)+bb(2)*x1(i))));
end
for i=5:8
j=i-4
F(i)=y2(j)-Pb0(j)*x2(j)/760*exp(-log(x2(j)+bb(2)*x1(j))+x1(j)*(bb(2)/(x2(j)+bb(2)*x1(j))-bb(1)/(x1(j)+bb(1)*x2(j))));
end
F
得到
F = -0.0156 -0.0020 0.0105 0.0098 -0.0005 0.0106 0.0055 0.0055

F= (y1实-y1计)2j+(y2实-y2计)2j=(-0.0156)2+(-0.0020)2+…+0.00552+0.00552=0.000627
(y1实-y1计)2j+(y2实-y2计)2j=(-0.0156)2+(-0.0020)2+…+0.00552+0.00552=0.000627
与程序拟和的结果参数一致。
(七)用实验值和计算值作温度组成图(t—x—y)
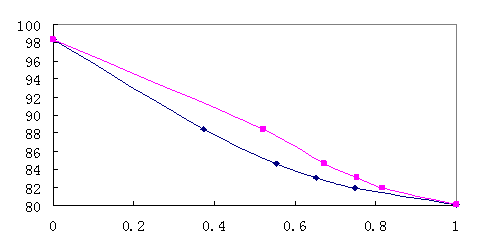
图3 苯的气液平衡图
(八) 实验结果讨论及误差分析
(1)实验结果讨论
从实验的结果的相图和气相组成的实验值和计算值的比较来看,本次实验测得以及回归所得实验数据可靠,误差均在实验允许范围内。从相图可以看出,本实验数据很好的体现了常规二元气液平衡相图规律。应用Wilson方程关联实验数据,并采用非线性最小二乘法进行回归处理,得出配偶参数,再求出气相组成,所得气相组成误差平方和为0.00627。即计算值和实验值的误差非常小,可以用关联得到的Wilson方程计算该物系的组成。
(2)实验误差分析
由于本次实验只是降温操作,每次均是取出混和液,加入纯苯,所以整个实验过程测定的温度是逐渐下降的,而且实验测定的气液相平衡组成是采集的数据点也不是十分的充足,以致相点分布欠佳。在使用阿贝折射仪测定折射率的时候存在读数误差,以及由折射率在折射率—组成的工作曲线上读取气液相组成时候存在误差。读取温度计的温度的时候存在估读误差。对计算结果回造成影响。取样的时候是否平衡釜已经达到气液平衡,且平衡釜上方汽相贮液槽内液体组成是否已经等于平衡气相组成,会对测定产生很大影响。
六、思考题
(1)实验中怎样判断气液两相已达到平衡?
答:实验中采用对比法来判断气液两相是否达到平衡。即先记录下来一个体系的温度,然后每隔2至3分钟读一次温度,如果相邻两次温度读数不再发生变化,则可判定气液两相达到平衡。
(2)影响气液平衡测定准确度的原因有那些?
答:①装置的气密性;②平衡温度的读取;③由阿贝折射仪读取混和液折射率的误差;④在阿贝折射仪工作曲线上由折射率读取气液相组成存在读数误差;⑤取样时气液是否达到平衡;⑥是否选取了合理的取样点。
(3)为什么要确定模型参数,对实际工作有何作用?
答:由于温度变化,但参数不会变,确定模型参数后,对于同样的物系,都可以使用,省去了实验的时间,直接计算就可,获得数据更快速、更方便。模型参数对于实际工作中有着很好的指导作用,而且Wilson方程有了二元参数后,可以用来预测多元混合物的性质。
[j1]调节三通阀
