实验三 草酸加热分解的差热分析实验
一、 实验目的
1. 了解差热分析仪的构造,掌握差热分析的基本原理及测量方法;
2. 学会差热分析仪的操作,并绘制草酸样品的差热图;
3. 掌握差热分析曲线的处理方法,对实验结果进行分析;
4. 了解热电偶的测温原理和如何利用热电偶绘制差热图。
二、 实验原理概述
差热分析仪的结构如下图所示。它包括带有控温装置的加热炉、放置样品和参比物的坩埚、用以盛放坩埚并使其温度均匀的保持器、测温热电偶、差热信号放大器和信号接收系统(记录仪或微机)。差热图的绘制是通过两支型号相同的热电偶,分别插入样品和参比物中,并将其相同端连接在一起(即并联,见图1)。A两支笔记录的时间—温度(温差)图就称为差热图,或称为热谱图。
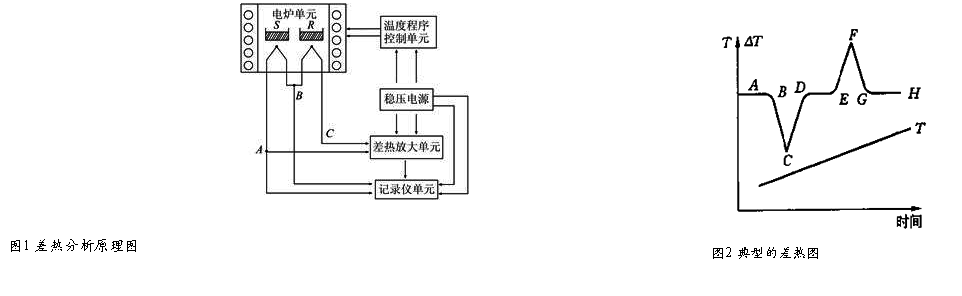
从差热图上可清晰地看到差热峰的数目、位置、方向、宽度、高度、对称性以及峰面积等。峰的数目表示物质发生物理化学变化的次数;峰的位置表示物质发生变化的转化温度(如图2中TB);峰的方向表明体系发生热效应的正负性;峰面积说明热效应的大小:相同条件下,峰面积大的表示热效应也大。在相同的测定条件下,许多物质的热谱图具有特征性:即一定的物质就有一定的差热峰的数目、位置、方向、峰温等,因此,可通过与已知的热谱图的比较来鉴别样品的种类、相变温度、热效应等物理化学性质。因此,差热分析广泛应用于化学、化工、冶金、陶瓷、地质和金属材料等领域的科研和生产部门。理论上讲,可通过峰面积的测量对物质进行定量分析。
温度测量系统:测温热电偶输出的热电势,先经过热电偶冷端补偿器,补偿器的热敏电阻装在天平主机内。经过冷端补偿的测温热电偶热电势由温度放大器进行放大,送入计算机,计算机自动将此热电势的毫伏值转换为温度。
差热测量系统:差热分析(DTA)是在程序温度控制下测量物质与参比物之间温度差随温度变化的一种技术。本仪器采用哑铃型平板式差热电偶,它检测到的微伏级差热信号送入差热放大器进行放大。如试样没有热反应,则它与参比物的温差△T=0;如试样在某一温度范围有吸热(或放热)反应,则试样温度将停止(或加快)上升,试样与参比物之间产生温差△T,把△T的热电势放大后经微机实时采集,可得图3的峰形曲线。
质量测量系统:当物质被加热时,随着温度的增高,物质内部在某一特定温度下产生的物理变化和化学性质的变化(如分解、氧化等)时,常常伴随着物质重量的变化。热重分析的原理就是将被加热试样的质量(或重量)变换成电信号。试样质量m在升温过程中不断变化,就得到热重曲线TGA。如图4。
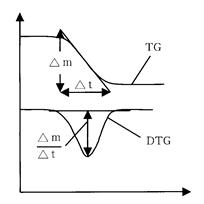

图3 差热曲线 图4 TGA和DTG曲线
试样一般用100~300目之粉末,聚合物可切成碎块或碎片,纤维状试样可截成小段或绕成小球,金属试样可加工成碎块或小粒,试样量一般不超过坩锅容积的五分之四,对于加热时发泡试样不超过坩锅容积的二分之一或更少,或用氧化铝粉沫稀释,以防止发泡时溢出坩埚,污染热电偶。坩埚装样后,可在桌面上轻墩几下。参比物是在测温区内对热高度稳定的物质,一般用α-Al2O3粉沫,粒度为100~300目,最好经过1300℃以上高温焙烧和干燥保存。参比物的导热性能及热容最好与试样接近,以减少差热基线漂移。做金属试样的差热分析时也可用铜或不锈钢做参比物。试样量较少或热容很小时,也可以不用参比物,直接放空坩埚。
三、 实验设备及材料
1. 设备:差热分析仪(SDT Q600)一台;计算机一台;电子天平一台。
2. 材料:分析纯草酸;参比物α-Al2O3。
四、 实验内容
1. 将待测样品放入一只坩埚中,在另一只坩埚中放入重量基本相等的参比物(α-Al2O3)。然后将其分别放在样品托的两个托盘上,盖好保温盖。
2. 启动热分析软件,依次设定所需参数。升温速率设置为10℃/min开始升温。
3. 记录升温曲线和差热曲线,直至温度升至发生要求的相变且基线变平后,停止记录。
4. 打开炉盖,取出坩埚,待炉温降至50℃以下时关闭设备。
五、 实验步骤
1. 启动计算机,打开差热分析程序。
2. 将α-Al2O3和草酸样品放进炉子,装入草酸样品、装满,颠实50次,再次加入草酸将坩埚填满。然后,关闭炉体,点击开始试验。
3. 将温差△T置零,升温速率设为10℃/min,程序开始自动测量温度和温差的变化,观察屏幕上的差热曲线,最后保存实验数据。
4. 当差热曲线出现2个峰以后,停止实验,对炉体进行冷却。当炉内温度降至50℃左右时开炉,取出坩埚。
5. 最后关闭电源,整理仪器。
六、实验注意事项
1. 坩埚一定要清理干净,否则埚垢不仅影响导热,杂质在受热过程中也会发生物理化学变化,影响实验结果的准确性。
2. 样品必须研磨的很细,否则差热峰不明显;但也不要太细。一般差热分析样品研磨到200目为宜。样品要均匀平铺在坩锅底部。否则作出的曲线极限不平整。
3. 实验过程中注意不要动计算机键盘。
七、实验报告及要求
1. 定性说明所得差热图谱的意义。
2. 根据热效应的温度范围,分析出“峰”的具体机理和原因。
3. 对产生的误差进行分析。
八、参考书籍
1. 吴思诚, 王祖铨. 近代物理实验(第3版). 高等教育出版社, 2005.
2. 金丽萍, 邬时清, 陈大勇. 物理化学实验. 华东理工大学出版社, 2005.
第二篇:草酸钙的热重-差热分析
综合热分析法测定草酸钙
【实验目的】
(1)掌握热重-差热分析原理和ZCT-A型综合热分析仪的操作方法,了解其应用范围。
(2)对草酸钙进行热重及差热分析,测量化学分解反应过程中的分解温度。
(3)测量物质在加热过程中所发生的物理化学变化,绘制相应曲线,从而研究材料的反应过程。
【实验原理】
热分析是物理化学分析的基本方法之一。综合热分析研究物质在加热过程中发生相变或其他物理化学变化时所伴随的能量、质量和体积等一系列的变化,可以确定其变化的实质或鉴定矿物。热分析技术种类很多,比较常用的方法有(1)差热法(DTA),(2)热重法(TG)[包括微分热重(DTG)],(3)差示扫描量热法(DSC)。
(1)热重分析
热重分析是在程序控制温度下,测量物质质量与温度关系的一种技术。热重法实验得到的曲线称为热重(TG)曲线。TG曲线以温度作横坐标,以试样的失重作纵坐标,显示试样的绝对质量随温度的恒定升高而发生的一系列变化。这些变化表征了试样在不同温度范围内发生的挥发组分的挥发,以及在不同温度范围内发生的分解产物的挥发。如图1、图2 CaC2O4·H2O的热重曲线,有三个非常明显的失重阶段。第一个阶段表示水分子的失去,第二个阶段表示CaC2O4分解为CaCO3,第三个阶段表示CaCO3分解为CaO。当然,CaC2O4·H2O的热失重比较典型,在实际上许多物质的热重曲线很可能是无法如次明了地区分为各个阶段的,甚至会成为一条连续变化地曲线。这时,测定曲线在各个温度范围内的变化速率就显得格外重要,它是热重曲线的一阶导数,称为微分热重曲线[图1也现示出了CaC2O4·H2O的微分热重曲线(DTG)]。微分热重曲线能很好地显示这些速率地变化。
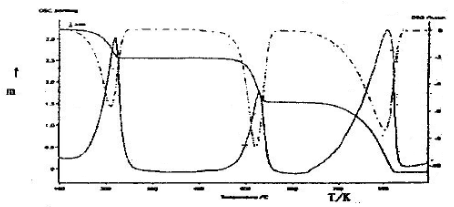
图1 CaC2O4·H2O的TG-DSC曲线(文献图)

图2 CaC2O4·H2O的TG曲线(文献图)
(2)差热分析(DTA)和差示扫描量热分析(DSC)
差热分析(DTA)是在试样与参比物处于控制速率下进行加热或冷却地环境中,在相同地温度条件时,记录两者之间地温度差随时间或温度地变化。差示扫描量热分析(DSC)记录地则是在二者之间建立零温度差所需地能量随时间或温度的变化。
差热分析和差示扫描量热分析所得到的谱图或曲线常画成在恒定加热或冷却的速率下随时间或温度变化的形式,其横坐标相应于时间或温度,作差热分析测量时,纵坐标为试样与参比物之温差,而作差示扫描量热分析时,纵坐标为试样池与参比池之功率差(dΔC/dt)。从图1可以看出,CaC2O4·H2O的DSC曲线(DTA 曲线与DSC 曲线相似)有三个向上的峰,分别表示CaC2O4·H2O热分解时发生了三个吸热反应。所以DSC(或DTA)反映的是所测试样在不同的温度范围内发生的一系列伴随着热现象的物理或化学变化。换言之,凡是有热量变化的物理和化学现象都可以借助于差热分析或差示扫描热分析的方法来进行精确的分析,并能定量地加以描述。
(3)草酸钙热分解过程
CaC2O4·H2O的热分解过程有如下三步:
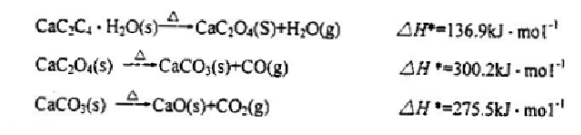
【实验仪器设备及材料】
北京精仪高科仪器有限公司ZCT-A型综合热分析仪;氮气(纯度99.99%);专用坩埚、镊子、药勺;电子分析天平;CaC2O4·H2O(分析纯)。
【实验步骤及方法】
1. 实验前准备
(1)首先应检查仪器连接系统是否正常,样品支架上清洁无任何杂质;
(2)打开N2钢瓶调压阀,将氮气瓶的出口压力调整到0.15-0.2MPa之间,将气氛箱的出口压力调整到0.1MPa,调节流量计的大小在80ml/min左右,开始实验前至少通气30分钟以上以确保空气排净。
(3)开启电脑,待电脑启动完成后,开启综合热分析仪主机上的电源开关,应该能听到仪器的自检报警声,响几声后停止。开机预热仪器至少三十分钟。
(4)用镊子转移坩埚,先将坩埚放于电子分析天平上归零,然后移出天平用专用小药勺往坩埚中添加草酸钙,并准确称取8-10mg(约占据2/3坩埚容积),保证样品在坩埚中均匀铺平,并记录数值。
(5)天平操作(此步骤指导老师操作):抬起炉体,观察托盘的左边是否有参比坩埚(正常情况下该坩埚会一直留在左盘),被测样品放置于托盘的右边;放下炉体。
(6)开启冷却水。
2 实验开始
(1)进入热分析数据站,运行电脑桌面上的“RSZ2013”软件,鼠标左键单击窗口上出现的图片。
(2)量程设置
鼠标左键单击菜单栏上的“新采集”选项,此时系统首先自动进行热重调零,调整完毕后进入“参数设定”画面:
输入“基本实验参数”,操作键盘及鼠标,对试验名称 、试验序号 、操作者姓名 、试样重量 等参数正确输入;对DSC量程,TG量程,DTG量程选取;
输入“升温参数”:操作鼠标、键盘,对起始温度(显示为当前炉温) 、升温速率(≤40℃/min) 20℃/min 、终值温度 950℃等内容输入完毕。具体参数的设置根据用户的实际使用要求按分析步骤进行操作。
单击确定“确定”,此时继电器吸合,加热指示灯亮,此时热分析系统处于工作状态。此时观察状态栏内TG数值应在TG量程的90%左右,不超过量程最大值。如果不符,按取消键重新进行采集。
(3)采集结束
屏上箭头指向“停止”钮,并确认Y、双击鼠标左键,使指示灯灭掉。
(4)数据存储
鼠标左键单击菜单栏的“保存”选项,输入文件名(中文、分子式或字符代号)后;单击“保存”。
3 数据处理
TG-DSC曲线分析
打开保存的文件,根据实验报告的要求,可任选以时间为横轴或温度为横轴(从主菜单“设置”中的“温度坐标”切换得到)。
TG曲线分析:右击鼠标,进入“曲线分析”菜单,选择TG曲线,在该曲线待分析失重段的左端起点双击鼠标左键,然后拖动至所选峰段的右端点处,观察所出现的文字位置是够合适,不合适的话通过上下移动鼠标调整至合适位置,然后松开左键,按上述方法依次分析三个失重过程。
DSC曲线分析:右击鼠标,选择处理DSC曲线,分别在该曲线上的三个吸热峰左端双击鼠标左键,然后拖动至所选吸收峰的右端点处双击,在弹出的窗口的左端选择需要分析的数据,并以此单击左键并将数值移动至合适位置(依次得到外推起始温度Te、峰顶温度Tm、反应峰面积、反应热焓)后单击“返回”键,此时回到原图并显示得到的分析数据。
若对分析结果不满意,单击的主菜单“重画”纽,可删除已写上去的分析数据。
鼠标左键单击主菜单的“打印”钮,此时,将从打印机输出一张“RSZ热分析报告”。
4 系统退出
鼠标左键单击RSZ主菜单的“文件”钮,选择“关闭”项,按屏幕提示正常退出该系统,并依次关闭仪器、电脑、N2钢瓶总阀、冷却水。
【实验注意事项】
(1)转移坩埚和称取样品时,严禁用手直接触碰,而使用专用镊子夹取坩埚,并轻拿轻放;
(2)样品要均匀平铺在坩埚中,保证待测样品受热均匀;
(3)软件没有记忆功能,因此在采样过程中,不能关闭程序;
(4)在仪器分析工作过程中不要触摸仪器和敲打晃动实验台,以免发生触电、灼伤和对分析曲线造成不必要的干扰。
(5)实验结束后,当加热炉温度降至200℃以下时,方可关闭冷却水。
【思 考 题】
如果增大升温速率,CaC2O4·H2O分解温度会发生怎样的变化?
