高三专题复习《化学键》
教学模式:先学后教、当堂达标的高效课堂
教学手段:复习丛书和多媒体辅助教学
复习目标:
1.理解化学键的概念、离子键和共价键的概念。
2.知道化学键与化学反应中物质变化和能量变化的关系。
3.理解离子化合物和共价化合物概念,掌握化学键和化合物的关系。
4.了解化学键强弱对物质性质的影响。
考向分析
本讲重要知识有化学键、离子键、共价键、离子化合物、共价化合物的概念。主要考查化学键及化合物类型的判断,、8电子结构的判断等。预测今后年高考仍会考查物质所含化学键类型的判断为主要考向。
教学过程
【知识梳理】
一、化学键
1.概念:相邻 强烈的 。
2.化学反应的本质:反应物中的 和生成物中的 。
3.化学反应中能量变化的实质是反应物中旧化学键断裂需要 ,生成物中新化学键形成 能量,因此化学反应一定伴随能量变化。
4、化学键的主要类型有 和 。
二、共价键
1.概念:原子间通过 所形成的相互作用。
2.共价键的形成过程 HCl:
3.共价键的分类
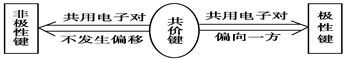
三、离子键
1.概念: 离子之间通过 作用形成的化学键。
2.离子键的形成过程 NaCl:
四、离子化合物和共价化合物
1.共价化合物是 的化合物,离子化合物是 的化合物。
2、化学键与化合物关系

【自学检测】
1.现有如下各种说法:
①在水中氢、氧原子间均以化学键相结合 ②金属和非金属化合时一定形成离子键 ③离子键是阳离子、阴离子的相互吸引力 ④根据电离方程式HCl===H++Cl-,判断HCl分子里存在离子键 ⑤H2分子和Cl2分子的反应过程是H2、Cl2分子里共价键发生断裂生成H原子、Cl原子,而后H原子、Cl原子形成离子键的过程
上述各种说法正确的是( )
A.①②⑤ B.都不正确 C.④ D.①
2.下列各组物质中化学键类型相同的是( )
A.HCl、MgCl2、NH4Cl B.H2O、Na2O、CO2
C.CaCl2、NaOH、H2O D.NH3、H2O、CO2
3.食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是( )
A.炒菜时放入食盐并不破坏NaCl中的化学键 B.HCl是共价化合物
C.NaCl熔化时破坏共价键 D.HCl的结构式是H—Cl
【合作探究】
1、化学键是一种强烈的静电吸引作用吗?
所有物质中都存在化学键吗?
水中相邻的氢、氧原子间均以化学键结合吗?
化学键被破坏一定发生化学变化吗?
2、仅由非金属元素组成的物质中一定不含离子键吗?由金属元素和非金属元素一定形成离子键吗?
3、离子化合物含有哪些化学键?举例说明。
4、在化合物和离子化合物中原子一定达到8电子稳定结构吗?举例说明。
【要点总结】
1、化学键概念:
①相邻 ②强烈作用
③作用力不仅有引力还存在同性电荷间的斥力作用。
④分子间的相邻原子间存在较弱的作用力是分子间作用力(范德华力)。
2、化学键与物质的关系:
①一般非金属元素通过共价键结合形成物质。有非金属单质O2、H2金刚石等;非金属形成的化合物如氢化物、氧化物、含氧酸、有机化合物;碱中的OH-,盐中的复杂的阳离子如NH4+、复杂阴离子如CO32-。
②活泼的金属和活泼的非金属通过离子键形成化合物。有金属氧化物如Al2O3;碱如KOH;盐如NH4Cl、NaCl等。
③稀有气体本身原子核外最外层均是稳定结构,不存在化合价,是单原子分子。
3、化合键与化合物:
①根据化合物中含有的化学键不同,把化学键分为共价化合物和离子化合物。
②共价化合物只含共价键,不含离子键;离子化合物一定含离子键,可能含共价键。
③对于电解质,离子化合物的电解质在熔融状态下能电离能导电,共价化合物的电解质只有在水溶液中能电离能导电。
④在化合物中原子通过共用电子或得失电子的方式形成稳定结构,可能是最外层8电子如CCl4,也有2电子如NaH,还有课能是特殊结构如PCl5。
4、化学键与化学反应:
①化学反应的实质是反应物中旧化学键断裂同时在生成物中形成新的化学键的过程
②化学反应中能量变化是由于化学键变化导致的
③化学键破坏,不一定发生化学反应,如物质的电离。
【例题展示】
例题1:将HCl、Ar、NH3、MgO、CO2、NaCl、NaOH、C6H12O6、C2H4、金刚石、N2、NH4NO3、H2O2、Na2O2、AlCl3等物质按以下要求填空:
(1)只存在共价键的是______________________。
(2)只存在离子键的是______________________。
(3)既存在离子键,又存在共价键的是____________________。
(4)既不存在离子键,又不存在共价键的是________________。
(5)属于离子化合物的是 ,属于共价化合物的是 。
(6)含有非极性键的离子化合物 ,含有非极性键的共价化合物 。
★教师点拨:判断化学键类型的方法:
1、看构成元素。非金属元素间是共价键,活泼非金属和活泼金属是离子键。
2、看物质的类型。只共价键的物质有:非金属单质、非金属氢化物、非金属氧化物、酸、有机物;只含离子键的有:金属氧化物、简单的盐如NaCl、金属氢化物如NaH。即含共价键又含离子键的有:碱、含复杂离子的盐如NH4Cl、含活泼金属的特殊化合物如Na2O2。
例题2:
X、Y为两种短周期主族元素,其原子的最外层电子数分别为1和6,则X、Y两种元素形成的化合物( )
A.一定是离子化合物 B.一定是共价化合物
C.一定形成X2Y型化合物 D.以上答案均不正确
★教师点拨:最外层1电子可能是短周期主族元素H或Na,最外层6电子的元素为短周期的O或S,因此形成的化合物可能为共价化合物H2O、H2S,也有可能为离子化合物Na2O、Na2S、Na2O。
【走近高考】
(2011·浙江高考T9有改动)X、Y、Z、M、W为五种短周期。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的。下列说法正确的是( )
A.原子半径:W>Z>Y>X>M
B.XZ2、X2M4、W2Z2均为共价化合物
C.由X元素形成的单质存在同素异形体
D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
★教师点拨:高考中常把元素周期表的考察与化学键的判断结合在一起,增大了题目的难度,只有正确推断出元素,才可以对选项中性质的比较、化学键判断、分子结构等做出正确判断。
【当堂达标】
1.下列说法中不正确的是( )
A.金属和非金属原子之间一定形成离子键 B.两个非金属原子之间形成的化学键一定是共价键
C.含有离子键的物质不可能是单质 D.单质中不一定含有共价键
2.下列每组中各物质内既有离子键又有共价键的一组是( )
A.NaOH、H2SO4、(NH4)2SO4 B.MgO、Na2SO4、NH4HCO3
C.Na2O2、KOH、Na2SO4 D.HCl、Al2O3、MgCl2
3.原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物,Y与氧元素可组成Y2O和离子化合物Y2O2。
(1)写出Y2O2的结构式__________________。其中含有的化学键是 _______________。
(2)用方程式表示Z和Y生成化合物的过程 _____________________________________。
(3)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是________(化学式)
教学反思与评价

第二篇:化学键总结
1.化学键
化学反应的实质:旧化学键的断裂,新化学键的形成。 阴、阳离子通过静电作用而形成的化学键叫做离子键。
离子键形成条件: 活泼金属元素与活泼非金属元素之间容易形成。 电子式:标出【】和电荷
原子之间通过共用电子对的相互作用所形成的化学键,叫做共价键。 共价键形成条件: 一般是非金属元素原子间的相互作用 非极性键: 同种非金属元素原子之间形成非极性共价键 极性键: 不同种非金属元素原子之间形成极性共价键 如:H2、Cl2、HCl、CO2 等分子中均含有共价键。
2.化学键与物质构成
? 离子化合物——含有离子键的化合物; ? 共价化合物——只含有共价键的化合物。
说明:①离子化合物含有离子键,也可能同时含共价键. 如NaOH、Na2SO4 、 NH4Cl等 ②当一个化合物中同时存在离子键和共价键时,该化合物称为离子化合物
③ 当一个化合物只含有共价键时,该化合物才称为共价化合物 如:H2、Cl2、HCl、CO2 ④酸类物质均属于共价化合物,强碱均属于离子化合物,
大多数盐类物质属于离子化合物(但AlCl3、FeCl3、NH4Cl例外,它们属于共价化合物)。 下列变化不需要破坏化学键的是:( ) A. 加热分解氯化铵 B. 干冰气化 C. 水通电分解 D. 氯化钠溶于水 . 下列几组化合物,化学键型不相同的是:( ) A. NH3 和H2O B. HCl和HNO3 C. H2S和Na2S D. CaCl2和NaCl
下列微粒中,含有离子键又含有共价键的是( ) A. NH3 B. NH4Cl C. H2S D. KCl 下列说法中正确的是 ( C )
(A) 含有共价键的分子一定是共价分子 (B)只含有共价键的物质一定是共价化合物
(C)离子化合物中可能含有极性共价键或非极性共价 键 (D)氦分子中含有共价键
判断下列化合物中含有哪些类型化学键,是离子化合物还是共价化合物
NaF CH4 H2O CaO KBr HF CaCl2 O2 CO2 NH3 NaNO3 NaOH HNO3 B C BC
也可能是离子化合物,如 NaOH, Na2O2 。 也可能是单质分子,如氯气,氮气。 氦气是单原子分子,不存在化学健。
离子化合物:NaF、CaO、KBr、CaCl2、NaNO3、NaOH 共价化合物:CH4、H2O、HF、O2、CO2、NH3、HNO3
2. 分子间作用力和氢键
把分子聚集在一起的作用力叫做分子间作用力(也叫范德华力)
(1)分子间作用力比化学键弱得多,是一种微弱的相互作用,它主要影响物质的熔、沸点等物理性质,而化学键主要影响物质的化学性质。
(2)分子间作用力主要存在于由分子构成的物质中,如:多数非金属单质、稀有气体、非金属氧化物、酸、氢化物、有机物等。
(3)分子间作用力的范围很小(一般是300-500pm),只有分子间的距离很小时才有。 (4)一般来说,对于组成和结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔、沸点越高。如卤素单质:F2<Cl2<Br2<I2 又如气态氢化物:Cf4<Ccl4<Cbr2<Ci4
但一些氢化物HF、H2O和NH3的沸点会反常,由于氢键
氢键 :由于氢原子的存在而使分子间产生的一种比分子间作用力稍强的
相互作用——氢键。
(1)氢键不属于化学键,比化学键弱得多,比分子间作用力稍强,也属于分子间作用力的范畴,
(2)形成条件:氢原子与得电子能力很强、原子半径很小的原子形成的分子之间。如HF、H2O、NH3等分子间易形成氢键。 (3)特征:具有方向性。
(4)结果1:氢键的形成会使含有氢键的物质的熔、沸点大大升高。如:水的沸点高、氨易液化等。这是因为固体熔化或液体汽化时,必须破坏分子间作用力和氢键 (5)结果2:氢键的形成对物质的溶解性也有影响,如:NH3极易溶于水。
