燃料及其利用
一、燃烧
1、定义:可燃物与氧气发生的一种发光、放热的剧烈的氧化反应。
2、燃烧的条件: ①可燃物; ②必须与氧气(或空气)接触; ③温度要达到着火点。
3、我们所见到的燃烧一般都是可燃物在空气或氧气中的燃烧,事实上,燃烧还可以 在其他一些气体环境中进行。例如镁可以在氮气和二氧化碳中燃烧,钠在氯气中燃烧,因此,凡是发光、放热的剧烈的氧化反应都叫燃烧。
二、灭火的原理和方法
1、燃烧需要同时满足三个条件,若破坏其中的任何一个条件,就能达到灭火
的目。
2、由燃烧的条件可推论灭火的原理:
①清除可燃物或使可燃物与其他物品隔离。
②使可燃物隔绝氧气(或空气)。
③使温度降低到可燃物的着火点以下。
3、以下几种灭火的方法都是利用了上述原理:
①将未燃烧的可燃物搬离火灾现场,就是清除可燃物;
②用沙土灭火,就是使可燃物隔绝空气; ③用水灭火,就是使温度降低到可燃物的着火点以下。
4、常用灭火器有:泡沫灭火器、干粉灭火器、二氧化碳灭火器,应根据不
同的火灾,采用不同的灭火器。
1
三、爆炸
1、爆炸:可燃物在有限的空间内急剧地燃烧,就会在短时间内聚积大量的热,使气体的体积迅速膨胀而引起爆炸。
2、 一切可燃性气体、可燃性液体的蒸气、可燃性粉尘与空气(或氧气)的混合物遇火种均有可能发生爆炸。
四、燃料和能量
1、三大化石燃料: 煤、石油、天然气(混合物、均为不可再生能源)。
(1)煤:“工业的粮食”(主要含碳元素);煤燃烧排放的污染物:SO2、NO2(引起酸雨),CO、烟尘等。
(2)石油:“工业的血液”(主要含碳、氢元素)。
(3)天然气是气体矿物燃料(主要成分:甲烷),是较清洁的能源。
2、两种绿色能源:沼气、乙醇
(1)沼气的主要成分:甲烷.甲烷的化学式: CH4(最简单的有机物,相对分子质量最小的有机物)。
物理性质:无色,无味的气体,密度比空气小,极难溶于水。
化学性质: 可燃性 CH4+2O2CO2+2H2O (发出蓝色火焰)
(2)乙醇 (俗称:酒精, 化学式:C2H5OH)
化学性质: 可燃性 C2H5OH+ 3O22CO2+3H2O
工业酒精中常含有有毒的甲醇CH3OH,故不能用工业酒精配制酒!
乙醇汽油的优点:(1)节约石油资源 (2)减少汽车尾气
(3)促进农业发展 (4)乙醇可以再生
3、化学反应中的能量变化:
(1) 放热反应:如所有的燃烧 (2)吸热反应:如C+CO22CO
4、燃料充分燃烧的条件是:
(1)燃烧是要有足够多的空气; (2)燃料与空气要有足够大的接触面
2
五、使用燃料对环境的影响
1、酸雨的危害:(1)腐蚀建筑物 (2)影响水生物、动植物生长
(3)污染江河湖泊 (4)影响农作物和森林的生长等。
2、防止酸雨的形成:
(1)、减少煤中的含硫量,对煤炭中的硫资源进行合理的开发和利用;
(2)、工厂排出的废气要处理;(3)、开发新能源;(4)、加强环境监测。
3、煤和石油等化石燃料燃烧造成对空气的污染 ,主要有以下几个方面原因:
(1)燃料中的一些杂质如硫等燃烧时,产生SO2等;
(2)燃料燃烧不充分 ,产生CO;
(3)末燃烧的碳氢化合物及碳粒,尘粒等排队放到空气中。
4、汽车尾气中的主要污染物:有NO,末燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘。
5、减少汽车尾气对空气的污染可采取措施:
(1)使用催化净化装置,使有害气体转化为无害气体;
(2)使用无铅汽油,禁止含铅物质的排放;
(3)改进发动机的燃烧方式,以使汽油能充分燃料;
(4)使用压缩天然气和液化石油气;(5)开发新能源等。
6、新能源(1)氢能.风能.核能.太阳能.地热能和潮汐能等。
(2)开发新能源的作用:解决化石能源枯竭,减少环境污染。
7、人类能源的新希望——可燃冰
(1)可燃冰的化学名称为“天然气水合物”。
(2)可燃冰是由天然气(主要成分为甲烷)和水在低温、高压的条件下形成的冰状固体,因其极易燃烧,因此称为“可燃冰”。
1、通常使可燃物燃烧的条件是 ( )
(1)可燃物跟氧气(或空气)接触 (2)将可燃物加热
(3)使可燃物跟气体接触 (4)达到可燃物的着火点
A、(1)和(2) B、(3)和(4) C、(2)和(4) D、(1)和(4)
2、点燃的火柴竖直向上,火柴梗不易继续燃烧,其原因主要是 ( )
A、火柴梗温度达不到着火点 B、火柴梗着火点较高
C、火柴梗潮湿不易燃烧 D、火柴梗接触氧气较少
3
3、下列现象中,一定由化学变化引起的是 ( )
A、发光发热 B、爆炸 C、燃烧 D、蒸发
4、关于燃烧,下列说法正确的是 ( )
A、可燃物燃烧时,一定有发光、发热的现象 B、都是有氧气参与的反应
C、可燃物燃烧时一定有火焰产生 D、在纯氧中任何物质都可以燃烧
5、下列场所中,宜贴上“严禁烟火”标语的是 ( )
A、石灰窑厂 B、炼铁厂
C、面粉加工厂 D、制冰厂
6、下列情况: ①煤的燃烧; ②工业废气的任意排放; ③燃放鞭炮; ④以汽油为燃料汽车尾气的排放; ⑤用氢气为燃料的新型燃气车排放的尾气。会引起空气污染的是 ? ?
A.①④⑤ B.①②③ C.①②③④ D.①②③④⑤
7、下列做法存在严重事故隐患的是 ? ? A.用石灰沙浆抹墙 B.用干冰制造舞台上的云雾
C.将液化石油气的残液倒入下水道 D.将活性炭放在冰箱内去除异味
8、在治理城市空气污染中所采取的措施不正确的是 ? ?
A.焚烧落叶 B.增大绿化面积 C.减少用煤作燃料 D.汽车改用清洁燃料
9、随着经济的发展,能源与环境问题成为人们日益关注的热点。从发展的角度看,你认为下列燃料中最理想的是 ? ?
A.煤 B.石油 C.氢气 D.天然气
10、根据你的生活经验和所学知识判断,下列做法错误的是 ? ?
A.电线短路着火,立即用水浇灭 B.加油站、面粉厂贴有“禁止烟火”的标志
C.焊割金属时,用稀有气体作保护气 D.做菜时油锅不慎着火,迅速用锅盖盖灭
11、20xx年常德桥南 “12 .21”特大火灾教训惨痛, 如果室内遭遇火灾时, 下列自救措施中不正确的是 ? ?
A.尽快到达最近的可用楼梯出口逃走 B.可将湿毛巾捂在口鼻上做防毒面具
C.房间内浓烟弥漫时,可匍匐爬行逃走 D.躲在衣柜内等待求援
12、图书馆或存放精密仪器的工作室失火, 应使用的灭火器是 ? ?
A.泡沫灭火器 B.液态二氧化碳灭火器
C.干粉灭火器 D.以上三种灭火器均可
13、酸雨对下列设施和建筑物损害最少的是 ? ?
A.大理石塑像 B.铝合金制品
C.钢梁大桥孔 D.柏油道路
4
第二篇:九年级化学上册第四单元知识点
第四单元知识点
一、水
1、水的组成:(重点)
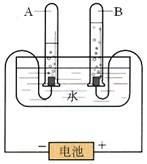
(1)电解水的实验
a.装置--水电解器
b.电源种类--直流电
c.加入硫酸或氢氧化钠的目的--增强水的导电性
通电d.反应原理:水 → 氢气 + 氧气
产生位置 负极 正极
体积比 2 : 1 (口诀:正氧负氢,氢二氧一) 体积比偏大的原因:1、氧气的溶解能力比氢气强
2、氧气的氧化性强,与电极发生反应,消耗了一部分 e.检验:O2:出气口置一根带火星的木条,现象:木条复燃
H2:出气口置一根燃着的木条,现象:气体燃烧,产生淡蓝色的火焰,放热
(2)结论: 直接结论:①水是由氢、氧两种元素组成的。
氢气是由氢元素组成的。
氧气是由氧元素组成的。
间接结论:②化学变化中,分子可分而原子不可分。
③电解水产生气体体积比=分子个数比
④一个水分子由两个氢原子和一个氧原子构成
从图中所获得的信息:
宏观方面:①水通电生成氢气和氧气
②在化学变化中元素的种类不变
③水是由氢、氧两种元素组成的
④氢气是由氢元素组成的
⑤氧气是由氧元素组成的
⑥此反应是分解反应
微观方面:①水由水分子构成
②每个水分子由一个氧原子和两个氢原子构成
③氢气由氢分子构成
④每个氢分子由两个氢原子构成
⑤氧气由氧分子构成
⑥每个氧分子由两个氧原子构成
⑦在化学变化中,分子的种类改变,原子的种类和数目不变。 ⑧氢原子的体积比氧原子小
2、水的污染: 1% 。 (1(2;
②农药、化肥的不合理施用
③生活污水的任意排放
(3)爱护水资源:
①节约用水
②防止水体污染(措施):工业三废要经处理达标排放、提倡零排放;


- 1 -
生活污水要集中处理达标排放、提倡零排放;
合理施用农药、化肥,提倡使用农家肥;加强水质监测。
3、水的净化(蒸馏的标准装置不是中考课标要求、活性炭吸附和过滤是重点)
(1)水的净化效果由低到高的是:
静置沉淀
明矾(KAl(SO4)2·12H2O)吸附沉淀:玻璃棒搅拌的作用是加速溶解
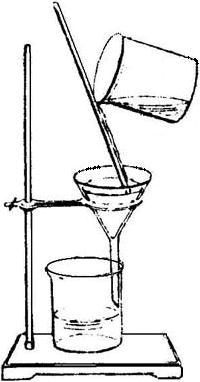
过滤:除去不溶性固体小颗粒
活性炭吸附:①吸附一些可溶性杂志、臭味和色素(主要)②滤去不溶性物质(次要) 消毒:O3、ClO2、Cl2、漂白粉----消灭大肠杆菌(消毒效果由高到低)
蒸馏:蒸馏过后的水是纯净物
★注意:除消毒外其余净化方法均为物理方法。
其中净化效果最好的操作是蒸馏。
★ 过滤的注意事项:(重点)
一贴:滤纸紧贴漏斗内壁----加快过滤速度
二低:滤纸低于漏斗边----贴紧,加快过滤速度
液面低于滤纸边----防止液体未经过滤,使滤液浑浊
三靠:烧杯紧靠玻璃棒----防止液体洒出
玻璃棒轻靠三层滤纸重叠处----防止滤纸破损
漏斗下端紧靠烧杯内壁----防止滤液飞溅
★过滤后仍然浑浊的原因:①滤纸破损;②盛接仪器不干净;③滤液高于滤纸边 ★过滤速度减慢的原因:①滤纸和漏斗间有气泡;②大颗粒不溶物堵塞滤纸孔
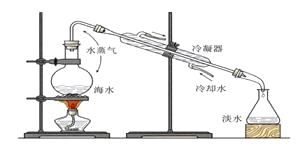
★蒸馏装置的注意事项:(理解就可以)
如果是正规装置,冷凝管下进水上出水的目的:使水填满冷凝管,起到更好的冷凝效果 烧瓶中放碎瓷片的作用:防止暴沸
刚开始的馏分弃掉,以防仪器中的杂质溶解在蒸馏水中
如果是简易装置,接蒸馏水的试管浸没在冷水浴中,使水蒸气冷凝
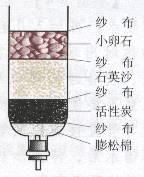
如果是简易装置,实验完毕后先移走导管,再熄灭酒精灯:防止冷凝水倒流,炸裂试管 ★简易净水器
所有的物质都有过滤作用,层层过滤,由粗到精,
顺序不能改变。
最上面一层纱布的作用:过滤
其余三层的纱布作用:隔离上下两层不同的物质
★分离混合物的两种物理方法:
a.过滤:除去不溶性杂质,利用物质的溶解性不同。
例:分离氯酸钾用二氧化锰做催化剂反应后的剩余物质氯化
钾和二氧化锰,因为氯化钾是能溶于水的,而二氧化锰不能溶
于水,所以先将混合物加水充分溶解再过滤,滤纸上得到的剩
余物为二氧化锰,滤液中的物质蒸发结晶之后就是氯化钾。
b.蒸馏:除去可溶性杂质,利用两种物质的沸点不同。
例:分离酒精和水。在78.5℃达到酒精的沸点,酒精先蒸发出;在100
℃达到水的沸点,
- 2 -
蒸发出蒸馏水。
(2)硬水与软水:(重点)
a.定义 硬水是含有较多可溶性钙、镁化合物的水;
软水是不含或含较少可溶性钙、镁化合物的水。
b.鉴别方法:用肥皂水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水
c.硬水软化的方法:实验室常用蒸馏的方法,生活中常用煮沸的方法
d.长期使用硬水的坏处:①浪费肥皂,洗不干净衣服;②锅炉容易结成水垢,不仅浪费燃
料,还易使管道变形甚至引起锅炉爆炸。③长期饮用容易引起结
石。
二、氢气 H2
1、物理性质:密度最小的气体(向下排空气法收集);难溶于水(排水法收集)
2
2H+O==点燃 =2 HO 点燃前,要验纯 文字表达式:氢气+22 2
上方,杯壁有水珠产生。
(验纯方法:用试管收集氢气靠近火焰,发出“噗”的一声说明氢气较纯,发出尖锐的爆鸣声说明氢气不纯,氢气不纯时点燃易发生爆炸)
3、氢能源三大优点:无污染、放热量高、来源广
三、物质的组成、构成及分类
组成:物质(纯净物)由元素组成 原子:金属、稀有气体、金刚石、石墨、硅等
物质构成 分子:如水由水分子构成 H2O、H2、O2、N2、Cl2
+-离子:如氯化钠由钠离子(Na)氯离子(Cl)构成 NaCl、MgCl2
混合物(多种物质)
分类 单质 :金属、非金属、稀有气体
纯净物 (一种元素)
化合物
其中一种是氧元素的化合物
其他
注意:只含一种元素的物质不一定是单质,还可能是混合物如:O2 ,和O3
含多种元素的物质不一定是化合物还可能是混合物
含氧元素的物质不一定是氧化物如KClO3 ,O2
- 3 -
