��һ��������Ԫ�ص�ԭ�ӽṹ�����ʵĵݱ����

������������������
����������������ͬ�������壬�����г�����������ı���ɡ
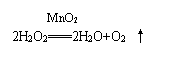
�������ⲻ�ȶ��ֽ⣬������������Ư����
����֪ʶ��ϵ
3�������������������
��ɫ���д̼�����ζ���ж����壻�ܶȱȿ�����������ˮ��1��40�����������ڽ�����Ȫʵ�飬��SO2��HCl��NH3������Һ������10�棩
4����������Ļ�ѧ����
1��������������
�ܺͼӦ�����κ�ˮ��SO2+2NaOH===Na2SO3+H2O
��ˮ��Ӧ������Ӧ���SO2+H2O===H2SO3�����������ˮ��Һʹ��ɫʯ����Һ��죩
������������ˮ�γɵ�������ֻ�ܴ�������Һ�У����ܲ��ȶ������ֽ��ˮ�Ͷ������ʶ�����������ˮ�ķ�Ӧ�ǿ��淴Ӧ��SO2+H2O H2SO3
H2SO3
2���������ԣ�
SO2����ͨ�������ᣬ��Һ����ǣ��е���ɫ��������֡�
SO2��2H 2S===3S����2H 2O
3������ԭ�ԣ�SO2ʹ��ˮ���������Һ��ɫ
SO2��Br2��2H 2O=== H2SO4��2HBr
5SO2+2KMnO4+2H2O===K2SO4+2MnSO4+2H2SO4
 2SO2��O2 2 SO3
2SO2��O2 2 SO3
��SO3+H2O===H2SO4��SO3����ɫ����SO3��һ����ɫ���壬�۵���16.80C���е�Ҳֻ��44.8�棬������ˮ������ˮʱ�ų��������ȡ���
4����Ư���ԣ�SO2ʹƷ����Һ��ɫ�����ڶ�������ɸ�ijЩ��ɫ���ʻ��ϳ���ɫ���ʣ������ϳɵ���ɫ����ȴ�Dz��ȶ��ģ��ֽ���ָ�ԭ����ɫ���ʵ���ɫ��
Ư���ԵıȽ�

��Cl2��SO2�������Ư�ף��ܷ���ǿƯ��Ч����Ϊʲô��
���𰸡����ܣ�SO2��Cl2��2H2O=== H2SO4��2HCl
SO2��CO2�������
����SO2����ij��÷�������Ʒ����Һ�����ܷ�ʹ����ɫ����ʱ�����ټ��ȿ��ܷ��ٸ�ԭ��
����CO2����ij��÷������ó���ʯ��ˮ�����ܷ�ʹ�����ǣ�����ʱ�ٱ���塣
������CO2ʱ������Ӱ��SO2�ļ���
������SO2ʱ�����CO2�ļ���Ӧ�ȳ�ȥSO2�����ó���ʯ��ˮ����CO2���塣
��ȥCO2�е�SO2�����÷�����ʹ���������ͨ��������ˮ������KMnO4��Һ��NaHCO3��Һ(����SO2)����ͨ��Ʒ����Һ(����SO2�Ƿ���)��
5���Ʒ�
1��.��ҵ�Ʒ�
a�����ȼ�շ� S+O2 SO2
SO2
b������������4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
2��.ʵ�����Ʒ�
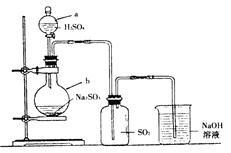 Na2SO3������H2SO4��Ũ)===Na2SO4��SO2����H2O
Na2SO3������H2SO4��Ũ)===Na2SO4��SO2����H2O
ʵ���г�ʹ�����ʵ���������Ϊ60%���ҵ����ᣬҲ����Ũ���ᡣ
�����ú�ϡ�����ᣬ��ΪSO2��ˮ�е��ܽ�Ƚϴ��³�ѹ��1���ˮ���ܽ�40�����SO2
6�������������Ⱦ��pHС��5.6����ˮ����֮Ϊ���ꡣ
6. Ũ����
��1���������ʣ���ɫ��״Һ�壬������Ũ������������Ϊ98.3%���е�Ϊ338�棬�߷е��ѻӷ��ԡ�
��2����ѧ���ʣ��� ��ˮ�ԣ��������
������ʽ��
<1> ��ˮ����������ܣ�����ˮ���ҷ��ȡ�
<2> ����������ˮ��������Ϊ����������ܸ������⡢�廯�⡢�⻯�⡢������
<3> ��ᾧˮ���ﷴӦ��
ʵ�飺Ũ�����뵨����Ӧ���ɵ�����ɫ��Ϊ��ɫ˵��Ũ��������ˮ�ԡ�
�� ��ˮ�ԣ�̿����
<1> ��ˮ����Ũ��������ʣ�����ϡ��������ʣ���Ũ��������ˮ�ԡ�
<2> ��ˮ����Ũ����Ļ�ѧ���ԣ����ʱ�Ũ������ˮ�Ĺ����ǻ�ѧ�仯�Ĺ��̡���Ӧʱ��Ũ���ᰴˮ�������⡢��ԭ�����ı�Ϊ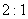 ��ȡ�л����е���ԭ�Ӻ���ԭ�ӡ�
��ȡ�л����е���ԭ�Ӻ���ԭ�ӡ�
<3> �ɱ�Ũ������ˮ������һ��Ϊ���⡢��Ԫ�ص��л���������ǡ�ľм��ֽм���������ʱ�����ˮ�������˺�ɫ��̿��̿������
�� ǿ������
ʵ��6��5��Ũ������ͭ��Ӧ����ͬѧע�ⷴӦ��������Ӧ������ڵ����ݡ�
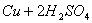 ��Ũ��
��Ũ��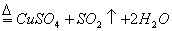
ǿ����������������ã���������������ã���
������Ũ����Ҳ��ľ̿��Ӧ��
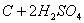
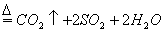
����������Ӧ��Ԫ�ػ��ϼ۵ı仯�����ָ���������ͻ�ԭ����
˼���������ʵ��֤��Ũ������̿��Ӧ�����ֲ������ʵ��װ��ͼ��
���ܣ��ۻ������й�Ӧ�ã��ֱ��Al��Fe��˵��ԭ��
�ڶ�ƪ������17����Ԫ��--����Ʒ���ϡ��߿���ѧ֪ʶ��ȫ�̽���
����17����Ԫ��
1����ϰ�ص�
1������Ԫ�ص��������ʺͻ�ѧ���ʵĵݱ���ɣ�
2�����ʡ��������������⡢��������������뻯ѧ���ʣ�
3���ص�����Ļ�ѧ���ʼ�����Ԫ�����ʵݱ���ɡ�
2���ѵ�۽�
��һ��������Ԫ�ص�ԭ�ӽṹ�����ʵĵݱ����

������������������
����������������ͬ�������壬�����г�����������ı���ɡ
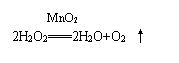
�������ⲻ�ȶ��ֽ⣬������������Ư����
����֪ʶ��ϵ
һ�����仯���������
��һ��������Ҫ���������ת����ϵ������ͼ��
ע�⣺
1��������������������Ե�����
��������õ��ӡ����������ԡ�����������
���������Ӧ����H+�������ԣ��������еģ�������������ԣ�����������ص㣩��������
2��������������ȷǽ����������ʵ�ѧϰ�����շǽ����������ʵ�һ�㷽��Ӧ�����м������������
�������ķ�Ӧ��������ķ�Ӧ���������ķ�Ӧ����ǽ����ķ�Ӧ����ˮ�ķ�Ӧ����������ķ�Ӧ�����ķ�Ӧ������ķ�Ӧ�����εķ�Ӧ�������л��ﷴӦ���ȡ�
3�����ջ��������ʵ�һ�㷽��Ӧ�����м������������
�ȶ��ԣ���ȼ�ԣ�����ԣ������Ժͻ�ԭ�ԣ������Եȡ�
3�����⾫��
����1����Щʵ����ʵ˵����Ԫ�صķǽ����Ա���Ԫ��ǿ������ԭ�ӽṹ֪ʶ���Խ��͡�
������Ŀǰ����ѧϰ�����ַǽ���Ԫ�أ�ͨ��±�塢����Ԫ�ص�ѧϰ�ɵó����Ƚ����ַǽ���Ԫ�صķǽ��������ǿ��һ��ɸ������¼������ʵ����ʵ���ٷǽ���������H2���ϵ������Լ��⻯����ȶ��Դ�С��������������Ӧˮ���������ǿ�����۷ǽ������ʼ���û���Ӧ��
�𰸣�����˵����Ԫ�طǽ����Ա���Ԫ��ǿ����Ҫʵ����ʵ�У���������������Ӧʱ���տɷ�����ը����Ӧ���ң����ʼ��ȱ�Ϊ�����ſ���H2���ϣ���H2S����HCl�ȶ�����H2SO4�����Բ���HClO4ǿ����H2S��Cl2��Ӧ���������ʣ�������Cl2��Ӧ����FeCl3������������Ӧ����FeS��
S��Cl��ԭ�ӵ��Ӳ�����ͬ����Clԭ�������������϶࣬��Clԭ�Ӱ뾶��Sԭ��С������������ԭ�Ӻ˵������ϴ���Ԫ�طǽ�����Ӧ����Ԫ��ǿ��
�������ṹ�������ʣ���������������ǰ��ѧ��֪ʶ����ָ��Ԫ�ػ�����֪ʶ��ѧϰ���Դ��������ԭ�ӽṹ��Ԫ��������֪ʶ�����⡣
����2��������(Se)�ı���Ʒ�ѽ����г�����֪��Ԫ������������ͬ�������������������й������������в���ȷ����
A.���������Ļ�ѧʽΪSeO3
B.����Se��һ�ְ뵼�����
C.ԭ�Ӱ뾶�������С
D.���ʵ������Ա�������������ǿ����O3��
�������������Ĺؼ����ڸ����Se��O��S��Cl��Br��Ԫ����Ԫ�����ڱ��е����λ�ù�ϵ��Se���ʺͳ������������ʡ���Se����Ϊ�뵼����ϣ������Ǻ�ǿ���������ȡ�����Ԫ�������ɵ�֪ʶ���ж�ѡ�������Կ�ס�
Seλ��Ԫ�����ڱ��ĵڢ�A�壬�����Ϊ6�����ӣ������Ϊ+6�ۣ���ͼ�Ϊ��2�ۣ����������������ʽΪSeO3��������Seԭ�Ӱ뾶��Sԭ�ӵĴ����ֲ��ֽ������ʡ�������Ϊ�뵼����ϡ����ѡ��A��B����ȷ��
����O��S��Cl��Br��Se��Ԫ�����ڱ��е����λ�ù�ϵ������Ԫ�������ɵ�֪ʶ�����жϳ�ԭ�Ӱ뾶��С��ϵΪ��Se��S��Se��Br�����ʵ������ԵĹ�ϵΪO3��O2��S��Se��Cl2��Br2��Se����˿��ж�C��D��ѡ���еIJ����жϴ��ڴ���
�𰸣�CD

 ��������ѧϰԪ�ػ�����֪ʶʱ��Ӧ�����ýṹ ���� ��;֮������ϵ�����ͬ���д�����Ԫ�أ�ץסͬ���ڡ�ͬ����Ԫ�����ʵĵݱ���������������δ֪�Ļ�̫��Ϥ��Ԫ�ػ�������ʣ���ѧϰԪ�ػ�����֪ʶ����������ϢǨ����ij���˼ά������
��������ѧϰԪ�ػ�����֪ʶʱ��Ӧ�����ýṹ ���� ��;֮������ϵ�����ͬ���д�����Ԫ�أ�ץסͬ���ڡ�ͬ����Ԫ�����ʵĵݱ���������������δ֪�Ļ�̫��Ϥ��Ԫ�ػ�������ʣ���ѧϰԪ�ػ�����֪ʶ����������ϢǨ����ij���˼ά������
����3��0.1 molij���ʸ����������ַ�Ӧ����������1.6 g����������ֵ��ʵ�Ԫ����
A.�� B.ͭ C.�� D.��
��������ַ�Ӧ���������ӵ�1.6 g��Ϊ�μӷ�Ӧ�������������n(S)��
 ��˵����n(����)��n(S)��0.1 mol��0.05 mol=2��1�������ĸ�ѡ����ϸ÷�Ӧ���ʵ���֮��(2��1)�ģ�ֻ��Cu��K��2Cu+S
��˵����n(����)��n(S)��0.1 mol��0.05 mol=2��1�������ĸ�ѡ����ϸ÷�Ӧ���ʵ���֮��(2��1)�ģ�ֻ��Cu��K��2Cu+S Cu2S��2K��S
Cu2S��2K��S K2S��
K2S��
�𰸣�BD
�����������漰��S���ʵ������ԣ��ǻ���֪ʶ������������������Խ���������һЩ��۽���ʱ������ͬѧ�������ղ���ͨ�����⣬������ѧ�����ո�֪ʶ�㣬ͬʱҲ������ѧ��˼ά�������Ժ������ԡ�������ͬѧ�Ƿ����Ͷ���������ѧ��ѧ��Ӧ������������
����4��1995��ŵ������ѧ�������������о������㱻�ƻ��������λ������ѧ�ң������еij�������˳������������ߣ����������ϵ����������(��CCl2F2�����ڹ�������·ֽ⣬����Clԭ�ӣ�Clԭ�ӻ�Գ�����������õ��ƻ�����(�����ķ���ʽΪO3)���йط�ӦΪ��

O3 O2��O Cl��O3====ClO��O2 ClO��O====Cl��O2
�ܷ�Ӧ��2O3====3O2
(1)������������������ķ�Ӧ�����У�Cl��
A.��Ӧ�� B.������ C.�м���� D.����
(2)O2��O3֮��Ĺ�ϵ�� ��
�������ش��1��ʱ��Ҫע��۲��ܷ�Ӧ���˷�Ӧ�ķ�Ӧ����O3����������O2����Ȼѡ��A��B�����������ų��������ڷ�Ӧ���в�����Ԫ�أ���ԭ����ȻҲ�������м������ѡ��C��ȻҲ���DZ���𰸡��������жϣ���ԭ��ֻ���Ǵ������Ӹ����ķ�Ӧ���̿����ڶ�����������Ӧ����ȷ����ʾ����ԭ���ڷ�Ӧǰ��������������������һ������
��ˣ���1��Ĵ���ѡ��D��
O3��O2���ǵ��ʣ����Ҷ�������Ԫ�ع��ɵĵ��ʣ�ֻ�����ǵķ�����ɲ���ͬ���ɴ˿ɼ���O3��O2���ڡ���ͬ��Ԫ�ع��ɵIJ�ͬ���ʡ���һ��������������Ӧ������������ͬ�������塣
�𰸣�(1)D (2)ͬ��������
������������������ϢǨ�����⡣��������1995��ŵ������ѧ��������о���Ŀ���������˷������ƻ�����������ķ�Ӧ������
��Ŀ��ȡ�Ľ��£������ǵ�ǰ������ѧ�б���ע�Ľ���֮һ�����ǣ����ʵ��龳ȴ���ѣ�ͨ����˼�����ͻ���ȷ�ش�
����5��(1994��ȫ��)���з�Ӧ������ʵ�����Ʊ���������
�ٸ�������ȷֽ�
2KMnO4 K2MnO4��MnO2��O2��
K2MnO4��MnO2��O2��
��������ȷֽ�
2NH4NO3 4H2O��2N2����O2��
4H2O��2N2����O2��
�۹���������ֽ�2H2O2 2H2O��O2��
2H2O��O2��
�ܶ��������ȷֽ�2NO2 2NO��O2
2NO��O2
A.ֻ�Т� B.�ٺ͢� C.�ٺ͢� D.�٢ۢ�
�������ڱ�����������4����Ӧ�У����˸�������ȷֽⷴӦ��������֪��ʵ�������������Ʒ�֮�⣬����������ֽ�Ҳ���Է��������ʵ�����Ʊ�������Ϊ�ˣ��ɽ�������������һֻ��ƿ�ڣ��ӷ�Һ©���е�������������������������������ÿ��Ƶ��ٵķ��������ڲ�����������������
����淋��ȷֽⲻ������ʵ������������һ������Ϊ�¶Ȳ�ͬ����立ֽ�IJ��ﲻͬ����ʹ��������Ŀ��ָ���ķ�Ӧ�����ɵ��ǵ����������Ļ�����壬���Է��룻ͬʱ�����������������ը�����ȱ���ɿ��İ�ȫ�ԡ�
NO2���ȷֽ�Ҳ��Ȼ��������ʵ�����Ʊ�������������Ϊ��Ӧ�ﲻ���ƣ���ʹ��Ӧʵ���ˣ���������Ҳ�����룬���������ڳ����»����ܻ�������������NO2��
�𰸣�C
������һ��˵�������ʵ�ʵ����(����������ѧ��ѧʵ������)�Ʒ���Ҫ�����������Ϊ����Ӧ�����ܿ�һЩ����Ӧ���������ܼ������Ƚ����У�����ʹ�Ʊ��IJ��ﵥһ���ڷ��룻���Է�Ӧ��ijɱ����ܺģ����Խ��ٿ��ǣ�������ʹ�ó��õ������豸�����Թܡ���ƿ���ձ��ȵȣ���Ӧ��Ϊ��ȫ��
����6������(O3)��һ���е�����ζ�ĵ���ɫ���壬�����б�������ǿ�������ԡ�������ʹʪ��ĵ��۵⻯����ֽ��������Ӧ�������������������Ӧ�Ļ�ѧ����ʽ�ǣ� �������Ӧ������������ ����ԭ������ ��
�������������Ϣ��֪����һ��ǣ���ɳ���(O3)��KI������������ԭ��Ӧ�����۵⻯����ֽ������˵���е���(I2)�����������л�ͬʱ��������(O2)���ɻ��ϼ۷���������������OԪ�ؼ�̬���䣬��ʵ�ʲ�û�вμ�������Ӧ����˿���֪���������õ�ʵ�����dz����еIJ�����ԭ�ӡ�����ԭ����ԭ������ˮ���ڵ������һ�����ΪOH������K����ɲ����е�KOH����˷�Ӧ�л�����H2O�μӷ�Ӧ���Ӷ�������⡣
�𰸣�����ʽ��O3��2KI��H2O====I2��O2��2KOH����������ⵥ��(I2������ԭ�����������(KOH)��
��������������Ϣ�ھ��⣬Ҫ�����ھ���������Ϣ��ץס������KI��ֽ��������һ����(��ʾ��I2��������)���������������ԭ�Ĺ�����������⡣
����7��(1999��㶫��25)�������A��D�ĸ��漰H2O2�ķ�Ӧ(δ��ƽ)����д�հ�
A.Na2O2��HCl����H2O2��NaCl
B.Ag2O��H2O2����Ag+O2��H2O
C��H2O2 H2O��O2
H2O��O2
D.H2O2��Cr2(SO4)3��KOH����K2CrO4��K2SO4��H2O
(1)H2O2�����������Եķ�Ӧ��(�����) ��
(2)H2O2�����������������ֻ�ԭ�Եķ�Ӧ��(�����) ��
(3)H2O2���������Եķ�Ӧ��(�����) ��������Ϊ ��
��������ӦA��һ����������ԭ��Ӧ��������Ϊ����֪��ǿ�ᣬ����Na2O2��Ӧ��������������õ�H2O2�����ա�ǿ����û����ᡱ�Ĺ��ɣ��ڴ˷�Ӧ��H2O2���ֳ���������ʡ�
��ӦB��Ag2O��ɵ��������ɼ�H2O2����һ�ֻ�ԭ�������е���Ԫ��Ӧ��������Ϊת����Ϊ�����������������е�ˮ������Ԫ�ؿ���Ϊ��������������
��������ķֽⷴӦC����һ������������ԭ��Ӧ��H2O2�ȱ����������ԣ��ֱ����˻�ԭ�ԡ�
�𰸣�(1)D (2)C
(3)A ��һ��Ӧ�ɿ�����ǿ����ȡ����ķ�Ӧ
�����������Թ�������Ϊ�زģ����鿼���й�������ԭ�Ļ���֪ʶ�Լ�˼ά�������ԣ�ͬʱ����Ծ�������ķ����ж�������
4��ʵս����
һ��ѡ���⪤
1.���Ϻ��߿��⣩��������ķе��ˮ�ߣ����������ֽ⡣ij�Լ������Ƶ�7%~8%�Ĺ���������Һ����Ũ����30%��Һʱ���ɲ��õ����˷�����
A.��ѹ���� B.��ѹ����
C.����ʯ�ҳ�ѹ���� D.��ѹ����
2.������������ȷ����
A.������������ɻ�����Na2Se��
B.������ˮ��Һ�����Ա�����������
C.��������Ա��������������
D.�������ڿ�������ȫȼ��ʱ�����ɶ���������ˮ
3.��Ԫ�ؼ��仯���ﲻ���ܾ��е�������
A.�ڵĻ��ϼ��У�2�ۡ���4�ۡ���6�۪�
B.�ڵ���������TeO2��TeO3��
C.����������ֱ�ӻ��ϣ���H2Te��H2Se�ȶ���
D.�����ڳ�����ɫ����ԭ�Ա���ǿ
4.�������ı���Ʒ�ѿ�ʼ�����г�����֪��Ԫ�����Ԫ��ͬ���ڣ������й���������������ȷ����
A.ԭ������Ϊ24��
B.��̬�⻯��ΪH2Se��
C.�ǽ����Ա�������
D.��ۺ�����ΪH2SeO4��
5.�����й��������ʵ�˵����ȷ���Ǫ�
A.��ʢ������������Ȼ������ɫ���ʪ�
B.�������ⲻ�ȶ������Ծ��õ�����������Ǫ�
C.�������ǿ��ԭ�ԣ����������ڷ�Ӧ��ֻ������ԭ����
D.�����������ᣬ��ͨ�����ֽⷴӦ��ȡǿ�᪤
6.���������м�����H2S��Ӧ����������ˮ��Ӧ���Ǫ�
A.FeSO4��Һ��
B.Na2S��Һ��
C.C��SO4��Һ��
D.��ˮ��
7.ͬ��ͬѹ�£�ȼ��20 mL H2S��ȥO2 16 ��L������ȼ�յ�H2S�벻���ȼ�յ�H2S������֮��Ϊ��
A.1��2 B.2��3
C.7��3 D.3��7��
8.����O3��˵���д�����Ǫ�
��O3���д̼��Գ�ζ����˱���Ϊ����������
��O2��O3����Ԫ�ص�ͬ�������媤
��O3��O2�ܶȴ�Ҳ��O2������ˮ��
��O3��O2�ȶ��������²��ֽ⪤
�ݳ�����Ư���������ê�
��������O3���Դ̼��������ӿ�ѪҺѭ������˿�����O3����Խ��Խ�ê�
�߿����и�ѹ�ŵ硢��ѹ�����ӡ������������O3���ɪ�
A���٢ڢ� B.�ܢݢު�
C.�ܢ� D.�ݢߪ�
9.������˵��Ԫ��Rһ��Ϊ����Ԫ�ص��Ǫ�
A.RΪ�ǽ���Ԫ�أ����������Ӧˮ�������ʽΪH2RO3��
B.R�ĵ�����H2���ϳ�H2R��
C.R�ĵ����������ϳ�Al2R3��
D.R���⻯���ˮ��Һ������
10.RΪ������Ԫ�أ���ԭ�������еĵ��Ӳ���Ϊ������������һ�룬�������γɵĺ������������
��R2O ��RO
��RO ��R2O
��R2O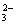 ��RO
��RO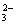 �������ж���ȷ���Ǫ�
�������ж���ȷ���Ǫ�
A.�����γɢ�ʱ���������γɢڢ۪�
B.�����γɢ�ʱ���������γɢۢܪ�
C.�����γɢ�ʱ���������γɢܪ�
D.�����γɢ�ʱ�������γɢ�
������ѡ���⣨��50�֣���
11.�������⣨H2O2������˫��ˮ��ҽ���Ͽ����������������
(1)���з�̪��NaOH��Һ�еμ�˫��ˮ����Һ�ɺ�ɫ������ɫ����Ҫԭ����˫��ˮ���� �ԡ���
(2)��˫��ˮ�����ữ�ĸ��������Һ�У���Һ�Ϻ�ɫ���ʣ���ʱ˫��ˮ���ֳ� �ԡ�
(3)���õ��ͻ�����ɫ����(��bSO4)�����ڣ���bS����˫��ˮ�������ָֻ�ԭò���йط�Ӧ�Ļ�ѧ����ʽΪ ��
12.(6��)����������Ļ������H2S ��K2S ��Al2S3 ��CuS ��FeS������(�����)��
(1)���������ֵ��ʻ��϶��ɣ�ֻ������Һ�����������ӷ�Ӧ�����ɵ��� ��
(2)ֻ�������ֵ��ʻ��϶��ɣ���������Һ�����������ӷ�Ӧ���ɵ��� ��
(3)���������ֵ��ʻ������ɣ���������Һ�����������ӷ�Ӧ���ɵ��� ��
13.(4��)��a ���������ֳ����ݣ���һ��������O2��Ӧ�Ƶ�SO2���ڶ���������������ϼ��ȣ��ٽ����ò���Ͷ��ϡH2SO4�У���H2S����SO2��H2S��ϣ��������a��3���磬���һ�ݵ�������
14.(1)��m �����ۺ�n������۾��Ȼ�ϣ����ܱ������м��ȵ����ȣ���ȴ�������ٺ���b��mol·L��1������Ͳ��ٲ�������?�����ѷų��������ռ��������ڱ�״���µ�������Ƕ�����?��
(2)����0.1 mol���ۺ�1.6 g��۾��Ȼ�Ϻ�����ʯ�������þƾ��Ƽ�����ȼ����ȫ��Ӧ����ȫ�����������ϡH2SO4�г�ַ�Ӧ���������������������ڱ�״������������2.24 L��������ԭ��
15.(6��)��֪�����ͬ�壬�������ƣ����û�ѧ����ʽ��������ʵ������
(1)CS2��Na2Sˮ��Һһ����ˮ��Һ����ɫ����ɫ ��
(2)��2S5����K2Sˮ��Һ�� ��
(3)Na2S2��Һ�м�ϡHCl����dz��ɫ���� ��
16.ij������Һ(������ΪNa��)�п��ܻ���SO ��S2����SO
��S2����SO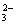 ��Cl����Br����NO
��Cl����Br����NO ��CO
��CO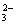 ��HCO
��HCO �е�һ�ֻ������֡���������ʵ�飨����ͼ��ʾ��(ÿ��ʵ�������Լ�������)��
�е�һ�ֻ������֡���������ʵ�飨����ͼ��ʾ��(ÿ��ʵ�������Լ�������)��
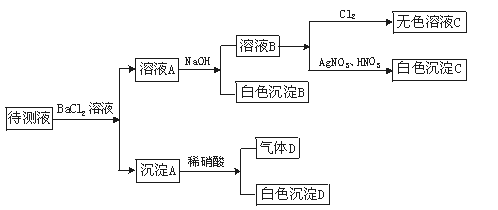
�ش��������⣺��
(1)����Һ�Ƿ���SO ��SO
��SO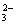 ?��
?��
(2)����B�Ļ�ѧʽΪ ��
(3)��������ʵ�飬����Һ�п϶�û�е������� ���϶����ڵ������� ��
17.(10��)ȡ�����Ƶ�����A��B������1 L��0��2��mol·L��1��������Һ�õ���ɫ����C����ҺD(��Һ�����Ϊ1 L����ͬ)�����˷��������C����ϴ�ӡ�������ڿ�����ȼ�գ������ɵ�1��3��������E������ҺD�ֵù�����C(��������ǰһ�εõ�����ͬ)����ҺF��F��������Ũ��Ϊ0��01��mol·L��1����F�м�A��B����������E����δ���й��������ɡ�
(1)A��B��C��E������?��
(2)��ҺD��F�и�����Щ����?���ǵ����ʵ���Ũ�ȸ�Ϊ����?��
(3)д���йط�Ӧ����ʽ��
�����
һ��1.������Һ̬���ʵķе���ѹǿ�йأ���Сѹǿ���ܽ�����е㣬�����������¶Ȳ���������ʹˮ������H2O2�ֲ���ֽ⡣��
�𰸣�B��
2.B 3.C 4.A 5.AB 6.B 7.D 8.C 9.BC 10.A��
����11.(1)���� (2)��ԭ��
(3)P��S��4H2O2===P��SO4��4H2O��
12.(1)�� (2)�ڢ� (3)�٢ݪ�
13.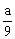 ��(H2S����)��
��(H2S����)�� ��(SO2����)��
��(SO2����)��
14.(1)250 m��7 b �̣�0��4 m�̪�
(2)�������۱�����Ϊ��������ᷴӦ���ٲ������壬�ʲ����������С��2.24 L����
15.(1)CS2��Na2S===Na2CS3��
(2)P2S5��K2S===2KPS3��
(3) Na2S2��2HCl===2NaCl��S����H2S��
16.(1)����SO ��SO
��SO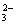 �е�һ�֣������ֶ��С�
�е�һ�֣������ֶ��С�
(2)BaCO3��
��3��Br����S2�� CO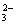 ��HCO
��HCO (��SO
(��SO ��SO
��SO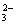 ����)
����)
17.(1)A��Na2S B��Na2SO3 C��S �ţ�SO2��
(2)D�У�NaCl 0������mol·����1��HCl��0������mol·����1��H2S��0��02��mol·����1
F�У�NaCl��0������mol·����1��HCl��0������mol·����1
(3)2Na2S��Na2SO3��6HCl===6NaCl��3S����3H2O��
2Na2S��4HCl===4NaCl+2H2S
S��O2 SO2��
SO2��
2H2S��SO2===3S����2H2O
