1.在常温下20 L密闭容器中通入a molH2、b molO2(a≤4,b≤4,a、b均为正整数),点燃后充分反应恢复到原温度时,容器中气体(水蒸气忽略不计)密度最大可能是 ( )
A 5.6 g/L B 9.6 g/L C 11.2 g/L D 56 g/L
2.同温同压下,某容器中充满O2重116 g,若充满CO2重122 g,现充满某气体重114 g,则某气体的相对分子质量为 ( )
A 28 B 60 C 32 D 44
3.只要知道下列哪一组物理量,就可以估算出气体分子间的平均距离?
(A)阿伏伽德罗常数、气体的摩尔质量和质量;
(B)阿伏伽德罗常数,气体的摩尔质量和体积;
(C)该气体的密度、体积和摩尔质量;
(D)阿伏伽德罗常数、该气体的摩尔质量和密度。
[解析]阿伏伽德罗常数是联系宏观世界和微观世界的桥梁,具有代表性的关系式有:设分子的质量为m,则M=NA·m;设物质的摩尔体积为V,则每个分子占有的体积为Vm=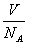 ,(此式对固体和液体可以近似理解为每个分子的体积,对气体可以理解为每个分子平均占有的空间体积)。另外,物质的密度
,(此式对固体和液体可以近似理解为每个分子的体积,对气体可以理解为每个分子平均占有的空间体积)。另外,物质的密度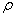 =M/V,利用这些关系式,再利用体积公式,就可对本题的各选项进行选择。
=M/V,利用这些关系式,再利用体积公式,就可对本题的各选项进行选择。
已知气体的摩尔质量和质量,可以求出物质的量,再知道阿伏伽德罗常数,只能求出分子总数。
已知阿伏伽德罗常数和气体的摩尔质量和体积,无法求得分子总数。
已知气体密度和体积及摩尔质量,只能求出摩尔数,不知阿伏伽德常数,无法求分子总数。
已知阿伏伽德罗常数及该气体的摩尔质量和密度,可以求出该气体的摩尔体积。
[答案]D。
4. 下列两种气体的分子数一定相等的是
A.质量相等、密度不等的N2和C2H4
B.等体积等密度的CO和C2H4
C.等温等体积的O2和N2
D.等压等体积的N2和CO2
5. 下列条件下两瓶气体所含原子数一定相等的是
A同质量、不同密度的N2和CO
B同体积、同密度的C2H4和C3H6
C同温度、同体积的H2和N2
D同压强、同体积的N2O和CO2
6.常温下,在某容积固定的密闭容器里分别充入两种气体各 ,在一定条件下充分反应后,恢复至原温度,容器内气体的压强降为开始时的1/4,则原混合气体可能是
,在一定条件下充分反应后,恢复至原温度,容器内气体的压强降为开始时的1/4,则原混合气体可能是
A. 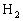 和
和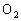 B.
B. 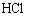 和
和 C.
C. 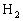 和
和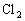 D.
D. 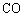 和
和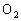
解析:V、T相同时,由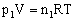 、
、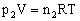 可推出:
可推出: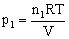 ,
,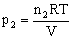 ,所以
,所以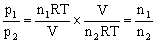 。即同温同体积条件下,气体的压强之比等于其物质的量之比。反应后气体的压强为反应前气体压强的1/4,说明反应后气体的总物质的量是反应前气体的总物质的量的1/4。常温下,
。即同温同体积条件下,气体的压强之比等于其物质的量之比。反应后气体的压强为反应前气体压强的1/4,说明反应后气体的总物质的量是反应前气体的总物质的量的1/4。常温下,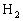 与
与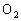 反应后生成的水为液态,剩余气体为未反应完的
反应后生成的水为液态,剩余气体为未反应完的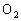 (
(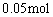 ),则反应后气体的总物质的量是反应前的
),则反应后气体的总物质的量是反应前的 ,故A项正确。在题给条件下,
,故A项正确。在题给条件下,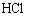 与
与 恰好完全反应,生成
恰好完全反应,生成 固态物质,气体的压强几乎为0,故B项错误。在题给条件下,
固态物质,气体的压强几乎为0,故B项错误。在题给条件下,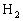 与
与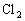 恰好完全反应,生成
恰好完全反应,生成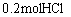 气体,反应前后气体的总物质的量不变,故C项错误。
气体,反应前后气体的总物质的量不变,故C项错误。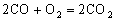 ,生成
,生成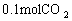 ,余下
,余下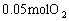 ,则反应后气体的总物质的量是反应前的
,则反应后气体的总物质的量是反应前的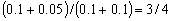 ,故D项错误。
,故D项错误。
答案:A
7.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是 ( B )
A.甲的分子数比乙的分子数多 B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小 D.甲的相对分子质量比乙的相对分子质量小
第二篇:阿伏伽德罗定律及其推论习题课11
阿伏伽德罗定律及其推论习题课
1.同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是
A.密度比为16:11 B.密度比为11:16
C.体积比为1:1 D.体积比为11:16
2.(全国高考题)根据阿伏加德罗定律判断,下列叙述中正确的是 ( )
A. 同温同压下两种气体的体积之比等于摩尔质量之比
B. 同温同压下两种气体的物质的量之比等于密度之比
C. 同温同压下两种气体的摩尔质量之比等于密度之比
D. 同温同体积下两种气体的物质的量之比等于压强之比
3.(广东)同温同压下两个容积相等的贮气瓶,一个装有C2H4,另一个装有C2H2和C2H6的混合气体,两瓶内的气体一定具有相同的( )
A、质量 B、原子总数
C、碳原子数 D、密度
4.同温同压下,4个容器中分别装有4种气体。已知各容器中的气体和容器的容积分别是:a.CO2,100ml; b. O2,200ml; c.N2,400ml; d.CH4,600ml。则4个容器中气体的质量由大到小的顺序是( )
A.a>b>c>d B.b>a>d>c
C. c>d>b>a D. d>c>a>b
5.SO3(气)、SO2、 O2(气)的质量比为40:32:8时,同温同压下它们的体积的整数比为( )
A.3:2:2 B.2:2:1 C、1:1:1 D、2:1:2
6.在一定温度下和压强下,1体积X2(气)跟3体积Y2(气)化合生成2体积气体化合物,则该化合物的分子式是( )
A.XY3 B.XY C.X3Y D.X2Y3
7.同温同压下,某集气瓶充满O2时为116g,充满CO2时为122g,充满气体A时为114g,则A 的式量为( )
A.60 B.32
C.44 D.28
8.在标准状况下,13g某气体的分子数与14gCO的分子数相等,此气体在标准状况下的密度为 ( )
A.1.25 g /L B. 2.32g/L
C.1.65g/L D.1.16g/L
9.同温同压下,16.5 g气体X 所占体积与12 g O2 的体积相同,则X 的相对分子质量是( )
A. 22 B. 28
C .44 D.88
10.等质量的下列各种气体,在相同温度,相同容积的密闭容器中,压强从大到小顺序正确的是 ( )
① Cl2 ② HCl ③ N2 ④ O2
A.①>②>③>④ B.①>②>④>③
C.③>④>②>① D.④>③>①>②
11.(上海 卷)下列两种气体的分子数一定相等的是( )
A.质量相等、密度不等的N2和C2H4
B.等温等密度的CO和C2H4
C.等温等体积的O2和N2
D.等压等体积的N2和CO2
12.现有CH4和O2两种气体,它们的相对分子质量之比为 ,若各取1g,则它们的物质的量依次是 、 ,它们的物质的量之比为 。由此可见, 当两种气体的质量相同时,它们的分子数和相对分子质量成 比。
13.若一定条件下,氢气的摩尔质量为M g/mol,密度为ρg/L,阿伏加德罗常数为NA,完成下列问题 :(1)该条件下,1L H2中所含氢气分子数为
(2)1g H2中所含氢气分子数为
(3)单个氢气分子的质量为
(4)该条件下,单个氢气分子占有的体积为
14.标准状况下CO2和CO的混合气体15g,体积为10.08L,则此混合气体中CO2和CO的物质的量各是多少?
15. 标准状况下,112 mL 某气体的质量为 0 . 14 g , 则其摩尔质量为? 相对分子质量为 ?
16.已知在标准状况时,N2和O2组成的混合气体中,二者的体积之比为4:1,试计算该混合气体的密度?
