一, 雷诺数Re(Reynolds number)表示作用于流体微团的惯性力与粘性力[1]之比。两个几何相似流场的雷诺数相等,则对应微团的惯性力与粘性力之比相等。
雷诺数较小时,黏滞力对流场的影响大于惯性力,流场中流速的扰动会因黏滞力而衰减,流体流动稳定,为层流;若雷诺数较大时,惯性力对流场的影响大于黏滞力,流体流动较不稳定,流速的微小变化容易发展、增强,形成紊乱、不规则的紊流流场。
雷诺数越小意味着粘性力影响越显著,越大则惯性力影响越显著。
二,荧光产生原理:
光致发光-物质分子吸收光能后,其电子由基态跃迁到激发态,激发态的分子以电磁辐射的形式释放能量回到基态,称为光致发光。
荧光-受光激发的分子从第一激发单重态的最低振动能级回到基态所发出的辐射。
磷光-受光激发的分子从第一激发三重态的最低振动能级回到基态所发出的辐射。
荧光光谱的主要参数和特征:
(1)量子产率:荧光量子产率也叫荧光效率或量子效率,它表示物质发射荧光的能力,通常用下式表示 发射荧光量子数 / 吸收光量子数
(2)荧光寿命:当某种物质被一束激光激发后,该物质的分子吸收能量后从基态跃迁到某一激发态上,再以辐射跃迁的形式发出荧光回到基态.当激发停止后,分子的荧光强度降到激发时最大强度的1/e所需的时间称为荧光寿命,它表示粒子在激发态存在的平均时间,通常称为激发态的荧光寿命。
(3)亮度:………
斯托克司(stokes)位移:斯托克司位移为最大荧光波长与最大激发波长之差
特征:(1)荧光淬灭:是指导致特定物质的荧光强度和寿命减少的所有现象。
(2)荧光漂白:photochemical destruction of a fluorophore, a phenomenon describing a fluorophore inability to be excited again after undergoing repetitive excitation and emission cycles.
(3)荧光闪烁:The phenomenon of random switching between ON (bright) and OFF (dark) states of the emitter under its continuous excitation.
主要荧光标记:
有机染料 荧光蛋白 量子点
三,单分子研究中常用显微术:(原理)
(1)激光共聚焦显微镜:Confocal 利用放置在光源后的照明针孔和放置在检测器前的探测针孔实现点照明和点探测,来自光源的光通过照明针孔发射出的光聚焦在样品焦平面的某个点上,该点所发射的荧光成像在探测针孔上,该点以外的任何发射光均被探测针孔阻挡。照明针孔与探测针孔对被照射点或被探测点来说是共轭的,因此被探测点即共焦点,被探测点所在的平面即共焦平面。计算机以像点的方式将被探测点显示在计算机屏幕上,为了产生一幅完整的图像,由光路中的扫描系统在样品焦平面上扫描,从而产生一幅完整的共焦图像。只要载物台沿着Z轴上下移动,将样品新的一个层面移动到共焦平面上,样品的新层面又成像在显示器上,随着Z轴的不断移动,就可得到样品不同层面连续的光切图像 。
(2)全内反射荧光显微镜TIRF:全内角反射荧光显微镜(total internal reflection fluorescence microscope,TIRFM),利用光线全反射后在介质另一面产生衰逝波的特性,激发荧光分子以观察荧光标定样品的极薄区域,观测的动态范围通常在200 nm以下。因为激发光呈指数衰减的特性,只有极靠近全反射面的样本区域会产生荧光反射,大大降低了背景光噪声干扰观测标的,能帮助研究者获得高质量的成像质量和可靠的观测数据。故此项技术广泛应用于细胞表面物质的动态观察。
光学原理:当一束光从光密介质进入光疏介质时,根据斯涅耳定律一部分光会发生折射,而一部分光会发生反射,当入射角度不断增大,折射角也会不断增大,当折射角刚好达到90度时,就发生了全反射现象。全反射发生后,折射光有一个临界状态沿着折射面传播,这部分光我们称之为隐失波,其能量在Z轴上呈现指数衰减。
(3)近场光学显微镜NSOM:根据非辐射场的探测与成像原理,能够突破普通光学显微镜所受到的衍射极限,采用亚波长尺度的探针在距离样品表面几个纳米的近场范围进行扫描成像的技术,在近场观测范围内,在样品上进行扫描而同时得到分辨率高于衍射极限的形貌像和光学像的显微镜。近场光学显微镜适用于超高光学分辨率下进行纳米尺度光学成像与纳米尺度光谱研究。传统光学显微镜的分辨率受到光学衍射极限影响,分辨率不超过该波长尺度范围。与传统光学显微镜不同的是,近场光学显微镜利用亚波长尺度探针,可以得到更小分辨率。
使用由熔拉或腐蚀光纤波导所制成之探针,在外表镀上金属薄膜已形成末端具有15nm至100nm直径尺寸之光学孔径(optical aperture) 的近场光学探针,再以可作精密位移与扫描探测之压电陶瓷材料(piezo-electrcal ceramics) 配合原子力显微技术(atomic force microscopy, AFM) 所提供精确的高度回馈控制,将近场光学探针非常精确地(垂直与水平于样品表面的方向之空间解析度可分别达到约0.1nm 与1nm) 控制在被测样品表面上1nm 至100nm 的高度,进行三维空间可回馈控制的近场扫描(scanning),而具有奈米光学孔径之光纤探针即可做接收或发射光学讯息之用,由此获得一真实空间之三维近场光学影像,因其与样品表面距离远小于一般光波波长,测得的信息皆属近场光学作用的信息,无平常常见的远场光学中绕射极限的光学解析度限制。
四,单分子荧光共振能量转移smFRET:
原理:荧光共振能量转移是指在两个不同的荧光基团中,如果一个荧光基团(供体 Donor)的发射光谱与另一个基团(受体 Acceptor)的吸收光谱有一定的重叠,当这两个荧光基团间的距离合适时(一般小于100Å),就可观察到荧光能量由供体向受体转移的现象,即以前一种基团的激发波长激发时,可观察到后一个基团发射的荧光。简单地说,就是在供体基团的激发状态下由一对偶极子介导的能量从供体向受体转移的过程,此过程没有光子的参与,所以是非辐射的,供体分子被激发后,当受体分子与供体分子相距一定距离,且供体和受体的基态及第一电子激发态两者的振动能级间的能量差相互适应时,处于激发态的供体将把一部分或全部能量转移给受体,使受体被激发,在整个能量转移过程中,不涉及光子的发射和重新吸收。如果受体荧光量子产率为零,则发生能量转移荧光熄灭;如果受体也是一种荧光发射体,则呈现出受体的荧光,并造成次级荧光光谱的红移。
产生条件: 供体和受体都能发光
供体的发射谱和受体的激发谱必须有部分重叠
供体和受体的距离必须小于100Å
供体和受体的取向状态合适
对荧光标记要求: 光稳定,足够亮,对标记分子影响小…
供体发射谱和受体吸收谱有一定重叠
供体发射谱和受体发射谱尽可能分开
供体和受体的量子产率相当
准备过程:标记荧光分子
表面固定
数据分析
五,smFRET应用和技术进展:
应用:? structure, dynamics, and mechanism of nucleic acids
? protein–nucleic acid interaction
? protein-protein interaction
? molecular motors
? protein-folding
?Translation, DNA processing, homologous recombination, transcription regulation,nucleosome dynamics, membrane fusion
技术进展:smFRET in Living Cells
smFRET Methods Based on Alternating Laser Excitation (ALEX)
Multiple FRET Pair Methods
Combinations of smFRET with Other Single-Molecule Methods
六,荧光相关光谱FCS:
原理:荧光相关光谱技术是一种利用荧光强度随时间的涨落进行分析检测的荧光光谱技术。某一物质的荧光强度与其浓度成正比。同样,在开放微区内平衡时记录的荧光信号强度也与其中的荧光分子数成正比。由于荧光分子的扩散( 或由于化学反应)导致进入或离开微区的分子数目总是在其平衡值处发生变化,因而导致荧光信号强度F(t)也不断变化( 即产生荧光的涨落现象),它是时间的函数。
(是一种统计小样本中荧光分子的荧光强度波动的相关分析方法,在这种方法 的经典模式中,样本体积被聚焦激光束和共焦小孔所限定,样本发出的荧光被高数值孔径的显微镜物 镜所收集,然后被灵敏的单光子计数器所监测,被探测到的荧光是随时间波动的,且这些时间函数是自相关的,归一化的荧光波动自相关函数提供了两类信息,函数的大小反比于所观测的荧光分子的平均数量,时间衰退的速率和形态反映了所观测的荧光分子的动力学特征)
自相关函数:The physical meaning of the autocorrelation is that it is directly proportional to the probability of detecting a photon at time τif there was a photon detection event at time zero.
(1) The temporal decay of the correlation, that is, the temporal decay of G(τ) with increasing lag-time τ, will be proportional to the diffusion speed of the molecule: the larger the diffusion coefficient, the faster are the fluorescence correlation decays.
(2) second important property of (ACF) is its dependence on the concentration of fluorescing molecules. There is a direct connection between the inverse concentration of fluorescing molecules and the amplitude of the ACF.
荧光交叉相关光谱FCCS:………
Scanning FCS:………
衍射极限(diffraction resolution limit)
因为一般光学系统的口径都是圆形,这样每个物点的像就是一个弥散斑,两个弥散斑靠近后就不好区分,这样就限制了系统的分辨率,这个斑越大,分辨率越低。这个限制是物理光学的限制,是光的衍射造成的。 分辨率最高只能到光波长的一半。
衍射极限公式是sinθ=1.22λ/D。其中θ是角分辨率,λ是波长,D是光圈直径。
突破衍射极限的方法
1, 基于软件的解决方法 FIONA STORM PAML
2, 基于硬件的解决办法 STED SSIM
超高分辨成像
PSF的平均标准误
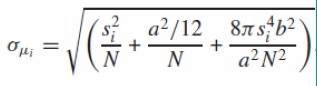
第一项, 光子数误差
第二项, 像素尺寸误差
第三项, 背景误差
一,FIONA(单纳米精度荧光成像)
1.原理:在一秒内一个荧光发色团收集10000个光子,凭借大量的光子数据,根据PSF(点函数)计算,像素可以精确到2.8±1.4nm
2.精度:2.8±1.4nm
3.应用举例:肌球(myosin)蛋白步行模型
二,SHRImP(单分子光漂白高分辨成像)
原理:原本两个荧光团定位,其中一个漂白后,利用两种图像对比可以精确定位
三,SHREC(单分子高分辨率荧光共定位)
原理:用不同的荧光分子(通常为2个)作为探针,共同标记同一部位,交叠成像,经行定位。
举例:myosin V的步行
双链DNA长度的测量
分子的取向:分子取向力发生在极性分子与极性分子之间。由于极性分子的电性分布不均匀,一端带正电,一端带负电,形成偶极。因此,当两个极性分子相互接近时,由于它们偶极的同极相斥,异极相吸,两个分子必将发生相对转动。这种偶极子的互相转动,就使偶极子的相反的极相对,叫做“取向”。
1,DOPI(散焦定位成像)
原理:成像CCD不汇聚光线至焦点,这样发光的样本成像就会呈现出散焦的斑块,光斑包含着取向信息。精度与所收集的光子数相关。
举例:肌球蛋白V的角度信息
2.PolTIRFM(偏振全内发射荧光显微镜)
原理:当有偏振光打入时,荧光分子会优先吸收与其取向平行的光,产生荧光,获取坐标数后计算,可以获得荧光分子取向信息。
举例:myosin VI
四,STORM(随机光学重构显微镜)
原理:随机光学重建显微镜(STORM)是一种高级的光学显微术,通过这一技术能够表现组织或细胞更加细微的结构。之前广泛应用于生物医学领域的光学显微技术由于受到衍射极限的限制,分辨率通常为几百个纳米左右。这要比细胞内典型的分子结构大,这样很多生物学的研究都无法用光学显微镜实现。而STORM采用光转换荧光探针,在时间上分离相互重叠发光的荧光分子,然后重构得到高分辨率图像..利用激活子-报告子形成光开关,再随机照射成像,如此循环,得到一组荧光图像,最后把所成像叠加。
分辨率:20nm横向,50nm轴向
举例:神经细胞的观察
五,PAML(光激活定位显微技术)
原理:依赖于一系列的光激活荧光蛋白,荧光蛋白再依次漂白,获得搞精度成像
精度:10nm
基于硬件
一, STED(受体发射损耗显微术)
原理:能量由基态到激发态会吸收光子,从激发态回到基态时会释放光子,两种光子的波长,极性,取向相同,根据捕捉到的光子成像。激发光和衰减光的重叠决定了分辨率。
精度:6nm-20nm
举例:神经细胞树突
二, SSIM(饱和结构照明显微术)
原理:通过衍射光栅将激发光分成两束到达样本,出现正弦曲线图案,激发光在顶点激发荧光,在零点不激发从而产生暗视野。大量的成像是通过扫描和转动转盘实现的,可以突破衍射极限。
精度:50nm
原子力显微镜原理AFM:将探针装在一弹性微悬臂的一端,微悬臂的另一端固定,当探针在样品表面扫描时,探针与样品表面原子间的作用力会使得微悬臂轻微变形,这样,微悬臂的轻微变形就可以作为探针和样品间作用力的直接量度。一束激光经微悬臂的背面反射到光电检测器,可以精确测量微悬臂的微小变形,实现了通过检测样品与探针之间的原子间作用力来反映样品表面形貌和结构。
AFM测量对样品无特殊要求,用来研究包括绝缘体在内的固体材料表面结构。从而弥补了扫描隧道显微镜的不足。与STM最大的差别在于并非利用电子隧穿效应,而是检测原子之间的接触,原子键合,范德华力等来呈现样品的表面特性。
接触模式:在整个扫描成像过程之中,探针针尖始终与样品表面保持紧密的接触, 相互作用力是排斥力。悬臂施加在针尖上的力有可能破坏试样的表面结构。若样品表面柔嫩而不能承受这样的力,便不宜选用接触模式对样品表面进行成像。
非接触模式:悬臂在距离试样表面上方5~10 nm 的距离处振荡。样品与针尖之间的相互作用由范德华力控制,样品不会被破坏,而且针尖也不会被污染,特别适合于研究柔嫩物体的表面。这种操作模式的不利之处在于要在室温大气环境下实现这种模式十分困难。因为样品表面不可避免地会积聚薄薄的一层水,它会在样品与针尖之间搭起一小小的毛细桥,将针尖与表面吸在一起,从而增加尖端对表面的压力。
敲击模式:介于接触模式和非接触模式之间,是一个杂化的概念。悬臂在试样表面上方以其共振频率振荡,针尖仅仅是周期性地短暂地接触/ 敲击样品表面。当检测柔嫩的样品时,敲击模式是最好的选择之一。
一旦AFM开始对样品进行成像扫描,装置随即将有关数据输入系统,如表面粗糙度、平均高度、峰谷峰顶之间的最大距离等,用于物体表面分析。同时,AFM 还可以完成力的测量工作,测量悬臂的弯曲程度来确定针尖与样品之间的作用力大小。
单分子力谱:基于AFM等技术的的单分子力谱是研究高分子体系中的分子内与分子间相互作用,进而揭示起超分子结构的本质及动态过程的一种新型纳米表征技术。
力-伸展曲线(FEC):首先吸附高分子样品的基片随着压电陶瓷管的运到而与针尖逼近。在样品表面开始逼近微悬臂而并没有接触到针尖的过程中,如果悬臂每一天受到吸引或排斥力,微悬臂处于一种松弛状态,光学检测信号为零。压电陶瓷管的扫描信号被记录下来,形成扫描基线。如图A。当针尖接近样品表面时,针尖与基底之间的排斥力使得悬臂发生偏转如图B(这种由排斥力引发的偏转为负向偏转),从力谱仪上获得的光电信号经过转换后,就可以得到一条力—伸展曲线。当针尖与样品分离时,连到针尖与基片之间的高分子链会被拉伸,而这种针尖与样品的相互作用会引起悬臂弯曲,此时悬臂为正向偏转,表现为吸引力。导致力曲线上拉伸信号产生的这一区域能够给出关于单链弹性性质的丰富信息,因此成为数据分析过程中的重点研究对象。如图C。最后,当高分子受到进一步拉伸后,这种介于针尖和基底之间的桥连结构中较为薄弱的部分会发生脱落,使悬臂迅速复原,表现为力曲线上的力值迅速掉回零点。
光阱:一种通过高度聚焦激光束产生力(量级通常为皮牛顿级)移动微小透明物体的装置。用于移动细胞或病毒颗粒,把细胞捏成各种形状,或者冷却原子。光是一种特殊的物质,携带有能量和动量,光与物质相互作用时彼此交换能量和动量,产生各种效应。 光与物质间可以交换动量,使受光照射的物体受到一个力或力矩,也即产生光的力学效应。由于通常光源发出的光产生的力学效应太微弱,这一效应在激光发明之后才引起人们的关注,并取得了突破性进展。基本原理:高度聚焦激光束通常是通过使激光通过显微镜物镜得到的。聚焦后的激光光束最窄的部分(光束腰)会存在非常强的电场梯度。介电质颗粒会被吸引至电场梯度最高的区域,也就是光束的中心。同时,电场还会在光束传播方向上对颗粒产生力。这点可以通过动量守恒来理解。光束中的介电质颗粒会吸收并散射光子,于是就会产生相应的动量的变化。如果颗粒不在光束腰上,由于光场光强梯度的影响,颗粒各个方向上会受到不均匀的力将其拉向光强最强的区域。光镊是非常精确的设备,可以将亚微米级的颗粒移动亚纳米级的距离。所以,光镊常常被用于研究和操作DNA,蛋白质,酶甚至是单个分子。在定量科学测量中,通常电介质颗粒都会不移动到离光束中心很远的地方。
Scattering force:位于光传播方向上,大多数情况下所受的力
Gradient force:位于光密度梯度上,如果光有很大的亮度剃度时比较明显
当颗粒与光束中心的距离很小时,颗粒受到的力与颗粒与光束中心的距离成正比。因此,其特性类似于普通的弹簧系统,遵守胡克定律.
磁阱:用电磁场形成的一种“势能坑”原子可以被收集在坑内存起来。一种原子阱叫“磁阱”,它利用两个平行的电流方向相反的线圈构成。这种阱中心的磁场为零,向四周磁场不断增强。陷在阱中的原子具有磁矩,在中心时势能最低。偏离中心时就会受到不均匀磁场的作用力而返回。这种阱曾捕获1012个原子,捕陷时间长达12min。
FISH荧光原位杂交:将DNA(或RNA)探针用特殊的核苷酸分子标记,然后将探针直接杂交到染色体或DNA纤维切片上,再用与荧光素分子偶联的单克隆抗体与探针分子特异性结合来检测DNA序列在染色体或DNA纤维切片上的定性、定位、相对定量分析.
FRAP荧光漂白恢复:用荧光素标记膜蛋白或膜脂,然后用激光束照射细胞表面某一区域,使被照射区的荧光淬灭变暗。由于膜的流动性,淬灭区域的亮度逐渐增加,最后恢复到与周围的荧光强度相等。根据荧光恢复的速度可推算出膜蛋白或膜脂扩散速度。
FLIP荧光漂白消失:有些荧光恢复的速度非常快,荧光漂白与恢复几乎同时发生,所以FRAP实验无法实现这些快速变化标本的动力学研究。FLIP与FRAP类似,同样在细胞上选取局部刺激区域,用强激光反复刺激,不同之处是FRAP记录的是被漂白区域的荧光恢复过程,而FLIP记录的是未被漂白区域的荧光损失过程,该技术为检查内质网、细胞核和细胞质等区室的边界提供了强有力的工具。
FLIM荧光寿命成像:荧光寿命是指分子受到光脉冲激发后返回基态之前在激发态平均停留的时间,处于激发态的荧光分子在退激发到基态的过程中发射荧光释放能量,激发态荧光团荧光强度的衰减用数学式表达为单指数函数。荧光寿命取决于荧光分子所处的微环境,通过对样品荧光寿命的测量和成像可以定量获取样品的功能信息。以往荧光分析或成像技术大多基于荧光强度的测量,容易受激发光强度、样品猝灭和荧光染料的分布浓度等许多因素的影响,因此难以做到定量测量,而FLIM的测量一般来说是绝对的,不受激发光强度变化、荧光团的浓度和光漂白等因素的影响,且不受其他限制强度测量因素的制约,仅与荧光团所处的微环境密切相关,因此,通过对样品进行FLIM,可以对分子所处微环境中的许多生物物理、生物化学参数如PH值、离子浓度、氧压、溶液疏水性及猝灭剂(如碘化物、丙烯酰胺)等的分布,进行定量测量。应用:细胞内PH值和离子浓度成像,细胞过程的时间分辨成像,组织成像和临床应用,FRET+FLIM测定细胞内分子的相互作用
玻璃微针分析法?
基于流体力学分析法?
