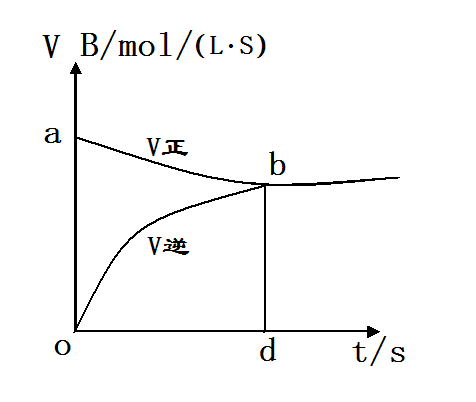
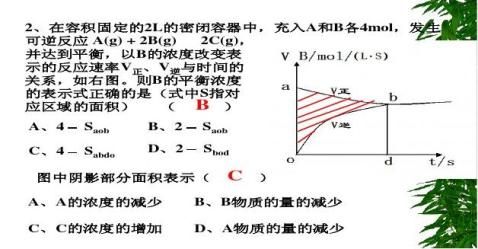
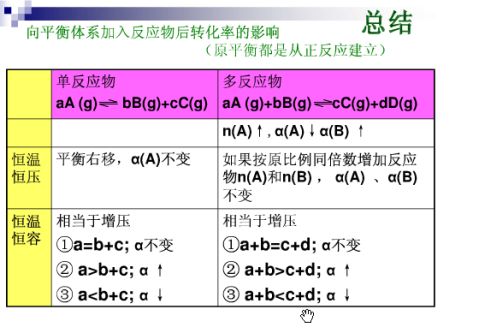
小结平衡转化率问题 平衡转化率=某反应物转化的物质的量(或物质的量浓度)?100% 该反应物的起始起始物质的量(或物质的量的浓度)
别要引导学生在审题过程中进行4个关注:一要关注容器是否可变,二要关注化学反应是否可逆,三要关注各物质的状态是否都为气体,四要关注反应两边气体体积是否相等,现将有关平衡转化率的问题小结如下:
一、多种反应物
1.可逆反应达到平衡后加其一。
这种情况不管状态如何均认为所加物本身转化率减小其它物质转化率增大 例1:正反应方向移动,,反应达到平衡后增大的转化率 ,而的浓度,则平衡向的转化率 。
3C(g)+2D(g)达到平衡后加入C逆向运用: 例2.反应: 在恒温恒容的容器中3A(g)+B(g)
则A的转化率
2、可逆反应达到平衡后按等比例加入各种反应物,分2种情况
(1)恒温恒压:由于恒温恒压时等比例扩大或缩小反应物的用用量均与原平衡等效,故转化率不变,各反应物和生成物的体积分数不变,各反应物和生成物物质量会跟原平衡相比,等比例增加,但浓度不变。
(2)恒温恒容:此时可以看成反应叠加后,增大压强使平衡向气体总系数小方向移动。
例3.
充入充入和和。在密闭容器中按,反应达到平衡后,若其它条件不变,再按,反应重新达到平衡后,平衡转化率 和的比例的比例的平衡转化率 。
例4.
二、一种反应物
由于反应只有一种所以无论反应物加多少量都可视为等比例增加反应物的用量,故认为有两种情况: 。反应达到平衡后按比例增大反应物浓度,达到新的化学平衡时,各反应物的转化率均 。
1、恒温恒压:由于恒温恒压时等比例扩大或缩小反应物的用用量均与原平衡等效故转化率不变,各反应物和生成物的体积分数不变,各反应物和生成物物质量会跟原平衡相比,等比例增加,但浓度不变。
2、恒温恒容:此时可以看成反应叠加后,增大压强使平衡向气体总系数小方向移动移动。
例6.在恒温恒容下
入,反应达到平衡后,再向密闭容器中加,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均增大,颜色变深,
NO2转化率增大。
分析:该反应可认为后加入NO2与原反应进行叠加,叠加后气体总体积增加,为了
使体积维持不变,只能向体系加压从而引起叠加后的平衡向生成N2O4的方向移动。
逆向运用:
例7恒T恒V ,反应达到平衡后,再向密闭容器中加入N2O4,反应达到平衡时NO2、N2O4的物质的量(或物质的量浓度)均 ,颜色 ,
N2O4向NO2转化的转化率 。
例8.
反应达到平衡后,
再向密闭容器中加入,达到平衡后,PCl3的物质的量会 ,(填“增加”还是“减少”)但是反应达到新
的平衡时PCl5物质的量会 ,(填“增加”还是“减少”)的转化率 (填
“增大”还是“减小”), PCl5在平衡混合物中的百分含量较原平衡时 ,(填“增
加”还是“减少”)
例9.
反应达到平衡后,再向密闭容器中加入HI,HI的平衡转化率 。H2的物质的量 ,I2的物质的
量 。
例10.某温度下,在一容积可变的容器中,反应2A(g)+B(g)=2C(g)达到平衡时,A、B、C的物质的量分别为4mol、2mol、4mol。保持温度和压强不变,平衡后再向体系中加各物质按下列情况加入平衡怎样移动?
A.均加1mol, B.均减1mol
三、另类(平衡后充入惰性气体)
1. 恒温恒容条件下充入“惰性气体”,化学平衡不移动。因平衡体系的各组分浓度均未发生变化,故各反应物转化率不变。
2. 恒温恒压条件下充入“惰性气体”,化学平衡向气体体积增大的方向移动。因为此
时容器容积必然增大,相当于对反应体系减压,继而可判断指定物质的转化率变化。
小试身手
1、某恒温恒容的容器中,建立如下平衡:2NO2(g)=== N2O4(g),在相同条件下,若分别向容器中通入一定量的NO2气体或N2O4气体,重新达到平衡后,容器内N2O4的体积分数比原平衡时 ( )
A.都增大 B.都减小 C.前者增大后者减小 D.前者减小后者增大
2、例一定温度下,将amol PCl5通入一个容积不变的反应器中,达到如下平衡:PCl5(g) PCl3(g)+Cl2(g),测得平衡混合气体压强为p1,此时再向反应器中通入amol PCl5,在温度不变的条件下再度达到平衡,测得压强为p2,下列判断正确的是 ( )
A.2p1>p2 B.PCl5的转化率增大 C.2p1<p2 D.PCl3%(体积含量)减少
3、在一容积可变的密闭容器中,通入1molX和3molY,在一定条件下发生如下反应:X(g)+3Y(g) ==== 2Z(g),到达平衡后,Y的转化率为a%,然后再向容器中通入2molZ,保持在恒温恒压下反应,当达到新的平衡时,Y的转化率为b%。则a与b的关系是 ( )
A.a=b B.a>b C.a<b D.不能确定
4、两个体积相同的密闭容器A、B,在A中充入SO2和O2各1mol,在B中充入SO?2和O2各2 mol,加热到相同温度,有如下反应2SO2(g)+ O2(g) 2SO3(g),对此反应,
下述不正确的是 ( )
A.反应速率B>A B.SO2的转化率B>A
C.平衡时各组分含量B = A D.平衡时容器的压强B>A
5、一定量混合气体在密闭容器中发生如下反应:xA(气)+yB(气) nC(气),达到平衡后,测得A气体的浓度为0.5mol/L。保持温度不变将容器的容积扩大1倍,再达平衡时,测得A气体的浓度为0.3mol/L,则下列叙述中正确的是( )
A、x+y<n B、该化学平衡向右移动
C、B的转化率增大 D、C的体积分数减小
6、一定温度下,在一个体积可变的密闭容器中加入2 molH2和2 molN2,建立如下平衡: N2(g)+3H2(g) 2NH3(g)相同条件下,若向容器中再通入1 mol H2和,1 molN2又达到平衡.则下列说法正确的是 ( )
A.NH3的百分含量不变 B.N2的体积分数增大
C.N2的转化率增大 D.NH3的百分含量增大
7、某温度下的密闭容器中发生如下反应:2M(g)+N(g) 2E(g),若开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2 mol M和1 mol N的混合气体,则达平衡时M的转化率为 ( )
A.20% B.40% C.60% D.80%
第二篇:转化率与等效平衡

4、反应物转化率与浓度的关系
(1)对于多种物质参加的反应(气、液态)
m A (g)+n B (g)p C (g)+q D (g)反应达到平衡后,C A ↑,B的转化率可提高,但A的转化率一般降低;C B ↑,A的转化率可提高,但B 的转化率一般降低。
同时增加A、B的浓度,m +n >p +q A、B的转化率都增大。
m +n< p +q
m +n= p +q
同时增加A、B的浓度,A、B的转化率都减小。同时增加A、B的浓度,A、B的转化率都不变。
(2)对于分解反应,要视反应前后物质的化学计量
数而定。
m A(g)n B(g)+ p C(g)
m =n+p不论如何改变反应物的浓度,
反应物的转化率都不变。
例:2HI(g)H2 (g)+ I2(g)
m < n+p
m >n+p增加反应物的浓度时,反应物的转化率减小。
例:2NH3(g

)N2(g)+ 3H2(g)
六、等效平衡问题及解题思路
1、等效平衡的含义
在一定条件(定温、定容或定温、定压)
下,只是起始加入情况不同的同一可逆反应达到平衡后,任何相同组分的分数(体积、物
质的量)均相同,这样的化学平衡互称等效平衡。
2、等效平衡的分类
⑴、定温、定容条件下的等效平衡
I 类:对于一般可逆反应,在定T、V条件下,改变起始加入情况,只要按可逆反应的化学计量数比换算成平衡式左右两边同一边物质的量与原平衡起始量相同,则两平衡等效。