高中化学必修2知识点归纳总结
第一章 原子核外电子排布与元素周期律
一、原子结构
 质子(Z个)
质子(Z个)
 原子核 注意:
原子核 注意:
中子(N个) 质量数(A)=质子数(Z)+中子数(N)
 1.原子数
A X 原子序数=核电荷数=质子数=原子的核外电子
1.原子数
A X 原子序数=核电荷数=质子数=原子的核外电子
核外电子(Z个)
★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层: 一(能量最低) 二 三 四 五 六 七
对应表示符号: K L M N O P Q
3.元素、核素、同位素
元素:具有相同核电荷数的同一类原子的总称。
核素:具有一定数目的质子和一定数目的中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说)
二、元素周期表
1.编排原则:
①按原子序数递增的顺序从左到右排列
②将电子层数相同的各元素从左到右排成一横行。(周期序数=原子的电子层数)
③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行。
主族序数=原子最外层电子数
2.结构特点:
核外电子层数 元素种类
 第一周期 1 2种元素
第一周期 1 2种元素
 短周期 第二周期 2 8种元素
短周期 第二周期 2 8种元素
 周期 第三周期 3 8种元素
周期 第三周期 3 8种元素
 元 (7个横行) 第四周期 4 18种元素
元 (7个横行) 第四周期 4 18种元素
素 (7个周期) 第五周期 5 18种元素
周 长周期 第六周期 6 32种元素
期 第七周期 7 未填满(已有26种元素)
 表 主族:ⅠA~ⅦA共7个主族
表 主族:ⅠA~ⅦA共7个主族
族 副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族
(18个纵行) 第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间
(16个族) 零族:稀有气体
三、元素周期律
1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。元素性质的周期性变化实质是元素原子核外电子排布的周期性变化的必然结果。
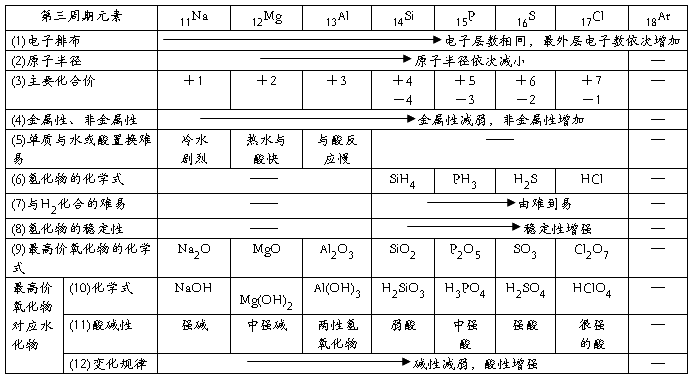
2.同周期元素性质递变规律
第ⅠA族碱金属元素:Li Na K Rb Cs Fr(Fr是金属性最强的元素,位于周期表左下方)
第ⅦA族卤族元素:F Cl Br I At (F是非金属性最强的元素,位于周期表右上方)
★判断元素金属性和非金属性强弱的方法:
(1)金属性强(弱)——①单质与水或酸反应生成氢气容易(难);②氢氧化物碱性强(弱);③相互置换反应(强制弱)Fe+CuSO4=FeSO4+Cu。
(2)非金属性强(弱)——①单质与氢气易(难)反应;②生成的氢化物稳定(不稳定);③最高价氧化物的水化物(含氧酸)酸性强(弱);④相互置换反应(强制弱)2NaBr+Cl2=2NaCl+Br2。
(Ⅰ)同周期比较:

(Ⅱ)同主族比较:

(Ⅲ)
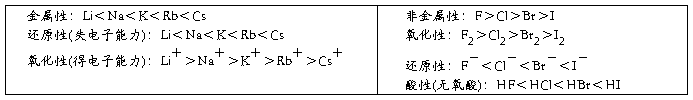
比较粒子(包括原子、离子)半径的方法(“三看”):(1)先比较电子层数,电子层数多的半径大。(2)电子层数相同时,再比较核电荷数,核电荷数多的半径反而小。
元素周期表的应用
1、元素周期表中共有个 7 周期, 3 是短周期, 3 是长周期。其中第 7 周期也被称为不完全周期。
2、在元素周期表中, ⅠA-ⅦA 是主族元素,主族和0族由短周期元素、 长周期元素 共同组成。 ⅠB -ⅦB 是副族元素,副族元素完全由长周期元素 构成。
3、元素所在的周期序数= 电子层数 ,主族元素所在的族序数= 最外层电子数,元素周期表是元素周期律的具体表现形式。在同一周期中,从左到右,随着核电荷数的递增,原子半径逐渐减小,原子核对核外电子的吸引能力逐渐增强,元素的金属性逐渐减弱,非金属性逐渐增强 。在同一主族中,从上到下,随着核电荷数的递增,原子半径逐渐增大 ,电子层数逐渐增多,原子核对外层电子的吸引能力逐渐 减弱 ,元素的金属性逐渐增强,非金属性逐渐 减弱 。
4、元素的结构决定了元素在周期表中的位置,元素在周期表中位置的反映了原子的结构和元素的性质特点。我们可以根据元素在周期表中的位置,推测元素的结构,预测 元素的性质 。元素周期表中位置相近的元素性质相似,人们可以借助元素周期表研究合成有特定性质的新物质。例如,在金属和非金属的分界线附近寻找 半导体 材料,在过渡元素中寻找各种优良的 催化剂 和耐高温、耐腐蚀材料。
化学键是直接相邻两个或多个原子或离子间强烈的相互作用。
1.离子键与共价键的比较
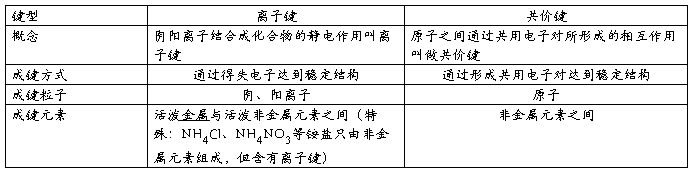
离子化合物:由离子键构成的化合物叫做离子化合物。(一定有离子键,可能有共价键)
共价化合物:原子间通过共用电子对形成分子的化合物叫做共价化合物。(只有共价键一定没有离子键)
 极性共价键(简称极性键):由不同种原子形成,A-B型,如,H-Cl。
极性共价键(简称极性键):由不同种原子形成,A-B型,如,H-Cl。
共价键
非极性共价键(简称非极性键):由同种原子形成,A-A型,如,Cl-Cl。
2.电子式:
用电子式表示离子键形成的物质的结构与表示共价键形成的物质的结构的不同点:(1)电荷:用电子式表示离子键形成的物质的结构需标出阳离子和阴离子的电荷;而表示共价键形成的物质的结构不能标电荷。(2)[ ](方括号):离子键形成的物质中的阴离子需用方括号括起来,而共价键形成的物质中不能用方括号。
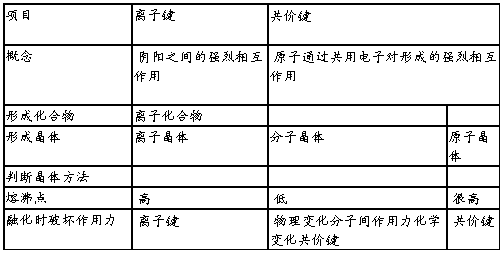
3、分子间作用力定义把分子聚集在一起的作用力。由分子构成的物质,分子间作用力是影响物质的熔沸点和 溶解性 的重要因素之一。
4、水具有特殊的物理性质是由于水分子中存在一种被称为氢键的分子间作用力。水分子间的 氢键 ,是一个水分子中的氢原子与另一个水分子中的氧原子间所形成的分子间作用力,这种作用力使得水分子间作用力增加,因此水具有较高的 熔沸点。其他一些能形成氢键的分子有 HF H2O NH3 。
第二篇:高中化学必修二第一章知识点和习题(含答案)
第一章 物质结构 元素周期律
一、原子结构
 质子(Z个)
质子(Z个)
 原子核 注意:
原子核 注意:
中子(N个) 质量数(A)=质子数(Z)+中子数(N)
 1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
1.原子(
A X ) 原子序数=核电荷数=质子数=原子的核外电子数
核外电子(Z个)
★熟背前20号元素,熟悉1~20号元素原子核外电子的排布:
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层: 一(能量最低) 二 三 四 五 六 七
对应表示符号: K L M N O P Q
3.元素、核素、同位素
元素:具有相同核电荷数的同一类原子的总称。
核素:具有一定数目的质子和一定数目的中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素。(对于原子来说)
二、元素周期表
1.编排原则:
①按原子序数递增的顺序从左到右排列
②将电子层数相同的各元素从左到右排成一横行。(周期序数=原子的电子层数)
③把最外层电子数相同的元素按电子层数递增的顺序从上到下排成一纵行。
主族序数=原子最外层电子数
2.结构特点:
核外电子层数 元素种类
 第一周期 1 2种元素
第一周期 1 2种元素
 短周期 第二周期 2 8种元素
短周期 第二周期 2 8种元素
 周期 第三周期 3 8种元素
周期 第三周期 3 8种元素
 元 (7个横行) 第四周期 4 18种元素
元 (7个横行) 第四周期 4 18种元素
素 (7个周期) 第五周期 5 18种元素
周 长周期 第六周期 6 32种元素
期 第七周期 7 未填满(已有26种元素)
 表 主族:ⅠA~ⅦA共7个主族
表 主族:ⅠA~ⅦA共7个主族
族 副族:ⅢB~ⅦB、ⅠB~ⅡB,共7个副族
(18个纵行) 第Ⅷ族:三个纵行,位于ⅦB和ⅠB之间
(16个族) 零族:稀有气体
三、元素周期律
1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。元素性质的周期性变化实质是元素原子核外电子排布的周期性变化的必然结果。
2.同周期元素性质递变规律
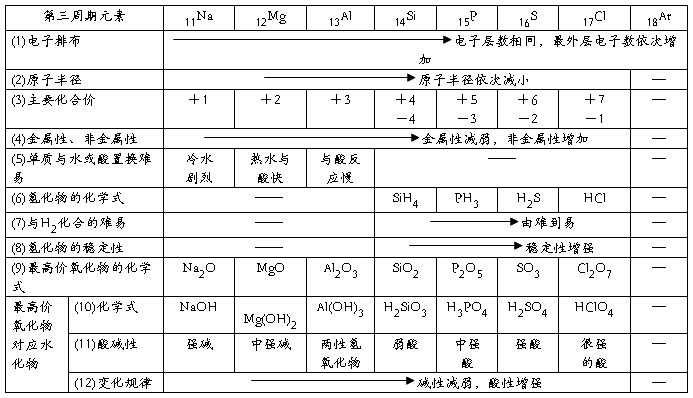
第ⅠA族碱金属元素:Li Na K Rb Cs Fr (Fr是金属性最强的元素,位于周期表左下方)
第ⅦA族卤族元素:F Cl Br I At (F是非金属性最强的元素,位于周期表右上方)
★判断元素金属性和非金属性强弱的方法:
(1)金属性强(弱)——①单质与水或酸反应生成氢气容易(难);②氢氧化物碱性强(弱);③相互置换反应(强制弱)Fe+CuSO4=FeSO4+Cu。
(2)非金属性强(弱)——①单质与氢气易(难)反应;②生成的氢化物稳定(不稳定);③最高价氧化物的水化物(含氧酸)酸性强(弱);④相互置换反应(强制弱)2NaBr+Cl2=2NaCl+Br2。
(Ⅰ)同周期比较:

(Ⅱ)同主族比较:

(Ⅲ)
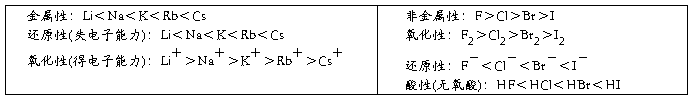
比较粒子(包括原子、离子)半径的方法:(1)先比较电子层数,电子层数多的半径大。
(2)电子层数相同时,再比较核电荷数,核电荷数多的半径反而小。
对除稀有气体元素原子以外的任何原子或离子的半径进行比较要“三看”:
① 首先看层,层少半径小;
② 同层看核,核大半径小;
③ 同核看价,价高半径小.
四、化学键
化学键是相邻两个或多个原子间强烈的相互作用。

1.离子键与共价键的比较
离子化合物:由离子键构成的化合物叫做离子化合物。(一定有离子键,可能有共价键)
共价化合物:原子间通过共用电子对形成分子的化合物叫做共价化合物。(只有共价键)
 极性共价键(简称极性键):由不同种原子形成,A-B型,如,H-Cl。
极性共价键(简称极性键):由不同种原子形成,A-B型,如,H-Cl。
共价键
非极性共价键(简称非极性键):由同种原子形成,A-A型,如,Cl-Cl。
2.电子式:
用电子式表示离子键形成的物质的结构与表示共价键形成的物质的结构的不同点:(1)电荷:用电子式表示离子键形成的物质的结构需标出阳离子和阴离子的电荷;而表示共价键形成的物质的结构不能标电荷。(2)[ ](方括号):离子键形成的物质中的阴离子需用方括号括起来,而共价键形成的物质中不能用方括号。
高一化学必修2第一章单元测试题
一、选择题
1.下列元素中,最高正化合价数值最大的是( )。
A.C B.F C.S D.Ne
2.已知某粒子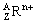 ,则元素R的原子序数是( )。
,则元素R的原子序数是( )。
A.Z B.A-Z C.Z-n D.Z+n
3.元素的性质随着元素原子序数的递增而呈周期性变化的原因是( )。
A.元素原子的核外电子排布呈周期性变化
B.元素的原子半径呈周期性变化
C.元素的化合价呈周期性变化
D.元素的金属性、非金属性呈周期性变化
4.下列粒子半径之比小于1的是( )。
A.r (Na+)/ r (Na) B.r (Cl-)/ r (Cl)
C.r (Na)/ r (Mg) D.r (Ca)/ r (Mg)
5.有A、B、C、D四种金属,投入水中只有D反应放出氢气,将A投入C的盐溶液中可置换出金属C,B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,则四种金属的金属性强弱顺序正确的是( )。
A.A>B>C>D B.D>B>A>C
C.B>A>C>D D.C>A>B>D
6.下列事实不能说明非金属性Cl>I的是( )。
A.Cl2+2I-==2Cl-+I2 B.稳定性:HCl>HI
C.酸性:HClO4>HIO4 D.酸性:HClO3>HIO3
7.下列说法错误的是( )。
A.原子半径:F<Mg<K B.稳定性:PH3>H2S>NH3
C.酸性:H3PO4<H2SO4<HClO4 D.碱性:Al(OH)3<Mg(OH)2<KOH
8.运用元素周期律分析下面的推断,其中不正确的是( )。
A.锂(Li)与水反应比钠与水反应剧烈
B.砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸
C.在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
D.HBrO4的酸性比HIO4的酸性强
9.X元素的阳离子和Y元素的阴离子都具有与Ar原子相同的电子层结构,下列叙述正确的是( )。
A.X的原子序数比Y小 B.X原子的最外层电子数比Y大
C.X的原子半径比Y大 D.X元素的最高正价比Y大


 10.已知下列反应:Cu+X2 CuX2、2Cu+Y Cu2Y、2X-+Z2 2Z-+X2,X2、Y 、Z2为三种元素的单质,在Cu2Y中,Y为-2价。下列关于X、Y、Z三种元素的最高价氧化物的水化物酸性由强到弱顺序正确的是( )。
10.已知下列反应:Cu+X2 CuX2、2Cu+Y Cu2Y、2X-+Z2 2Z-+X2,X2、Y 、Z2为三种元素的单质,在Cu2Y中,Y为-2价。下列关于X、Y、Z三种元素的最高价氧化物的水化物酸性由强到弱顺序正确的是( )。
A.HXO4>H2YO4>HZO4 B.HZO4>HXO4>H2YO4
C.HZO4>H2YO4>HXO4 D.H2YO4>HZO4>HXO4
11.A、B、C三种元素的核电荷数都小于18,A元素的原子最外层电子数是1,B元素原子的最外层得到1个电子就达到稳定结构,C元素原子最外层电子数是次外层电子数的3倍,则这三种元素组成的化合物不可能的是( )。
A.A2BC3 B.ABC3 C.ABC4 D.ABC
12.X、Y代表两种非金属元素,下列不能说明非金属性X比Y强的是( )。
A.Y的阴离子Y 2-的还原性强于X的阴离子X-
B.X的含氧酸的酸性比Y的含氧酸的酸性强
C.X的单质X2能将Y的阴离子Y 2-氧化,并发生置换反应
D.X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价
12.某元素R的最高价氧化物的水化物分子式是HnRO2 n-2,则在气态氢化物中R元素的化合价是( )。
A.3n-10 B.12-3n C.3n-4 D.3n-12
13.R、W、X、Y、Z为原子序数依次递增的11~18号元素中的五种元素,下列说法一定正确的是(m、n均为正整数)( )。
A.若R(OH)n为强碱,则W(OH)m也为强碱
B.若HnXOm为强酸,则Y是活泼的非金属元素
C.若Y的最低化合价是-2,则Z的最高正化合价为+6
D.若X的最高正化合价为+5,则五种元素都是非金属元素
14.已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )。
A.质子数:c>b B.离子的还原性:Y2->Z-
C.氢化物的稳定性:H2Y>HZ D.原子半径:X<W
15.已知某元素的原子序数,则不能推出该元素原子的( )。
A.质子数 B.中子数 C.电子数 D.核电荷数
16. 和
和 的原子半径,前者和后者的关系是( )。
的原子半径,前者和后者的关系是( )。
A.前者大 B.后者大 C.两者相等 D.不能确定
17.下列物质中,碱性最强的是( )。
A.NaOH B.Mg(OH)2 C.Al(OH)3 D.KOH
18.下列各组指定原子序数的元素,能形成A2B3型化合物的是( )。
A.6和8 B.11和9 C.12和17 D.13和8
19.已知核电荷数均小于18的X、Y、Z、W四种元素原子的电子层数相同,而原子半径依次增大,则下列物质中酸性最强的是( )。
A.HXO4 B.H2YO4 C.H3ZO4 D.H4WO4
20.A元素原子的最外层上有3个电子,它能与元素B形成A2B3型化合物,则B元素最高价氧化物对应的水化物的化学式是( )。
A.B(OH)3 B.H2BO3 C.H2BO4 D.H3BO4
21. 下列含有共价键的化合物是( )
A.HI B. NaOH C. Br2 D. NaCl
22. 下列电子式书写正确的是( )

23. 下列叙述正确的是( )
A.O2分子间存在着非极性共价键
B.CO2分子内存在着极性共价键
C.SO2与H2O反应的产物是离子化合物
D.盐酸中含有H+和Cl-,故HCl为离子化合物
24.含有下列键型的物质,可能为单质的是( )
A.只有离子键的物质 B.既有离子键,又有非极性键的物质
C.既有极性键,又有离子键的物质 D.只有非极性键的物质
25.下列不是离子化合物的是( )
A. H2O B. CaI2 C. KOH D. NaNO3
二、填空题
1.原子序数11~17的元素,自钠到氯,电子层数相同,最外层电子数从 增加到 ,随着核电荷数依次递增,原子半径依次 ,核对外层电子的引力逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,因此,金属性逐渐 ,非金属性逐渐 。
2.元素金属性的强弱,可以从它的单质与水或酸反应置换氢的 程度,以及它的最高价氧化物的水化物的 强弱来判断。元素非金属性的强弱,可以从它的最高价氧化物的水化物的 强弱,或它的单质跟H2生成气态氢化物的 及氢化物的 来判断。
3.具有双核10个电子的共价化合物的化学式是 ,三核10个电子的共价化合物的化学式是 ,四核10个电子的共价化合物的化学式是 ,五核10个电子的共价化合物的化学式是 。以上四种化合物的热稳定性由小到大的顺序是 。
4.已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
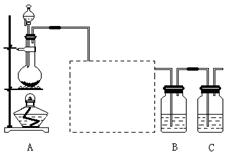
(1)装置A的分液漏斗中盛装的试剂是 ,烧瓶中加入的试剂是 。
(2)画出虚线框内的实验装置图,并注明所加试剂,说明装置的作用 。
(3)装置B中盛放的试剂是 (选填下列所给试剂的代码),实验现象为 ,化学反应方程式是 ,该反应属于四种基本反应类型中的 反应。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)从原子结构的角度简要分析氯元素的非金属性比硫元素的非金属性强的原因。 。
(5)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)。 。
(6)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气。在该反应中,Cl元素的化合价既有升高又有降低,即在反应中Cl元素的原子既能获得电子也能失去电子,能否说氯元素既具有金属性又具有非金属性?简述你的理由。 。
5.已知具有相同电子层结构的离子,核电荷数越大,离子半径越小。X和Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径比Y元素的阳离子半径大。Z和Y两元素原子的电子层数相同,Z元素的原子半径小于Y元素的原子半径。X、Y、Z三种元素原子序数的关系是 。
6. A、B、C、D、E、F六种元素,它们的核电荷数均小于18,且原子序数逐渐增大。已知:A、C、F三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。11.5g A单质恰好与100mL 5mol/L的盐酸完全反应,反应后溶液呈中性。D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。请回答下列问题:
(1)写出D的元素符号 ,E的最高价氧化物的水化物的分子式 。
(2)画出B元素的原子结构示意图 。
(3)若构成F元素的一种原子的质量数为35,写出其原子符号 ,它原子核内的中子数是 。
(4)A与F、C与F元素最高价氧化物的水化物反应的离子方程式依次为: 、 、 。
7.元素的性质随着元素 的递增而呈周期性变化,这个规律叫做元素周期律。元素性质的周期性变化是元素原子的 的周期性变化的必然结果。
8.通过简单地推理或计算填空:
(1)X原子有两个电子层,它能与最活泼的金属Y形成Y3X的化合物,X是 元素。
(2)若某元素原子的电子层数和Na原子的相同,最外层电子数与F原子相同,则该元素的原子序数是 。
(3)6C元素能够与某非金属元素R形成化合物CRx,已知CRx分子中各原子核外最外层电子总数为32,核外电子数总和为74。则R是 元素,x= 。
9.根据元素周期律填空:
(1)已知SiH4能够在空气中自燃,H2S可燃,试推测PH3应 ;
(2)已知H2SiO3为弱酸,H2SO4为强酸,则H3PO4为 ;
(3)已知氢氧化铝又称为铝酸(H3AlO3),当其失去水后变成HAlO2称为偏铝酸,则H3PO4称为 ,而HPO3称为 。
(4)已知NaOH为强碱,Al(OH)3为两性氢氧化物,则Mg(OH)2为 。
10.下表给出14~17号元素的一些性质,请回答:
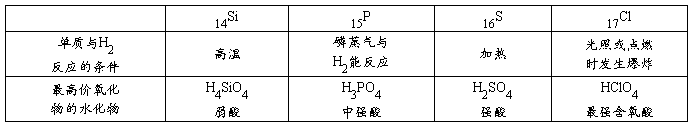
(1)它们所形成的氢化物中稳定性最差的是 ,还原性最差的是 。
(2)四种元素的非金属性随着元素原子序数的递增而逐渐 ,试从原子结构的角度加以解释。 。
(3)一定条件下,反应H2S+Cl2=2HCl+S能否发生?简述理由。
11. A、B、C三种元素的原子具有相同的电子层数,B的核电荷数比A大两个单位,C的质子数比B多4个。1mol A的单质与酸反应,能置换出1g H2,这时A转化为具有与氖原子的电子层结构相同的离子。请回答:
(1)写出B元素的化学名称 ,画出C元素的原子结构示意图 。
(2)若构成A元素的一种原子的质量数是23,写出其原子符号 。
(3)B元素的最高价氧化物及其对应的水化物具有 性。
12.某元素R原子的核外电子数等于核内中子数,该元素的单质2.8g与氧气充分反应,生成6.0g的化合物RO2。请回答:
(1)元素R的原子序数是 。
(2)元素R的原子共有 个电子层,能量最低的电子层中共有 个电子。
(3)写出元素R的最高价氧化物对应水化物的化学式 ,它的酸性比碳酸的酸性 。
答案:
一、选择题
1.C 2.A 3.A 4.A 5.B 6.D 7.B 8.A 9.C 10.B 11.A
12.C 13.B 14.B 15.B 16.A 17.D 18.D 19.A 20.C 21.B
22. D 23 .A 24. D 25. A
二、填空题
1.1 7 减小 增大 减弱 增强 减弱 增强
2.难易 碱性 酸性 难易 稳定性
3.HF H2O NH3 CH4 CH4<NH3<H2O<HF
4.(1)浓盐酸 MnO2
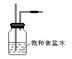 (2) 除去Cl2中的HCl气体
(2) 除去Cl2中的HCl气体
(3)A 有淡黄色沉淀生成 Na2S+Cl2=2NaCl+S↓ 置换
(4)Cl原子、S原子的电子层数相同,但最外层电子数Cl原子是7,S原子是6,且原子半径Cl<S,因此,在反应中Cl原子比S原子更容易获得电子达稳定结构,故氯元素的非金属性比硫元素的非金属性强。
(5)HCl的稳定性比H2S的稳定性强或者HClO4的酸性比H2SO4的酸性强。(其他合理答案均可)
(6)不能,金属性强弱的判断以元素的单质与水(或酸)反应置换氢的难易程度,以及它的最高价氧化物的水化物的碱性强弱为依据。非金属性的强弱以它与氢气生成氢化物的稳定性或它的最高价氧化物的水化物的酸性强弱来判断。(其他合理答案均可)
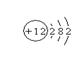 5.X<Y<Z
5.X<Y<Z
6.(1)Si H3PO4 (2)
(3)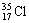 18
18
(4)H++OH-= H2O Al(OH)3+3H+=Al3++3H2O
7.原子序数 核外电子排布
8.(1)N (2)17 (3)Cl 4
9.(1)易燃 (2)中强酸 (3)磷酸;偏磷酸 (4)中强碱
10.(1)SiH4 HCl
(2)增强 四种元素原子的电子层数虽相同,但最外层电子数依次增加,随着核电荷数依次递增,原子半径依次减小,核对外层电子的引力逐渐增大,得电子能力逐渐增强,因此,非金属性逐渐增强。
(3)能够发生,因非金属性Cl>S,氧化性Cl2>S,故Cl2能置换出H2S的硫。

11.(1)铝
(2) (3)两
(3)两
12.(1)14 (2)3 2 (3)H4SiO4(或H2SiO3) 弱
