初中化学除杂题的解题方法
将混合物中的几种物质分开而分别得到较纯净的物质,这种方法叫做混合物的分离。将物质中混有的杂质除去而获得纯净物质,叫提纯或除杂。除杂题是初中化学的常见题,它灵活多变,可以综合考察学生的解题能力。现列举几种方法,供大家参考。
一.物理方法
1.过滤法原理:把不溶于液体的固体与液体通过过滤而分开的方法称为过滤法。如:氯化钙中含有少量碳酸钙杂质,先将混合物加水溶解,由于氯化钙溶于水,而碳酸钙难溶于水,过滤除去杂质碳酸钙,然后蒸发滤液,得到固体氯化钙。如果要获得杂质碳酸钙,可洗涤烘干。
练习1.下列混合物可以用溶解、过滤、蒸发操作来分离的是;
( )
A.CaC03 CaO B.NaCl KN03 C.NaN03 BaS04 D.KCl KClO3
2.结晶法原理:几种可溶性固态物质的混合物,根据它们在同一溶剂中的溶解度或溶解度随温度的变化趋势不同,可用结晶的方法分离。例如:除去固体硝酸钾中混有的氯化钠杂质,先在较高温度下制成硝酸钾的饱和溶液,然后逐步冷却,由于硝酸钾的溶解度随温度的升高而显著增大,温度降低,大部分硝酸钾成为晶体析出,而氧化钠的溶解度随温度的升高而增大得不显著,所以大部分氯化钠仍留在母液中,通过过滤把硝酸钾和氧化钠溶液分
开。为进一步提纯硝酸钾,可再重复操作一次,叫重结晶或再结晶。
练习2.下列混合物适宜用结晶法分离的是( )
A.NaN03 Na2C03 D.NaN03 NaCl C.NaOH
Mg(OH)2 D.NaCl BaS04
二.化学方法
原理:
(一).加入的试剂只与杂质反应,不与原物反应。
(二).反应后不能带人新的杂质。
(三).反应后恢复原物状态。
(四).操作方法简便易行。
初中常用化学除杂方法有以下几种:
1.沉淀法 使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。
A.KN03 [Ba(N03)2] B.NaCl [KN03] C.NaN03
[NaCl] D.Ca(N03)2 [AgCl]
2.气体法 将混合物中的杂质与适当试剂反应变成气体而除去。如:硝酸钠固体中含有少量碳酸钠杂质,可将混合物加水溶解,再加入适量稀硝酸溶液,硝酸与碳酸钠反应生成硝酸钠、水和二氧化碳,再蒸发滤液,获得硝酸钠固体。
练习4.下列混合物中的杂质(括号内的物质是杂质)适宜用气体法除去的是:( )
A.NaN03 [Ba(N03)2] B.NaCl [Mg(OH)2] C.KN03
[K2C03] D.Na2S04 [MgS04]
3.置换法 将混合物中的杂质与适量试剂通过发生置换反应而除去。
练习3 下列混合物可用沉淀法除去杂质(括号内的物质是杂质)的是( ) 如:硫酸锌固体中含有少量硫酸铜杂质,可将混合物溶解之后,加入适量锌粉,再过滤除去被置换出来的铜,蒸发滤液获得硫酸锌固体。
练习5.加入下列哪些物质可以除去硫酸亚铁溶液中混有的少量杂质硫酸铜( )
A.Zn B.Fe C.Cu D.Mg
练习6.将混有少量铁粉和锌粉的硫酸铜晶体溶于适量水,充分净置过滤,结果是( )
A.滤出了混杂在其中的铁粉 B.滤出了混杂在其中的锌粉 C.滤出了一些铜粉 D.什么也没滤出
4.吸收法 两种以上混合气体中的杂质被某种溶剂或溶液吸收,而要提纯的气体不能被吸收时,可用此方法。如:一氧化碳中含有二氧化碳时,可将混合气体通过盛有氢氧化钠的溶液。
5.其它法 将混合物中的杂质用化学方法转化成其它物质。如:氧化钙中含有碳酸钙,可采用高温燃烧的方法,使碳酸钙高温分解成氧化钙和二氧化碳,二氧化碳扩散到空气中,除去杂质。
第二篇:初中化学推断题题型与解题方法
初中化学推断题题型与解题方法(第一课时)
授课者 陈娥英
一、教学目的要求
1、知识与技能
(1)进一步熟悉常见物质的化学性质。
(2)能熟练掌握酸、碱、盐的化学性质。
2、过程与方法
(1)引导学生找出推断题中的突破口。
(2)学会解答化学推断题的方法和技巧。
3、情感态度与价值观
(1)培养学生的合作意识,以及勤于思考,严谨求实的科学态度。
(2)提高审题、分析、表达、判断等解题能力,运用所学化学知识解决实际问题。
二、教学重点和难点
重点:能综合运用所学过的知识解答化学推断题。
难点:找出推断题中的突破口。
三、课型
复习课
四、教学过程
[引入]从每一次的综合练习中我们可以知道推断题是必不可少的,所以我们应该熟练掌握常见类型推断题的解法。
一、叙述式推断题
[学生练] 1、有一包粉末可能含有碳酸钙、碳酸钠、硫酸钠、硫酸铜、硝酸钠中的一种或几种,某学生为了确定其组成,做如下实验,请根据实验现象进行推断,把 相应的物质的化学式填在表中的空格内。
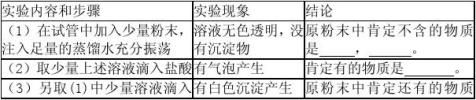

[[教师引导]
CuSO4;没有沉淀物,证明无CaCO3。
(2)加加HCl后有气泡产生,证明含有Na2CO3。
(3)因为溶液中含有Na2CO3加后BaCl2有白色沉淀生成,但也有可能含有Na2SO4。
(4)加稀HNO3后白色沉淀部分溶解并有气泡产生,证明(3)中不但含有BaCO3,
还含有BaSO4,所以原混合物中含有Na2SO4。
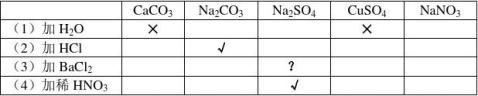
[学生练] 2、有一包白色粉末,可能由氯化银、碳酸钠、氢氧化镁、氯化钡、硫酸钠和硝酸钾中的某几种组成。为了鉴定其成分,实验如下:
(1)将少量粉末放入足量水中,搅拌、静置、过滤、得白色沉淀和无色滤液。
(2)向所得沉淀中加入足量稀硝酸,沉淀全部溶解,但无气体产生。
(3)向滤液中滴加硝酸银溶液,有白色沉淀生成,加入足量稀硝酸,沉淀不溶解。试根据以上现象推断该白色粉末中一定含有 ;一定没有 ;可能含有

。(填化学式)
[学生讨论]
[教师引导]
第一步不能判断哪一种物质是否存在。
(2)加加稀HNO3后,因为沉淀全部溶解,所以混合物中没有AgCl,有Mg(OH)2,对于BaCl2和Na2SO4,如果要有的话,只能含有其中一种;无气体产生证明无Na2CO3。
(3)加AgNO3溶液,有白色沉淀生成,加入足量稀硝酸,沉淀全部溶解,证明溶
液中含有氯离子,则溶液中含有BaCl2,所以原混合物中无Na2SO4。
小结:叙述式推断题:此类题型主要推断混合物中的成分,题目条件中已经给出了混合物的组成范围,要求根据实验现象确定哪些物质一定存在,哪些物质一定不存在,哪些则不能确定存在与否,解题时应该紧扣实验现象做出正确判断,尤其应该注意肯定判断出某些物质存在时,不能与其共存的物质肯定不存在。
二、表格式推断题
[学生练]3、有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。

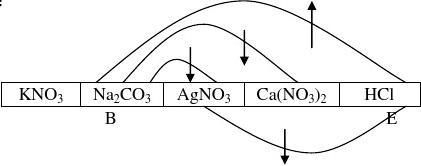
(1A ,B ,C ,D ,E 。
(2)写出有关反应的化学方程式。
A+E
B+E
[学生讨论]
[教师引导]
由题目中的表格可以知道本题的突破口两个:(1)B能与其中三种物质反应,而且两个反应能产生沉淀,一个能产生气泡;(2)E能与其中两种物质反应,一个反应能产生沉淀,一个反应能产生气泡。
先以表格形式列出物质两两反应的实验现象。
由表三可以清晰知道B是Na2CO3,E是HCl,当推知B和E后,剩下的物质的推断就能迎韧而解。
[学生练] 4、为了不用任何试剂区别下列四种物质的溶液:碳酸钠、硝酸银、硝酸和氯化钠,给它们分别编号并各取少量两两混合。现象是:甲跟乙、甲跟丁混合均产生白色沉淀;丙跟丁混合放出气体;甲跟丙、乙跟丙、乙跟丁均不反应。写出甲、乙、丙、丁的化学式及它们之间反应的化学方程式。
提示:解答上题时,可用图表形式使其简化,从而便于推断。如本题可列表如下:

(1)甲 乙 丙 丁
(2)写出有关反应的化学方程式。
甲跟乙
甲跟丁
丙跟丁
[学生讨论]
[教师引导]
本题的突破口有(1)甲能与其中两种物质反应都能产生沉淀;(2
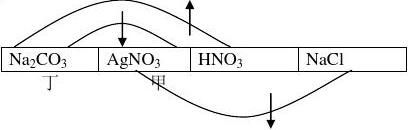
)丁能与其中两种物质反应,一个反应能产生沉淀,一个反应能产生气泡。
由表四可以清晰知道甲是AgNO3,丁是Na2CO3,当推知甲和丁后,剩下的物质的推断就一目了然。
小结:
二、表格式推断题:词题目给出了推断的范围并以表格形式列出了物质两两反应的实验现象,要求根据相互反应的现象推断各物质分别是什么。解题时可以抓住某一物质与其他都反应的或者反应最少的打开突破口;或先不管题目给的实验现象,将题中几种物质两两反应的反应自行列表,再与题中表格对照,对号入座即可。
20xx年5月
附录
溶液中不能大量共存的离子有以下;
1、H+与OH-– 2、H+与CO32-– 3、Ag+与Cl-– 4、Ba2+与SO42-–
5、Cu2+、Zn2+、Al3+、Fe2+、Fe3+、与OH-–
6、Ba2+、Ca2+、Ag+、与CO32-– 沉淀颜色
1、白色沉淀不溶于稀硝酸:AgCl、BaSO4
2、白色沉淀溶于酸而且有大量气泡产生:Ag2CO3、BaCO3、CaCO3
3、浅绿色沉淀:Fe(OH)2
4、红褐色沉淀:Fe(OH)3
5、蓝色沉淀:Cu(OH)2
溶液的颜色
1、蓝色溶液:含Cu2+的溶液,如CuSO4溶液,CuCl2溶液、Cu(NO3)2溶液。
2、浅绿色溶液:含Fe2+的溶液,如FeSO4溶液,FeCl2溶液、Fe(NO3)2溶液。
3、黄色溶液:含Fe3+的溶液,如Fe2(SO4)3溶液,FeCl3溶液、Fe(NO3)2溶液。
教学反思:
本节课的重点是让学生学会解推断题的方法,特别是要学会找题目中的突破口,在课堂上学生练习的时间大约是二十分钟,给学生足够的时间,但从巡堂观察学生的情况可以知道,学生解这类型的题目,还存在一些问题,主要有(1)没有审清题目,对题目中关键的词语没有注意到;(2)学生基础知识不扎实;(3)有小部分学生对这类型的题目,失去信心,不敢去做。
本人在讲解的过程中,尽量采用直观的教学方式,目的是让学生更容易掌握,但还有待提高。
20xx年5月
