北 方 民 族 大 学
学生实验报告
院(部): 化学与化学工程
姓 名: 郭俊雄 学 号: 20082995 专 业: 化学工程与工艺 班 级: 081 同组人员: 林艺明、 胡鹏、 秦开勉 课程名称: 化工原理实验 实验名称: 萃取实验 实验日期: 2010.11.11 批阅日期: 成 绩: 教师签名:
北方民族大学教务处制
实验名称:萃取实验
一、实验目的
1.了解转盘萃取塔的结构和特点;
2.掌握液—液萃取塔的操作;
3.掌握传质单元高度的测定方法,并分析外加能量对液液萃取塔传质单元高度和通量
的影响。
二、基本原理
萃取是利用原料液中各组分在两个液相中的溶解度不同而使原料液混合物得以分离。将一定量萃取剂加入原料液中,然后加以搅拌使原料液与萃取剂充分混合,溶质通过相界面由原料液向萃取剂中扩散,所以萃取操作与精馏、吸收等过程一样,也属于两相间的传质过程。
与精馏,吸收过程类似,由于过程的复杂性,萃取过程也被分解为理论级和级效率;或传质单元数和传质单元高度,对于转盘塔,振动塔这类微分接触的萃取塔,一般采用传质单元数和传质单元高度来处理。传质单元数表示过程分离难易的程度。
对于稀溶液,传质单元数可近似用下式表示:
NOR??x1dxx?x*x2 (1)
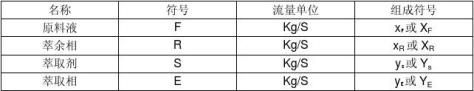
式中: NOR——萃余相为基准的总传质单元数;
X——萃余相中的溶质的浓度,以摩尔分率表示;
x*——与相应萃取浓度成平衡的萃余相中溶质的浓度,以摩尔分率表示。
x1、x2——分别表示两相进塔和出塔的萃余相浓度
…… …… 余下全文




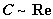 关系曲线应在 单对数 坐标纸上标绘。
关系曲线应在 单对数 坐标纸上标绘。 关系曲线在双对数坐标上应为 直线 。
关系曲线在双对数坐标上应为 直线 。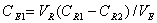 。
。