临床评估报告
(模板适用于设备)
文件编号:xxxxxxxx

编制:xxx
审核:xxx (需要有临床背景)
XXXXXXXXX有限公司
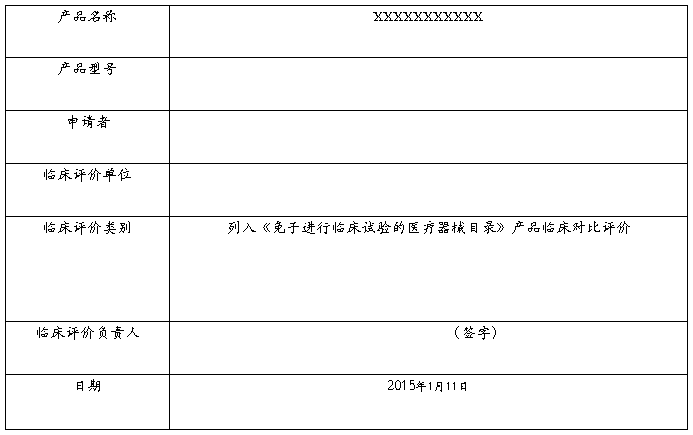
临床评价对象:(设备名称)
1. 临床使用情况的概述:
1.1 预期用途
1.2 基本结构
1.3 与其相配套的设施(如果有,包括连接接口的描述):
1.4 临床原理
3. 临床评价途径
EN ISO14155:2011Clinical investigation of medical devices for human subjects —
Part 1: General requirements
MDD指令2.7.1 V.3: 2009.12 医疗器械指南 临床评价:为企业与公告机构提供的指南附录D
4. 临床使用历史的描述:
4.1 使用历史:
4.2 临床出现不良事件的统计:
4.2.1 国内数据查询:
4.2.2 国外数据查询:
4.2.3 对临床不良事件信息的分析:
4.2.4 关于“严重不良事件”信息的分析。
4.3 临床文献的收集与分析
4.3.1 文献的纳入及排除标准:
纳入标准:1)文献主题和本临床课题相关度高、联系紧密的文章;
(应包括临床相关度要素,临床与这些要素的关联程度的描述,纳入或排除的理由)
…… …… 余下全文