霍城县中学教学参评设计
课题:电化学解题方法探究
——难点突破之电极反应式的书写
姓名:徐惠明
单位:新疆伊犁霍城县江苏中学
邮编:835200
邮箱:571069085@QQ.COM
电话:137xxxxxxxx
1
霍城县中学教学参评设计
电化学复习专题:
电化学解题方法探究
——难点突破之电极反应式的书写
1 理论依据
建构主义理论最核心的内容是:“以学生为中心,强调学生对知识的主动探索、主动发现和对所学知识意义的主动建构。建构主义认为,学习者要想完成对所学知识的意义建构,即达到对该知识所反映事物的性质、规律以及该事物与其它事物之间联系的深刻理解,最好办法是让学习者到现实世界的真实环境中去感受、去体验,因此,本节课我主要采用抛锚式教学或“情境性教学”。
即:创设情境--确定问题--自主学习--协作学习--效果评价 考纲要求
1、了解原电池和电解池的工作原理。能写出电极反应和电池反应方程式。
2、了解常见化学电源的种类及其工作原理。
3、理解金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。
2 教材分析
电化学是无机化学中很重要的内容,它与基本概念、基本理论、元素化合物等内容密切相关。化学能与电能的相互转化是氧化还原反应本质的拓展和应用,其中涉及到电极的判断和电极反应式、离子放电规律、电解产物分析及溶液pH的变化、电化学计算、实验设计等知识点。电化学还常常涉及到物理学中的串联电路、并联电路等。无疑,有关电化学知识也必然是物理学和化学的交汇点,这一融合正反映了突破学科中心,实施素质教育的新课程理念,将会成为理科综合测试的重点。为此,确立了本节内容的重点是“两池”(原电池和电解池)的化学反应原理,而电解产物的判断方法及溶液pH的变化规律则是本部分的难点。 3 学情分析
前面学生虽然已经学习了原电池与电解池的相关知识,探究了化学能与电能的相互转化,初步学会了电极反应式的书写,也接触到了几种化学电源及金属的电化学腐蚀等知识,但是对于原电池和电解池相关知识的理解仍然存在问题,在解题过程中也常常出现错误,因此,还需要再进一步加以对比、辨析和归纳,从而使学生对这些内容有更加全面和深刻的理解。
4 教学目标的确立
为了帮助学生进一步区分原电池和电解池,更好地理解和掌握电化学知识,我在教学过程中设立的教学目标如下。
4.1知识与技能:
通过原电池、电解池的知识对比,使 学生进一步掌握原电池、电解池的化学反应原理、电极的判断、电极反应式的书写、离子放电规律、电解产物分析及溶液pH值的变化、电化学计算、实验设计等知识点。
4.2过程与方法:
在复习原电池和电解池知识的过程中,运用对比、归纳、总结等教学方法通过问题探究,培养学生知识的迁移能力和多角度思维能力以及应用所学知识解决实际问题的能力。
4.3情感态度与价值观:
2
使学生在探究化学能与电能之间相互转化奥秘的过程中,提高学习化学的兴趣和热情,感受化学世界的奇妙与和谐。
5 教学流程
一、高考怎样考?--------考题体验
2011高考
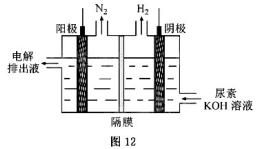
(4)电解尿素[CO(NH2)2]的碱性溶液制氢
的装置示意图
见图12(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为--------------------------------------------------- 20xx年高考
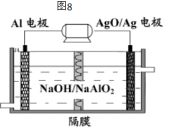
铝电池性能优越,Al-AgO电池可作水下动力电源,
其原理如图该电池的反应为----------------------------------------------
20xx年高考
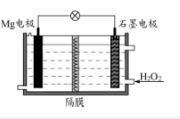
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以
海水为电解质,示意图如上。该电池工作时,下列说法正确的是( )
A. Mg电极是该电池的正极
B. H2O2在石墨上发生氧化反应
C. 石墨电极附近的溶液的pH值增大
D. 溶液中的Cl-向正极移动
二、迎考怎样准备?-----知识精要
1、两电池的对比
①构成:原电池:------------
电解池:---------------
3
②电极名称: 原电池:----------------- 电极反应:------------------- 电解池:----------------- 电极反应:------------------
【归纳】
电解时离子放电顺序:------------------------------------------
【特别提醒】高考时有时不按常规出牌,要随机应变
20xx年高考
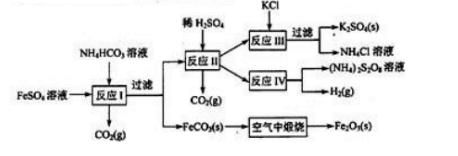
反应Ⅳ
常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为---------------------------- 。
2、两电池外电路电子流向
原电池:-------------------------
电解池:----------------------------
特别注意:
溶液中无电子通过,导电的是通过阴阳离子的移动而导电的。电流的方向与电子流的方向相反。
【典例精炼】
1、某种可充电聚合物锂离子电池放电时的反应为Li1-xCoO2+LixC6===6C+LiCoO2,下列说法不正确的是 ( )
A.放电时LixC6发生氧化反应
B.充电时,Li+通过阳离子交换膜从左向右移动
C.充电时将电池的负极与外接电源的负极相连
D.放电时,电池的正极反应为Li1-xCoO2+xLi++xe-===LiCoO2
2、控制适合的条件,将反应2Fe3++2I-2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是 ( )
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
3. 将两个铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产 4
生电流。下列叙述正确的是 ( )
①通入CH4的电极为正极
②正极的电极反应式为O2+2H2O+4e-===4OH-
③通入CH4的电极反应式为CH4+2O2+4e-===CO2+2H2O
④负极的电极反应式为CH4+10OH--8e-===CO32-+7H2O
⑤放电时溶液中的阳离子向负极移动
⑥放电时溶液中的阴离子向负极移动
A.①③⑤ B.②④⑥
C.④⑤⑥ D.①②③
4. 电解尿素[CO(NH2)2]的碱性溶液制氢气的装置示意图如下
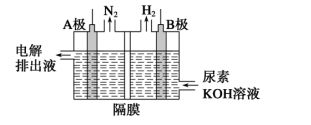
:
电解池中隔膜仅阻止气体通过,阴阳两极均为惰性电极,
(1)A极为________,电极反
________________________________________。
(2)B极为________,电极反
________________________________________。 应应式式为为
【归纳】陌生电极的书写方法
①标价定电子②平衡电荷③原子守恒
注意:
1、碱性不出现H+和CO2
2、酸性不出现OH-、
3、关注非水介质如熔融盐、 熔融金属氧化物
4、Fe做电极失2e-生成Fe2+
5、二次电池放电为原电池充电为电解池充电时正----正相接、负----负相接
【课后练习】
1、有关下列四个常用电化学装置的叙述中,正确的是
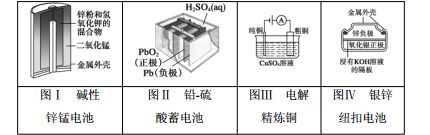
( )
A.图Ⅰ所示电池中,MnO2的作用是催化剂
B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
5
D.图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
2、 在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过 下列装置所示实验进行探究。下列说法正确的是 ( )
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-===Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O===4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
3、以黄铜矿精矿为原料,制取硫酸铜及金属铜的工艺如下所示:
Ⅰ.将黄铜矿精矿(主要成分为CuFeS2,含有少量CaO、MgO、Al2O3)粉碎。 Ⅱ.采用如下装置进行电化学浸出实验将精选黄铜矿粉加入电解槽阳极区,恒速搅拌,使矿粉溶解。
在阴极区通入氧气,并加入少量催化剂。
Ⅲ.一段时间后,抽取阴极区溶液,向其中加入有机萃取剂(RH)
发生反应:2RH(有机相)+Cu2+ (水相)----- R2Cu(有机相)+2H+ (水相)分离出有机相,向其中加入一定浓度的硫酸,使Cu2+得以再生。
Ⅳ.电解硫酸铜溶液制得金属铜。
(1)黄铜矿粉加入阳极区与硫酸及硫酸铁主要发生以下反应:
(2)CuFeS2+4H+===Cu2++Fe2++2H2S2Fe3++H2S===2Fe2++S↓+2H+ ①阳极区硫酸铁的主要作用是____________。
②电解过程中,阳极区Fe3+的浓度基本保持不变,原因是______________________。
(2)阴极区,电极上开始时有大量气泡产生,后有固体析出,一段时间后固体溶解。写出上述现象对应的反应式____________________。
(3)若在实验室进行步骤Ⅲ,分离有机相和水相的主要实验仪器是__________;加入有机萃取剂的目的是__________。
(4)步骤Ⅲ,向有机相中加入一定浓度的硫酸,Cu2+得以再生的原理是____________。
(5)步骤Ⅳ,若电解 200 mL 0.5 mol·L-1的 CuSO4溶液,生成铜 3.2 g,此时溶液中离子浓度由大到小的顺序是__________。
小结:电化学试题的一般解答方法
1、仔细审题,找出有效信息
如:是原电池还是电解池?
6
是什么电极?
是根据什么氧化还原反应设计?
是什么环境?
2、写出电极反应式
(1)确定发生化合价变化的元素
(2)确定转移的电子数
(3)明确反应环境,根据三大守恒完成方程式
3、根据题设回答问题
注意答题规范性
教学反思:
一:本堂课没有完全达到了我们的预期目标;层次好一些的班级学生能有六成的过关率,究其原因,学生没能更好的领悟老师的引导,同时科任老师也需从多方面来对学生进行更好的兴趣引导,高考复习需要的是老师的精心,学生的用心。 二:课堂的师生交互的,学生的参与活动方面:
本节课是多媒体课,通过课件中的丰富展示,如:
1、判断是原电池还是电解池:---------是否有外加电源
2、判断电极---------本质:氧化反应、还原反应
3、写出电极反应式-------本质是氧化还原反应
(1)根据放电顺序确定得失电子的物质
(2)根据化合价变化确定转移的电子数
(3)明确反应环境,根据“三大守恒”完成方程式
等方面,学生的参与意识还是很强的,回答的积极,正确率也高。但上升到高考试题,学生马上就产生了一定的恐惧感,我认为,我们的复习不全是知识的复习,在一定的场景中,实施心理疏导也显得尤为重要!!!
三:本节课我们采取的教学策略:
(1) 由浅入深,适时关注学生,学生能接纳的多讲,接纳有困难的慢讲。
(2) 精选高考模拟题,注意培养学生们的心理承受能力。切不可一次性就把学
生吓倒!!
本人充分运用了多媒体和信息技术创设生动教学情境的教学策略,实践结果说明了情境教学是有效的。
总之:从全过程来看,选题是适中的,内容是全面的。讲解是到位的,唯一美中不足的是,学生们的掌握程度不是很理想!!
教学感悟:人生如竞技场,总是看谁笑到最后的终点。让我们关注不同学段的差异性,一起思考怎样引领学生去“笑傲化学”。。。。。。
7
第二篇:电化学专题复习教案
电化学专题复习教案
一、考纲要求
正确区别原电池、电解池、电镀池的不同,掌握原电池、电解规律的应用及有关计算的方法技巧
二、知识结构

1、原电池、电解池、电镀池判断规律
若无外电源,可能是原电池,然后依据原电池的形成条件判定,主要思路是三“看” 先看电极:两种活泼性不同的金属(或其中一种非金属导体)作电极
再看溶液:用导线连接的两电极与 电解质溶液接触并形成闭合回路。
后看回路:在电解质溶液中能自发地发生氧化还原反应。
2、原电池的电极、电池反应式的写法。
①铅蓄电池:负极为 ,正极为 电解质溶液为硫酸。
负极:
正极:
电池反应:Pb+PbO2+2H2SO42PbSO4+2H2O
②银—锌高能电池:由负极为 ,正极为 ,电解质为KOH溶液。
( )极 Zn-2e+2OH-ZnO+H2O:( )极 Ag2O+2e+H2O
电池总反应: 2Ag+2OH-
③宇宙飞船上使用的氢氧燃料电池。H2为 极,氧气为 极,电解质为KOH溶
液。
负极(H2):
正极(O2):
电池反应:2H2+O22H2O
3、金属的腐蚀和防护
①金属腐蚀的本质是金属原子失去电子被氧化: ②金属腐蚀的类型及比较
化学腐蚀 电化学腐蚀
条件 金属与非电解质等直接接触 不纯金属或合金与电解质溶液接触 现象 无电流产生 有微弱电流产生
本质 金属被氧化的过程 较活泼金属被氧化的过程
相互关系 化学腐蚀与电化学腐蚀往往同时发生,但电化学腐蚀更普遍危害更严重。 ③金属腐蚀快慢的判断:
a.电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防腐蚀措施的腐蚀;
b.同一种金属的腐蚀:强电解质>弱电解质>非电解质
④金属的防护方法:(1)改变金属的内部结构(2)覆盖保护层(3)电化学保护法
4、分析电解应用的主要方法思路
通电前:电解质溶液的电离过程(包括电解质和水的电离)
离子移向:阴离子移向阳极,阳离子移向阴极
放电能力:
??阳极:金属阳极>S>I>Br>Cl>OH>NO3>SO2>F。 42+-----
阴极:Ag+>Hg2+>Fe3+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+。 电极反应: 电极反应式、总反应式
电解结果: 两极现象、水的电离平衡
离子浓度、溶液酸碱性、PH值变化等
四、例题精选
例1、把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上 有大量气泡产生,则四种金属的活动性顺序由强到弱为( )
A.a>b>c>d B.a>c>d>b
C.c>a>b>d D.b>d>c>a
例2、右图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。回答:
(1)直流电源中,M为 极。
(2)Pt电极上生成的物质是 ,其质量为
g。 (3)电源输出的电子,其物质的量与电极b、c、d
分别生成的物质的物质的量之比为:
2∶ ∶ ∶ 。
(4)AgNO3溶液的浓度(填增大、减小或不变。下
同)
,AgNO3溶液的pH ,H2SO4溶液的浓度 ,H2SO4溶液的pH 。 (5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为 g。
五、能力训练
1、在盛有饱和Na2CO3溶液的烧杯中插入惰性电极,保持温度不变,通直流电一段时间后,
则:
A.溶液的pH增大 C.溶液的浓度不变,有晶体析出 B.溶液的浓度增大,有一定量的晶体析出 D.溶液的pH减小
2、用铂作电极电解一定浓度的下列物质的水溶液。电解结束后,向剩余电解液中加适量水,能使溶液和电解前相同的是( )
A.AgNO3 B.H2SO4 C.NaOH D.NaCl

