碱金属及其化合物的性质实验报告
实验者: 实验日期:
实验目的:通过亲自做钠及化合物性质的实验,加强对碱金属及其化合物的性质的认识。
实验器材:试管、试管夹、烧杯、胶头滴管、铁架台、酒精灯、药匙、滤纸、
粗玻璃管,带导管的橡皮塞、铂丝、蓝色钴玻璃、水槽、镊子、蒸发皿、火柴、小刀
实验药品:钠、Na2O2、Na2CO3、NaHCO3、CuSO4溶液、 KCl溶液、稀盐酸、酚酞试液、澄清的石灰水。
实验步骤:
1、钠的性质

2、过氧化钠的性质
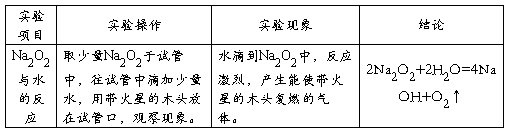
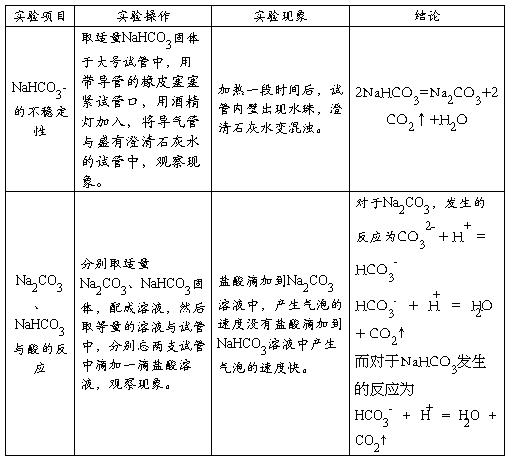
3、Na2CO3与NaHCO3的性质
4、用焰色反应检验Na+、K+、Cu2+

实验讨论:
1、在NaHCO3加热分解的实验时,为什么要先将导管移出烧杯,然后再熄灭酒精灯?
答:这样做主要是防止倒流。
2、做好焰色反应的关键是什么?
答:关键是将铂丝灼烧至无色。
[注意事项]:
1、不要用手直接接触金属钠
2、实验中所取钠块不得超过黄豆粒大小
第二篇:新编实验报告4(人教版高一)-碱金属单质及化合物的性质
高中化学实验四 碱金属单质及化合物的性质
【实验目的】
1、认识金属钠的物理性质,探究钠与氧气、水反应。
2、了解过氧化钠的物理性质,探究过氧化钠与水、二氧化碳的反应。
3、实验碳酸钠与碳酸氢钠的重要性质。
4、掌握焰色反应的实验操作。
【实验器具】
仪器:玻璃片、小刀、滤纸、镊子、坩埚盖、大烧杯、酒精灯、铁架台(带铁夹)、试管、火柴、铂丝(或光洁无锈铁丝)、酒精灯、蓝色钴玻璃(检验钾时用)
试剂:金属钠、过氧化钠、水、酚酞溶液、碳酸钠、碳酸氢钠、稀盐酸、氯化钠溶液、氯化钾溶液、胆矾粉末。
【实验探究过程与结论】
一、探究钠与过氧化钠的性质

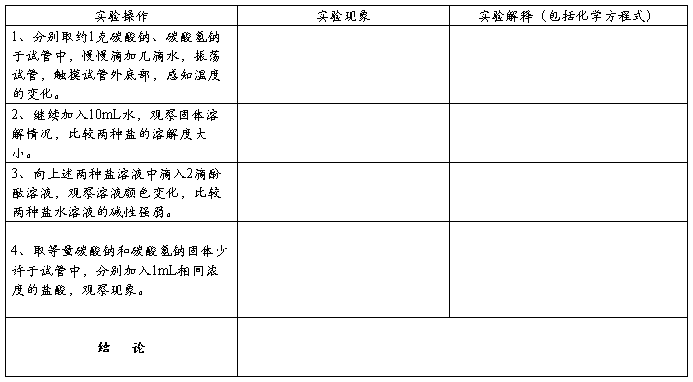
二、探究碳酸钠和碳酸氢钠的性质
三、焰色反应
1、实验操作
(1)将铂丝用稀盐酸清洗干净,再在无色火焰上灼烧至无色;
(2)蘸取试样(固体也可以直接蘸取)在无色火焰上灼烧,观察火焰颜色,从而判断试样中所含元素种类。
(3)将铂丝再用稀盐酸清洗干净,即可继续做新的实验。
注意:若检验钾元素要透过蓝色钴玻璃观察。因为多数情况下钾离子溶液中常含有钠离子,而钠元素的焰色反应为很浓的黄色,掩盖了钾元素很浅的紫色,导致无法判断)。
2、实验结果
钠元素的焰色为 ,钾元素的焰色为 ,铜元素的焰色为 。
【实验练习】
1.钠着火时,采用哪种来灭火方式最好…………………………………………………( )
A、水 B、煤油 C、泡沫灭火器 D、砂子
2.少量NaOH最好贮存在…………………………………………………………………( )
A、敞口塑料瓶中 B、玻璃塞的棕色瓶中
C、橡胶塞的广口瓶中 D、铁制容器中
3.下列关系正确的是………………………………………………………………………( )
A、还原性:Na>K B、离子半径:Na+>K+
C、热稳定性:Na2CO3>NaHCO3 D、熔点:Na<K
4.下列叙述中不正确的是…………………………………………………………………( )
A、钠在反应TiCl4+4Na=Ti+4NaCl中作还原剂
B、NaOH应密封保存,以防分解变质
C、金属锂不能保存在煤油中
D、盛放KOH溶液的试剂瓶不能用玻璃塞
5.将6g钠和3.2g硫粉迅速混合,放在石棉网上加热,反应后所得固体物质的成分是( )
A、Na2O和S B、Na2O和Na2O2 C、Na2O和Na2S D、Na2O2和Na2S
6.在实验室里做钠跟水反应的实验时,用到的仪器是…………………………………( )
a.试管夹,b.镊子,c.小刀,d.冷凝管,e.滤纸,f.研钵,g.烧杯,h.坩埚,
i.石棉网,j.玻璃片,k.药匙,l.燃烧匙
A、abdi B、cefk C、fghl D、bcegj
7.从理论上讲,Li是很活泼的金属,与水反应应当很剧烈。但事实上反应却是开始较快,一会儿就迅速缓慢起来。其原因主要是…………………………………………………( )
A、Li的密度很小,浮在水面上 B、生成物LiOH溶解度较小,附着在Li表面
C、反应开始放热而使速率变慢 D、反应产物对此反应有催化作用
8.在一定温度下,向饱和烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原温,下列说法正确的是…………………………………………………………………………( )
A、溶液中Na+浓度增大,有O2放出 B、溶液pH值不变,有H2放出
C、溶液中Na+数目减少,有O2放出 D、溶液pH值增大,有O2放出
9.下列对进行焰色反应的实验操作注意事项的说明,正确的是………………………( )
①钾的火焰颜色要透过蓝色钴玻璃观察
②先灼烧铂丝到火焰无色时,再蘸被检验物质
③每次实验后都要将铂丝蘸浓盐酸后灼烧至火焰无色为止
④实验时最好选择本身颜色较强的火焰
⑤没有铂丝可用无锈铁丝代替
A、仅③不正确 B、仅④不正确 C、④和⑤不正确 D、全部正确
10.Na2CO3是一种很重要的化学物质,某中学某学生拟在实验室中制备Na2CO3。下面是他的制备实验过程:
将50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量,生成NaHCO3,他设计了如下实验步骤:
①将50mL NaOH溶液均分为两份,各25mL;
②用第一份25mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③再小心煮沸溶液1~2分钟;
④在得到的溶液中加入另一份(25mL)NaOH溶液,使溶液充分混合。
问题:
I、在②中,刚通入CO2时发生的反应是 ;而后又发生反应 ;将以上两个反应分别改写成离子反应是 、 。
③中煮沸溶液的目的是 。
④中混合另一份NaOH溶液后发生的反应是 ,改写为离子方程式是 。
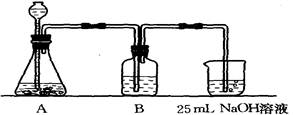 II、按该同学的设计,第②步实验装置如下:
II、按该同学的设计,第②步实验装置如下:
(1)装置A使用的试剂是 (固体)和 溶液;
(2)装置B使用的试剂最好是 (选择:水、饱和NaOH溶液、饱和Na2CO3溶液、饱和NaHCO3溶液),作用是 ,不选择其它三种试剂的原因是(简要文字说明) ;
(3)写出B中可能发生的离子方程式 ,如果不用B装置,最终得到的Na2CO3溶液中可能存在的杂质有 。
(4)有人认为实验步骤③、④顺序对调,即先混合、再煮沸更为合理,你认为对吗? 。为什么? 。
