配合物的生成和性质
一、实验目的
1、了解有关配合物的生成,配离子及简单离子的区别。
2、比较配离子的稳定性,了解配位平衡与沉淀反应、氧化还原反应以及溶液酸度的关系。
二、实验原理
由一个简单的正离子和几个中性分子或其它离子结合而成的复杂离子叫配离子,含有配离子的化合物叫配合物。配离子在溶液中也能或多或少地离解成简单离子或分子。例如:[Cu(NH3)4]2+配离子在溶液中存在下列离解平衡:
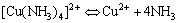
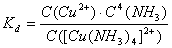
不稳定常数Kd表示该离子离解成简单离子趋势的大小。
配离子的离解平衡也是一种化学平衡。能向着生成更难离解或更难溶解的物质的方向进行,例如,在[Fe(SCN)]2+溶解中加入F-离子,则反应向着生成稳定常数更大的[FeF6]3- 配离子方向进行。
螯合物是中心离子与多基配位形成的具有环状结构的配合物。很多金属的螯合物都具有特征的颜色,并且很难溶于水而易溶于有机溶剂。例如,丁二肟在弱碱性条件下与Ni2+生成鲜红色难溶于水的螯合物,这一反应可作检验Ni2+的特征反应。
四、仪器及试剂
1、 仪器
试管、滴定管
2、 试剂
HgCl2(0.1mol·L-1)、KI(0.1 mol·L-1)、NiSO4(0.2 mol·L-1)、BaCl2(0.1mol·L-1)、NaOH(0.1mol·L-1)、1:1(NH3·H2O)、FeCl3(0.1mol·L-1)、KSCN(0.1 mol·L-1)、K3[Fe(CN)6](0.1 mol·L-1)、AgNO3(0.1mol·L-1)、NaCl(0.1 mol·L-1)、CCl4、FeCl3(0.5 mol·L-1)、NH4F(4 mol·L-1)、NaOH(2mol·L-1)、1:1H2SO4、HCl(浓)、NaF(0.1 mol·L-1)、CuSO4(0.1 mol·L-1)、K4P2O7(2 mol·L-1)、NiCl2(0.1 mol·L-1)、NH3·H2O(2 mol·L-1)、1%丁二肟、乙醚。
五、实验内容
1、配离子的生成与配合物的组成
(1)在试管中加入0.1 mol·L-1HgCl2溶液10滴(极毒!),再逐滴加入0.1 mol·L-1KI溶液,观察红色沉淀的生成。再继续加入KI溶液,观察沉淀的溶解。
反应式:HgCl2+2KI=HgI2↓+2KCl
HgI2+2KI=K2[HgI4]
(1) 在2只试管中分别加入0.2 mol·L-1NiSO4溶液10滴,然后在这2只试管中分别加入0.1 mol·L-1BaCl2溶液和0.1 mol·L-1NaOH溶液,
反应式:NiSO4+BaCl2= Ba SO4↓+NiCl2
NiSO4+2NaOH= Ni(OH)2↓+Na2SO4
在另一只试管中加入0.2 mol·L-1NiSO4溶液10滴,逐滴加入1:1NH3·H2O,边加边振荡,待生成的沉淀完全溶解后,再适当多加些氨水。然后将此溶液分成两份,分别加入0.1 mol·L-1BaCl2溶液和0.1 mol·L-1溶液。两支试管中均无现象。
反应式:NiSO4+2NH3·H2O= (NH4)2 SO4+Ni(OH)2↓
Ni2++6NH3 = [Ni(NH3)6]2+
2、简单离子和配离子的区别
在试管中加入0.1 mol·L-1FeCl3溶液,加入少量KSCN溶液,溶液变红,
方程式为:Fe3++SCN—=[Fe(SCN)]2+
以0.1 mol·L-1K3[Fe(CN)6]溶液代替FeCl3溶液做同样实验,无任何现象,
方程式为:K3[Fe(CN)6]= 3K++Fe(CN)63—
3、配位平衡的移动
(1)配位平衡与沉淀反应:
在试管中加入0.1 mol·L-1 AgNO3溶液,滴加0.1 mol·L-1NaCl溶液,观察现象;然后加入过量的氨水,观察现象,写出反应式,并解释之。
现象:有AgCl白色沉淀,加入NH3·H2O后沉淀溶解。
反应式:Ag++Cl-= AgCl ↓
AgCl+2NH3= Ag(NH3)2++Cl—
(2)配位平衡与氧化还原反应:
在试管中加入0.5 mol·L-1FeCl3溶液,滴加0.1 mol·L-1KI溶液,然后加入CCl4,振荡后观察CCl4层颜色。解释现象,并写出有关反应式。
现象:CCl4层溶入碘后变红,2Fe3++2I—=2Fe2++I2
在另一支盛有0.5 mol·L-1FeCl3溶液的试管中,先逐滴加入4 mol·L-1NH4F溶液变为无色,再加入0.1 mol·L-1KI溶液和CCl4。振荡后,观察CCl4层的颜色,解释之,并写出有关的反应式。
现象:CCl4层为无色透明溶液,无碘生成。
反应式:Fe3++6F—=FeF63—
(2) 配位平衡与介质的酸碱性 :
在试管中加入0.5 mol·L-1 FeCl3溶液10滴,逐滴加入0.4 mol·L-1NH4F溶液,呈无色。将此溶液分成两份,分别滴加2 mol·L-1NaOH溶液和1:1H2SO4溶液,观察现象,并写出有关化学反应方程式。
化学反应方程式:Fe3++6F—=FeF63—
FeF63—加入NaOH后有棕黄色絮状沉淀生成,反应方程式:
Fe3++3OH—= Fe(OH)3 ↓
FeF63—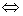 Fe3++6F— 平衡右移。
Fe3++6F— 平衡右移。
FeF63—加入H2SO4后变黄色,
F—+H+=HF FeF63—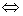 Fe3++6F— 平衡右移。
Fe3++6F— 平衡右移。
(3) 配离子的转化
往一支试管中加入2滴0.1 mol·L-1FeCl3溶液,加水稀释至无色,加入1-2滴0.1 mol·L-1KSCN溶液,再逐滴加入0.1 mol·L-1NaF溶液,观察现象并解释之。
Fe3++SCN—=[Fe(SCN)]2+
Fe3++6F—=FeF63—
[Fe(SCN)]2+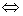 Fe3++SCN—
Fe3++SCN—
平衡右移,颜色褪去。
4、螯合物的形成
(1)往试管中加入约1mL 0.1 mol·L-1CuSO4溶液,然后逐滴加入2 mol·L-1K4P2O7溶液,先生成浅蓝色的焦磷酸铜沉淀。继续加入K4P2O7溶液,沉淀又溶解,生成深蓝色透明溶液。
2Cu2++ P2O74—= Cu 2P2O7↓
Cu2 P2O7+ P2O74—=2 CuP2O72—
(2)往试管中加入2滴0.1 mol·L-1NiCl2溶液及约1mL蒸馏水,再加入1-2滴2 mol·L-1氨水溶液,使呈碱性。然后加入2-3滴1%丁二肟溶液,观察生成的鲜红色沉淀。最后加入1mL乙醚,振荡,观察现象。
现象:鲜红色沉淀溶入乙醚溶液。
第二篇:实验十一 配合物的生成、性质与应用
实验十一 配合物的生成、性质和应用
一、实验目的
1.了解配合物的生成和组成。
2.了解配合物与简单化合物的区别。
3.了解配位平衡及其影响因素。
4.了解螯合物的形成条件及稳定性。
二、实验原理
由中心离子(或原子)与配体按一定组成和空间构型以配位键结合所形成的化合物称配合物。配位反应是分步进行的可逆反应,每一步反应都存在着配位平衡。
M + nR 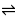 MRn
MRn 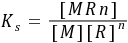 配合物的稳定性可由K稳 (即Ks)表示,数值越大配合物越稳定。增加配体(R)或金属离子(M)浓度有利于配合物(MRn)的形成,而降低配体和金属离子的浓度则有利于配合物的解离。如溶液酸碱性的改变,可能引起配体的酸效应或金属离子的水解等,就会导致配合物的解离;若有沉淀剂能与中心离子形成沉淀的反应发生,引起中心离子浓度的减少,也会使配位平衡朝离解的方向移动;若加入另一种配体,能与中心离子形成稳定性更好的配合物,则同样导致配合物的稳定性降低。若沉淀平衡中有配位反应发生,则有利于沉淀溶解。配位平衡与沉淀平衡的关系总是朝着生成更难解离或更难溶解物质的方向移动。
配合物的稳定性可由K稳 (即Ks)表示,数值越大配合物越稳定。增加配体(R)或金属离子(M)浓度有利于配合物(MRn)的形成,而降低配体和金属离子的浓度则有利于配合物的解离。如溶液酸碱性的改变,可能引起配体的酸效应或金属离子的水解等,就会导致配合物的解离;若有沉淀剂能与中心离子形成沉淀的反应发生,引起中心离子浓度的减少,也会使配位平衡朝离解的方向移动;若加入另一种配体,能与中心离子形成稳定性更好的配合物,则同样导致配合物的稳定性降低。若沉淀平衡中有配位反应发生,则有利于沉淀溶解。配位平衡与沉淀平衡的关系总是朝着生成更难解离或更难溶解物质的方向移动。
配位反应应用广泛,如利用金属离子生成配离子后的颜色、溶解度、氧化还原性等一系列性质的改变,进行离子鉴定、干扰离子的掩蔽反应等。
三、仪器和试药
仪器:试管、离心试管、漏斗、离心机、酒精灯、白瓷点滴板。
试药:H2SO4 (2mol·L-1)、HCl (1mol·L-1)、NH3·H2O (2, 6mol·L-1)、NaOH (0.1, 2mol·L-1) 、CuSO4 (0.1mol·L-1, 固体)、HgCl2 (0.1mol·L-1)、KI (0.1mol·L-1)、BaCl2 (0.1mol·L-1)、K3Fe (CN)6 (0.1mol·L-1)、NH4Fe (SO4)2 (0.1mol·L-1)、FeCl3 (0.1mol·L-1)、KSCN (0.1mol·L-1)、NH4F (2mol·L-1)、(NH4)2C2O4 (饱和)、AgNO3 (0.1mol·L-1)、NaCl (0.1mol·L-1)、KBr (0.1mol·L-1)、 Na2S2O3 (0.1mol·L-1,饱和)、Na2S (0.1mol·L-1)、FeSO4 (0.1mol·L-1)、NiSO4 (0.1mol·L-1) 、CoCl2 (0.1mol·L-1)、CrCl3 (0.1mol·L-1)、EDTA (0.1mol·L-1)、乙醇 (95%)、CCl4、邻菲罗啉 (0.25%)、二乙酰二肟(1%)、乙醚、丙酮。
四、实验内容
1.配合物的生成和组成
(1)配合物的生成
在试管中加入0.5g CuSO4·5H2O (s), 加少许蒸馏水搅拌溶解,再逐滴加入2mol·L-1的氨水溶液,观察现象,继续滴加氨水至沉淀溶解而形成深蓝色溶液,然后加入2mL 95%乙醇,振荡试管,有何现象?静置2分钟,过滤,分出晶体。在滤纸上逐滴加入2 mol·L-1NH3·H2O溶液使晶体溶解,在漏斗下端放一支试管承接此溶液,保留备用。写出相应离子方程式。
(2)配合物的组成
将上述溶液分成2份,在一支试管中滴入2滴0.1mol·L-1BaCl2溶液,另一支试管滴入2滴0.1mol·L-1NaOH溶液,观察现象,写出离子方程式。
另取两支试管,各加入5滴0.1mol·L-1CuSO4溶液,然后分别向试管中滴入2滴0.1mol·L-1 BaCl2溶液和2滴0.1mol·L-1NaOH溶液,观察现象,写出离子方程式。
比较二实验结果,分析该配合物的内界和外界组成,写出相应离子方程式。
2.配合物与简单化合物、复盐的区别
(1)在一支试管中加入10滴0.1mol·L-1FeCl3溶液,再滴加2滴0.1mol·L-1KSCN溶液,观察溶液呈何颜色?
(2)用0.1mol·L-1K3Fe(CN)6)溶液代替FeCl3溶液,同法进行实验,观察现象是否相同。
(3)如何用实验证明硫酸铁铵是复盐,请设计步骤并实验之。
提示:取3支试管,各加入5滴0.1mol·L-1NH4Fe(SO4)2溶液,分别用相应方法鉴定NH4+、Fe3+、SO4 2-的存在。
3.配位平衡及其移动
(1)配位平衡
在3支各加入少量自制的硫酸四氨合铜溶液的试管中,分别滴加2滴0.1mol·L-1BaCl2溶液、2滴0.1mol·L-1NaOH溶液、2滴0.1mol·L-1Na2S溶液,观察现象,说明原因。
(2)配合物的取代反应
在一支试管中,加入10滴0.1mol·L-1FeCl3溶液和1滴0.1mol·L-1KSCN溶液,观察溶液颜色。向其中滴加2mol·L-1NH4F溶液,溶液颜色又如何?再滴入饱和 (NH4)2C2O4溶液,溶颜色又怎样变化?简单解释上述现象,并写出离子方程式。
(3)配位平衡与酸碱平衡
①取2支试管,各加入少量自制的硫酸四氨合铜溶液,一支逐滴加入1mol·L-1HCl溶液,另一支滴加2mol·L-1NaOH溶液,观察现象,说明配离子[Cu(NH3)4]2+在酸性和碱性溶液中的稳定性,写出有关的离子方程式。
②在一支试管中,先加入10滴0.1mol·L-1FeCl3溶液,再逐滴滴加2mol·L-1NH4F溶液至溶液颜色呈无色,将此溶液分成两份,分别逐滴加入1mol·L-1HCl和2mol·L-1NaOH溶液,观察现象,说明配合物离子[FeF6]3-在酸性和碱性溶液中的稳定性,写出有关的离子方程式。
(4) 配位平衡与沉淀平衡
在一支离心试管中加入2滴0.1mol·L-1AgNO3溶液,按下列步骤进行实验:
①逐滴加入0.1mol·L-1NaCl溶液至沉淀刚生成;
②逐滴加入6mol·L-1氨水至沉淀恰好溶解;
③逐滴加入0.1mol·L-1KBr溶液至刚有沉淀生成;
④逐滴加入0.1mol·L-1Na2S2O3溶液,边滴边剧烈振摇至沉淀恰好溶解;
⑤逐滴加入0.1mol·L-1KI溶液至沉淀刚生成;
⑥逐滴加入饱和 Na2S2O3溶液,至沉淀恰好溶解;
⑦逐滴加入0.1mol·L-1Na2S溶液至沉淀刚生成;
写出每一步有关的离子方程式,比较几种沉淀的溶度积大小和几种配离子稳定常数大小讨论配位平衡与沉淀平衡的关系。
(5) 配位平衡与氧化还原反应
取两支试管各加5滴0.1mol·L-1的FeCl3溶液及10滴CCl4,然后往一支试管滴入2mol·L-1 NH4F溶液至溶液变为无色,另一支试管中滴入几滴蒸馏水,摇匀后在两支试管中分别再滴入5滴0.1mol·L-1KI溶液,振荡后比较两试管中CCl4层颜色,解释现象并写出离子方程式。
4.配合物的活动性
取一支试管加入10滴0.1mol·L-1的CrCl3和2mL 0.1mol·L-1 EDTA溶液,摇匀,是否有配合物生成,将溶液加热,观察现象并解释。
5.配合物的水合异构现象
(1)取一支试管加入0.5mL 0.1mol·L-1的CrCl3溶液,加热,观察溶液颜色变化,然后将溶液冷却,观察现象并解释。
反应方程式如下:[Cr(H2O)6]3++2Cl- 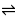 [Cr(H2O)4Cl2]+ +2H2O
[Cr(H2O)4Cl2]+ +2H2O
(2)取一支试管加入0.5mL 0.1mol·L-1CoCl2溶液,加热,观察溶液颜色变化,然后将溶液冷却,观察现象并解释。反应方程式如下:[Co(H2O)6]2++4Cl-  [Co(H2O)2Cl4]2- + 4H2O
[Co(H2O)2Cl4]2- + 4H2O
6.配合物的应用
(1)取两支试管各加10滴自制的[Fe(SCN)6] 3-、[Cu(NH3)4]2+,然后分别滴加0.1mol·L-1 EDTA溶液,观察现象并解释。
(2)在小试管中(或白瓷点滴板上),滴加一滴0.1mol·L-1FeSO4溶液及3滴0.25%邻菲罗啉溶液,观察现象,此反应可作为Fe2+离子的鉴定反应。
(3)在试管中加入2滴0.1mol·L-1NiSO4溶液及一滴2mol·L-1NH3·H2O和2滴二乙酰二肟溶液,观察现象,此反应可作为Ni2+离子的鉴定反应。
(4)在鉴定和分离离子时,常常利用形成配合物的方法来掩蔽干扰离子。例如Co2+和 Fe3+共存时,采用NH4F来掩蔽Fe3+,不需分离即可用KSCN法鉴定Co2+。
在一支试管中加入2滴0.1mol·L-1CoCl2溶液和几滴1mol·L-1 KSCN,再加一些戊醇(或丙酮),观察现象。
在一支试管中加入1滴0.1mol·L-1的FeCl3溶液和5滴0.1mol·L-1的CoCl2溶液,加几滴1 mol·L-1KSCN,有何现象?逐滴加入2mol·L-1的NH4F溶液,并振摇试管,观察现象;等溶液的血红色褪去后,加一些戊醇(或丙酮),振摇,静置,观察戊醇层颜色。
7.请思考一下利用现有的试剂还可以生成其它的配合物吗? 动手试试吧!
五、注意事项
1.在性质实验中一般来说,生成沉淀的步骤,沉淀量要少,即刚观察到沉淀生成就可以;使沉淀溶解的步骤,加入试液越少越好,即使沉淀恰好溶解为宜。因此,溶液必须逐滴加入,且边滴边摇,若试管中溶液量太多,可在生成沉淀后,离心沉降弃去清液,再继续实验。
2.NH4F试剂对玻璃有腐蚀作用,储藏时最好放在槊料瓶中。
3.注意配合物的活动性是指配合物在反应速度方面的性能。Cr-EDTA配合物的稳定性相当高(lgKs = 21),但反应速度较慢。在室温下很少发生反应,必须在EDTA过量且加热煮沸下才能形成相应配合物。
六、思考题
1.试总结影响配位平衡的主要因素。
2.配合物与复盐的区别是什么?
3.实验中所用EDTA是什么物质?它与单基配体相比有何特点?
4.为什么Na2S不能使K4Fe(CN)6产生FeS沉淀,而饱和的H2S溶液能使[Cu(NH3)4]2+溶液产生CuS沉淀?
