����ͭ�����нᾧˮ�����IJⶨ
[���˼��]
��ѧ��ͨ������ͭ�ᾧˮ�����IJⶨʵ�������ѧϰ������ƽ����������������ʹ�÷�����������ܣ�ѧϰС����ȡ����ز��������������Ͻ���ϸ�¡����渺���̬�ȶ�����ʵ�����Ҫ�ԡ���ѧ�ص����ѧ���IJ��������ϣ���ʦ��Ҫͨ��Ѳ��ָ��������ѧ��ѧϰ��������������ΪʲôҪ��������������ÿһ�����������壬�����������IJ�����������̡�
һ����ѧĿ��
1��֪ʶ�뼼��
������ƽ�����������в����������������IJ������ܣ��Լ����ز������ܣ�C����
2�������뷽��
��1��ͨ��ʵ���������ʶ�۲졢������ʵ�������Ŀ��ơ����ݴ����ȿ�ѧ������
��2��ͨ��ʵ�鱨�����д����ʶ��дʵ�鱨���һ��Ҫ�淶�뷽����
3�����̬�����ֵ��
ͨ��ʵ�����������ʵ�����ǡ��������桢һ˿�����Ŀ�ѧ̬�ȶ�ʵ������塣
������ѧ�ص���ѵ�
1����ѧ�ص�
�����������ز�����
2����ѧ�ѵ�
ʵ�������Ŀ��ơ����ݴ�����
������ѧ��Ʒ
ҩƷ��CuSO4·xH2O
������������ƽ���в��������������żܡ������ǡ�������������ǯ�����������ƾ��ơ�ҩ�ס�
ý�壺��ѧʵ���ң�����һ�飩
�ģ���ѧ����
1������ͼ
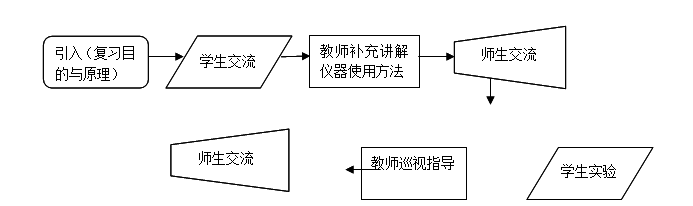



2������˵��
���룺���ڿΣ�������Ҫ����ͨ��ʵ�ʲ��������ղⶨ����ͭ����ᾧˮ�����ķ����Լ�������ʹ�á��ڲ���ǰ������ͬѧ�ǻ���ⶨ����ͭ����ᾧˮ����ԭ������˼����ʵ���Ŀ����ʲô����Ҫ��Щʵ����Ʒ��
ѧ��������ʵ��ԭ��������ͭ������ȵ�150������ʱ��ȫ��ʧȥ�ᾧˮ�����ݼ���ǰ����������������侧��Ľᾧˮ�������ȵȡ�
���佲�⣺������ƽ���в�����������������ʹ�÷����ͼ��ȡ����صȻ�������Ҫ�㡣
ʦ����������ʦ��ʾ�в�����ƽ�����ᡢ����������������ѧ��ģ����ϰ��
ʵ������� ѧ�������в���ʵ�飬��ĥ���������ٳơ����� �� �ٳ� ���ټ��� �� �ٳ��ء����㡣
Ѳ��ָ���� ��ǰ��ϸ����Ϊʲô��С����ȡ���Ϊʲô���ڸ���������ȴ����Ϊʲô���ܲ������Թܴ��������������ɣ�����Ҫ��ֵ�������ͷ������ԭ�ȵȡ�
ʦ����������Щ�������ܻ�����ʵ����
��ҵ����1����дʵ�鱨�档��2������������������������ã��ᾧˮ���뾧�������ᾧˮʵ�ʺ�����Ƚϣ���ƫ��ƫС������û��Ӱ�죿
�壮��ѧ����
1����ѧ����

2����Ҫ����
ʵ��� ����ͭ�����нᾧˮ�����IJⶨ
һ��ʵ��Ŀ��
����ʵ��ԭ��
����ʵ����Ʒ
�ġ���������������
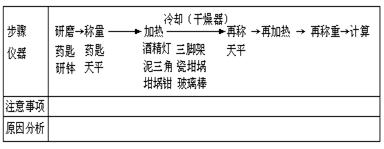
�塢������
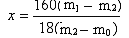
3���������
1 ��ѧ��ѧ��ʦ�ֲ� �Ϻ�����������
2 http://xiaohe.heyma.net
������ѧ��˼
ͨ������ͭ�ᾧˮ�����IJⶨʵ�飬ѧ���Ӹ��Է����������ʵ����ʺͱ仯���ɵ����⣻ѧ������ĥ�����ȡ�����������ȴ�����ز�����ʵ����������ʵ�������ȷ���Բⶨ����кܴ�Ӱ�����ʶ�������Ͻ���ϸ�¡����渺���̬�ȶ�����ʵ�����Ҫ�ԣ������ʵ�����ǡ��������桢һ˿�����Ŀ�ѧ̬���뾫�����ʶ��
���ڱ��ڿ�����ʵ�����ѧ���Լ�����ʵ�飬��ˣ���ѧ�н�ʦҪ���ع۲졢ָ��ѧ����ʵ��������̣�����ѧ���γ����õ�ʵ��ϰ�ߡ����渺��Ŀ�ѧ����
�ڶ�ƪ��ʵ��һ����ͭ������ᾧˮ�����IJⶨ
ʵ��һ ����ͭ������ᾧˮ�����IJⶨ
���ѧĿ��
1.ѧϰ�ⶨ������ᾧˮ�����ķ�����
2.������ƽ��ʹ�á�
3.��ϰ������ʹ�ã�����ѧ����ĥ������
���ѧ�ص�
1.�ⶨ����ͭ�����нᾧˮ������ԭ����
2.�ⶨ����ͭ�����нᾧˮ�����IJ������衣
��ڿΣ����ǽ�ѧϰͨ������ijЩ���ݣ��Ӷ��ⶨ�������нᾧˮˮ������
��������������ʶ�������塣
�������
�۽�ʦչʾ����ͭ�������ˮ����ͭ��ĩ��
�۽��ܣݴ�����ڿ����ķֱ�������ͭ�������ˮ����ͭ��
���ʣݣ������кβ�ͬ��
����������ͭ����Ϊ��ɫ���׳Ƶ������������仯ѧʽΪ������ˮ����ͭΪ��ɫ��ĩ���仯ѧʽΪ����������ˮ����ͭ�Dz�ͬ�����ʡ������������տ����е�ˮ����������ѧ��Ӧ��������ͭ���塣
���ʣݴӻ�ѧ����Ͽ�����ʲôԭ������˶��ߵ���ɫ����أ�
����������Ҫ����������ͭ�����к��нᾧˮ֮�ʡ�
���ʣ�����֤������ͭ�������нᾧˮ��
��ʦ�������û�ѧ����ʽ��ʾ������ת����
����һλͬѧ�Ϻڰ���д��
���������ˮ����ͭ��ĩ���Ƿ�� �нᾧˮ������
��ѧ���ݰ����
CuSO4·5H2O CuSO4+5H2O
CuSO4+5H2O
��ѧ���Ѿ��ⶨ1mol�����к���5mol�ᾧˮ���������Dz�֪��������ۣ���ô���Ǹ���βⶨ1mol�����к��м�mol�ᾧˮ�أ�
��Ϊ����ͭ�����нᾧˮ�����������軯ѧʽΪ��
�۲ݰ����CuSO4·xH2O
��Ȼ��ֻҪ���X��ֵ��֪��1mol����ͭ�����к���Ħ���ᾧˮ�ˡ�
��ϵ����������ʧˮ�ķ�Ӧ����ʽ��X��ֵ��������Щ�����й�ϵ��ˮ������ͭ������
��ʵ�������������ܲ�����ֻ�ܲ������������
ͨ���ⶨ��Щ�����Լ���ˮ������ͭ��������
��β����ˮ����ͭ�������Լ��ᾧˮ��������
ѧ��˼��
һ���ⶨԭ��
��ѧ�����ۺ�ش������ȡһ�����ľ�����Ʒ�����ȣ�ʹ��ʧȥȫ���ᾧˮ��Ȼ���ٳ�һ��ʧȥ�ᾧˮ�������ͭ��ĩ��������ǰ�����ε������Ϊ�ᾧˮ�����������ݽᾧˮ��������ԭ����������ȼ�����ýᾧˮ�����������ͪ�x��ֵ��
��ʦ�ݺܺã������ⶨԭ�����ǿɼ�ʾ���£�
�۽��Ⲣ�����CuSO4·nH2O CuSO4+nH2O
CuSO4+nH2O
�������IJ���ʵ������ԭ����
���� ------ ���� ------------����
�ڼ�������ͭ����ʱ������������Ȳ����������ᷢ������ͭ����ɽ��������
��ô��β��ܱ�������ͭ���Ȳ����������� ���ڼ���ǰ��ĥ��
�ڳ�����ˮ����ͭ������ǰ�����뱣֤�ᾧˮ�Ѿ���ȫʧȥ����ô�жϽᾧˮ��ȫʧȥ��ѧ���ش�
���ز���
�Ķ�;ʲô�Ǻ��ز�����Ϊʲô���ز����ܱ�֤�ᾧˮ��ȫʧȥ��
�ܷ�ͨ���ӳ�����ʱ������֤�ᾧˮ��ȫʧȥ��
������ͭ������ȫ�����ˮ����ͭ�������¶Ⱥܸߣ�����ֱ����������������
�ڲⶨ��ˮ����ͭ������֮ǰ����������Σ�
����ȴ��ˮ����ͭ��ʱ����ˮ����ͭ������ˮ�ֱ������ͭ���塣��������ȴʱ��������ʲô��
����ˮ����
���ڣ����Ҹ��ݲⶨ����ͭ����ᾧˮ������ԭ�����������ע������������ۣ���Ƴ�һ��������ʵ�鷽����
1.��ĥ����ͭ���� :2.��������������������ͭ������������
3.��������ͭ����ͬʱ�ò����������������ͭ���壬ֱ����ɫ����ͭ������ȫ��ɰ�ɫ��ĩ���Ҳ�����ˮ�����ݳ�����
4.��ȴ��Ȼ���������ڸ���������ȴ
5���� �������ڸ���������ȴ������������ƽ�ϳ�����������������ˮ����ͭ����������m2����
6.�ټ�����ȴ���� ��ʢ����ˮ����ͭ�������ټ��ȣ�Ȼ����ڸ���������ȴ���ٳ������������������������γ��������������0.1 gΪֹ��
7.���� ����ʵ�����ݼ�������ͭ������ᾧˮ�����������ͻ�ѧʽ��x��ʵ��ֵ��
ÿһ��������Ҫ��Щ������
������������ƽ�������и�ʴ�Ե�ҩƷ��Ӧ���ڲ�����������������ܳ����ȵ���Ʒ������ȴ�����³�������
���ʣ���Ҫ������Щ�Ϳ����Ӵ��ױ��ʻ�����ˮ����Ʒʱ����Ҫע��ʲô��
��ѧ���ش��Ҫʹ���������㹻�졣
���ȣ�չʾ�ձ����Թܣ��ĸ���ã����ɡ� ����
�۽����������һ�ֿ�ֱ���������ȵ��������ܳ��ܽϸߵ��¶ȣ��������żܺ�����������ʹ�á�ȡ��������ʱ��Ҫ������ǯ����������ע�ⲻ������ȥ�������ȵ�����
������������Ҫ���衣
����
Ϊʲô��ͬ��
��Щ��������ʹ���������
�۽�ʦ����ʵ�ϣ�����ʵ�����õ�����ͭ���壬������ˮ������ͭ��CuSO4·5H2O����
���ڣ����Ҹ�������ͭ����Ļ�ѧʽ����ᾧˮ��������������ʵ��ⶨ�Ľ������ݻ�ѧʽ����Ľ�����жԱȣ�������ʵ����
��ѧ�����
�۽�ʦ���������ʵ��������
�۸�С��ͬѧ�����Լ��ļ�������
��ʦ�����Ҷ��Լ���ʵ����������������
��ѧ���������ۣ����������۽�����н�����
�۽�ʦ�ܽ�ݶ��ڶ���ʵ����ԣ�ÿһ����������ȷ���ֱ��Ӱ����ʵ������ȷ�ԡ��ɸղŴ�ҵ����۽����֪���ڲ��������У�������ͭ������ˮ����ֻ�Ӹ��������ó��������������ʱ������ɲⶨ�����ƫС�����ڼ��ȹ�����������ͭ���������ʢ����ͭ���������Ԥ��δ�����������ʵ������ƫ�����⣬��ƽʹ�û������ȷ��Ҳ�����ʵ����
��ͶӰ��ϰ��
����ʵ�����вⶨ����ͭ����ᾧˮ������ʵ�飬��д���пհף�
(1)������������ѡ����������(�ñ����ĸ��д) ��
A.������ƽ(������) B.�в� C.�Թܼ� D.�ƾ��� E.������ F.������ G.����
H.������ I.ʯ���� J.���ż�
�����������⣬����Ҫ�������ǣ� ��
(2)ijѧ��ʵ���õ��������ݣ�

��д���ᾧˮ����(x%)�ļ��㹫ʽ(��W1��W2��W3��ʾ)
x%�� ��
�����ⶨ�����ƫ����ƫ��?____________��
�����з�����ѡ����ѧ������ʵ������ԭ�������(��д��ĸ)____________
A.����ǰ����ʱ����δ��ȫ����
B.������μ��Ⱥ��������ϴ�(����0.1 g)
C.���Ⱥ�����δ�������������ȴ
D.���ȹ�������������ʧ
