实验四 铵盐中氮含量的测定(甲醛法)
重点:容量瓶的使用;NaOH标液的配制和标定;甲醛法测定氨态氮的原理和操作方法;试验结果的记录和铵盐的含氮量计算。
难点:弱酸强化的基本原理;酸碱指示剂的选择原理和指示剂突变的判断。
一、 实验目的
1、掌握甲醛法测定铵盐中氮含量的基本原理
2、复习滴定及称量操作
二、实验原理
铵盐NH4Cl和(NH4)2SO4是常用的氮肥,系强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),故无法用NaOH标准溶液直接滴定。生产和实验室中广泛采用甲醛法测定铵盐中的含氮量。甲醛法是基于如下反应:
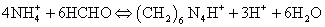
生成的H+和(CH2)6N4H+(Ka=7.1×10-6)可用NaOH标准溶液滴定,计量点时产物为(CH2)6N4,其水溶液显微碱性,可选用酚酞作指示剂。
三、仪器和试剂
邻苯二甲酸氢钾(KHP)分析纯;酚酞2g·L-1乙醇溶液;甲基橙1 g·L-1水溶液;(NH4)2SO4;0.1mol·L-1NaOH标准溶液(同实验3);40%甲醛;甲基红2g·L-1乙醇溶液。
四、实验内容
1.配制0.1mol.L-1NaOH500mL(称取2gNaOH配制成500mL溶液)。
2.将称量瓶洗涤并烘干,称取0.4~0.5g邻苯二甲酸氢钾三份分别放于锥形瓶中。
3.将称量得到的邻苯二甲酸氢钾用20-30mL水温热溶解,冷却后,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至溶液呈微红色,半分钟内不褪色,即为终点。
4.称取0.10~0.20g(NH4)2SO4 三份于锥形瓶中。
5.将称量得到的(NH4)2SO4用20-30mL水溶解后,加入5mL中性甲醛溶液,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至淡红色,半分钟内不变色,即为终点。
五、数据记录及处理
1.数据记录表格
2. 含氮量的计算
含氮量N%=CNaOH×VNaOH×M(N)×100%/m
六、注意事项
1.如果铵盐中含有游离酸,应事先中和除去,先加甲基红指示剂,用NaOH溶液滴定至溶液呈橙色,然后再加入甲醛溶液进行测定。
2.甲醛中常含有微量甲酸,应预先以酚酞为指示剂,用NaOH溶液中和至溶液呈淡红色。
3.滴定中途,要将锥形瓶壁的溶液用少量蒸馏水冲洗下来,否则将增大误差。
七、实验讨论
1、铵盐中氮的测定为何不采用NaOH直接滴定法?
答:铵盐NH4Cl和(NH4)2SO4是常用的氮肥,系强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),用NaOH标准溶液直接滴定,在滴定曲线上已无明显突跃,此时反应的完全程度很低,难以用指示剂来确定滴定终点。故不采用NaOH标准溶液直接滴定。
2、为什么中和甲醛试剂中的甲酸以酚酞作指示剂;而中和铵盐试样中的游离酸则以甲基红作指示剂?
答:选择指示剂是根据滴定终点溶液的酸碱性和指示剂的变色范围来决定的。酚酞指示剂的变色范围是8.0-9.6,甲基红指示剂的变色范围是4.4-6.2,中和铵盐试样中的游离酸时其滴定终点溶液显酸性,中和甲醛试剂中的甲酸时其滴定终点溶液显弱碱性,所以,中和甲醛试剂中的甲酸以酚酞作指示剂;而中和铵盐试样中的游离酸则以甲基红作指示剂。
3. NH4HCO3中含氮量的测定,能否用甲醛法?
答:不能用甲醛法测定。
NH4HCO3是弱酸弱碱盐,在水中的水解常数K=KW/(Ka×Kb)=1.31×10-3,因为Ka<Kb,溶液显碱性,可以加入1-2滴甲基橙,用0.1mol.L-1HCl溶液滴定溶液由黄色至橙色,加入5ml中性甲醛溶液,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至淡红色,半分钟内不变色。
第二篇:实验四 NaOH标准溶液浓度的标定、铵盐中铵态氮量的测定(甲醛法)
上一次实验(滴定分析基本操作练习)的问题:
1. 思考题:锥形瓶不需要先用该溶液润洗或烘干主要是因为它不会改变该溶液的物质的量。
2. 讨论:应该就实验过程中出现的现象、情况和实验结果进行讨论。讨论并不是思考题。例如可对相对平均偏差过大进行讨论分析,对使用不同指示剂时导致VHCl / VNaOH的比值有点差别,等等。
3. 不论是用NaOH溶液滴定HCl 还是HCl溶液滴定NaOH VHCl / VNaOH或VNaOH/ VHCl是一个不变的值,
4. 有效数字的保留。(比值保留四位有效数字,相对平均偏差要求保留两位有效数字)
5. 数据处理时表格设计要科学合理。
6. 实验步骤要简洁易懂。
实验三. NaOH标准溶液浓度的标定
铵盐中氮含量的测定(甲醛法)
一. 实验原理:
1. 碱标准溶液常用NaOH 或KOH来配制,由于固体NaOH 和KOH易吸收空气中的CO2和水分,因此常用间接法来配制,即先配制近似浓度,然后用基准物质(草酸H2C2O4、邻苯二甲酸氢钾KHP)来标定。
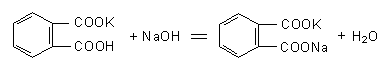
化学计量点:pH=9.1
指示剂:酚酞
终点颜色:无色→ 微红色

 计算:CNaOH/mol L-1=( )KHP/VNaOH×10-3 其中:MKHP=204.2
计算:CNaOH/mol L-1=( )KHP/VNaOH×10-3 其中:MKHP=204.2
2. (NH4)2SO4是一种氮肥,它和(NH4)2CO3,NH4Cl一样,肥效的高低重要取决于其含氮量,因此测定铵态肥的肥效,实际上就是测定以NH4+的形式存在的氮。(NH4)2SO4是强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),不满足cKa≥10-8故无法用NaOH标准溶液直接滴定,必须进行强化。生产和实验中广泛使用甲醛法测定铵盐中氮的含量。
4NH4++6HCHO (CH2)6N4H++3H++6H2O (4-1)
(CH2)6N4H++3H++6H2O (4-1)
生成的H+和(CH2)6N4H+(Ka=7.1×10-6)可用NaOH标准溶液直接滴定
(CH2)6N4H++3H++4OH-=(CH2)6N4+4H2O (4-2)
化学计量点时,产物是(CH2)6N4(Kb=10-9),其水溶液显微碱性(pKb=9),可选用酚酞作指示剂。终点颜色变化:无色→浅红色
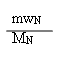 甲醛法准确度较差,但比较快速,故生产上用得较多。如果试样中含有Fe3+,影响终点观察,可改用蒸馏法。
甲醛法准确度较差,但比较快速,故生产上用得较多。如果试样中含有Fe3+,影响终点观察,可改用蒸馏法。
由(4-1)和(4-2)可知NH4+~ N~ OH-,所以 = cVNaOH×10-3

故wN= ×100%
其中c= ,MN=14.01
二.仪器与试剂:电子天平,滴定管,锥形瓶,容量瓶,移液管,量筒;NaOH,KHP,;(NH4)2SO4样品,酚酞指示剂,(1:1)甲醛
三.试验步骤
(一) NaOH溶液浓度的标定:称KHP 0.4-0.5g至锥形瓶中→加入20-30mL水溶解→加入1-2滴酚酞→用待标的NaOH溶液来滴定至微红色,30s不褪色,即终点→记录数据。(平衡三份)
(二)铵盐中氮含量的测定:
1. 甲醛的处理:(已经处理好,可直接取用)
2. (NH4)2SO4样品中游离酸的处理:这一步可不做,我们的样品基本不含有游离酸。
3. 测定:称取样品0.8~1.0g→小烧杯中→加水溶解→转移至100mL容量瓶中→定容至刻度→摇匀。吸取样液20.00mL→锥形瓶中→加入8mL中性甲醛→摇匀→放置1min→加入2d酚酞→用NaOH标液滴定至微红色且30s不褪色,即为终点。平衡三份。
四. 原始数据和结果
1. NaOH溶液浓度的标定

2. 铵盐中氮含量的测定
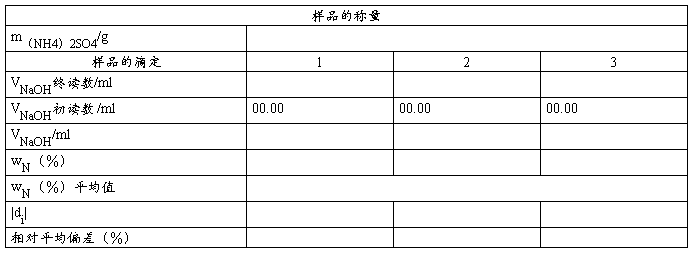
五. 注意事项
1. 电子天平的使用和滴定管的洗涤
2. 读数、记数应注意有效数字的保留。
3. 称量基准物时一般采用递减称量的方法。
4. 滴定管调零前应该把其他事宜准备好,调零后马上开始滴定,滴定后马上读数,防止因滴定管漏液而造成的读数误差。
4.
5. 甲醛预处理,除去甲醛中的游离酸(如甲酸)。如未中和,测定结果会偏高;如中和过量,则测定结果偏低。
6. 如果样品(NH4)2SO4要处理以除去游离酸,则要先加入甲基红指示剂,用NaOH溶液滴定至橙色,然后再加入甲醛进行测定。这时溶液的颜色变化为:微红→浅黄色→橙红(微红→浅黄色是甲基红颜色的变化,加入酚酞,用NaOH继续滴定,终点颜色是甲基红的黄色和酚酞的红色的混合色,故呈橙红色。)
7. 转移样液时,注意不要滴到外面。
8. 注意静置,使其反应完全。
六.思考题:P64-65:1、3、4中任选2题;P65-66任选两题
七.讨论

