实验三 硫酸铵肥料中含氮量的测定(甲醛法)
【实验目的】
1. 了解弱酸强化的基本原理
2. 掌握甲醛法测定氨态氮的原理和操作方法。
3. 熟练掌握酸碱指示剂的选择原理。
【实验原理】
1、NaOH标准溶液的标定
用基准物质(邻苯二甲酸氢钾,草酸)准确标定出NaOH溶液的浓度
⑴ 邻苯二甲酸氢钾:优点:易制得纯品,在空气中不吸水,易保存,摩尔质量大,与NaOH反应的计量比为1:1。
KHC8H4O4在100~125℃下干燥1~2h后使用。
化学计量点时,溶液呈弱碱性(pH≈9.20),可选用酚酞作指示剂。
⑵ 草酸 H2C204﹒2H2O: A.在相对湿度为5%~95%时稳定(能否放置在干燥器中保存?)。B.用不含CO2的水配制草酸溶液,且暗处保存。 注意:光和Mn2+能加快空气氧化草酸,草酸溶液本身也能自动分解。
滴定反应为: H2C2O4 + 2NaOH = Na2C2O4 + 2H2O
化学计量点时,溶液呈弱碱性(pH≈8.4),可选用酚酞作指示剂。
本实验所用基准物为邻苯二甲酸氢钾。
2.铵盐中氮含量的测定:
硫酸铵是常用的的氮肥之一,是强酸弱碱盐,可用酸碱滴定法测定其含氮量。但由于NH4+的酸性太弱(Ka=5.6×10-10),不能直接用NaOH标准溶液准确滴定,生产和实验室中广泛采用甲醛法进行测定。
将甲醛与一定量的铵盐作用,生成相当量的酸(H+)和质子化的六次甲基四铵盐(Ka=
7.1×10-6),反应如下:
4NH4+ + 6HCHO = (CH2)6N4H+ + 3H+ + 6H2O
生成的H+和质子化的六次甲基四胺(Ka=7.1×10-6),均可被NaOH标准溶液准确滴定(弱酸NH4+被强化)。
(CH2)6N4H++3H++4NaOH = 4H2O + (CH2)6N4 + 4Na +
4mol NH4+ 相当于4mol的 H+ 相当于4mol的 OH- 相当于4mol的 N。所以氮与NaOH 的化学计量数比为1。
化学计量点时溶液呈弱碱性(六次甲基四胺为有机碱),可选用酚酞作指示剂。
终点:无色→微红色(30s内不褪色)
注意:(1)若甲醛中含有游离酸(甲醛受空气氧化所致,应除去,否则产生正误差),应事先以酚酞为指示剂,用NaOH溶液中和至微红色(pH≈8)。 (2)若试样中含有游离酸(应除去,否则产生正误差),应事先以甲基红为指示剂,用NaOH溶液中和至黄色(pH≈6)(能否用酚酞指示剂?)。本实验用(NH4)2SO4试剂,不含游离酸,故不需要此步处理。
【实验步骤】
1. 配制0.1 mol/L NaOH溶液(P164——第四版;P99-第五版)
2.0.1mol·L-1 NaOH溶液的标定
用差减法准确称取0.4~0.6g已烘干的邻苯二甲酸氢钾三份,分别敲入三个已编号的250mL锥形瓶中,加40~50mL水溶解(可稍加热以促进溶解)——2~3d酚酞——用NaOH溶液滴定——微红色(30S内不褪)——记录VNaOH,计算C NaOH和标定结果的相对偏差(应小于或等于±0.2%,否则需重新标定。
3. 甲醛溶液的处理
取原装甲醛(40%)的上层清液20mL于烧杯中,用水稀释一倍,加入2~3滴0.2%的酚酞指示剂,用0.1 mol/L的NaOH 溶液中和至甲醛溶液呈微红色。(要不要记录VNaOH?)
4. 试样中含氮量的测定
准确称取2-3 g的(NH4)2SO4于小烧杯中,用适量蒸馏水溶解,定量地转移至250 mL 容量瓶中,用蒸馏水稀释至刻度,摇匀。
用移液管移取试液25.00 mL于250 mL锥形瓶中,加入10mL已中和的(1:1)甲醛溶液,再加入1~2滴酚酞指示剂摇匀,静置一分钟后(强化酸),用0.1 mol/L NaOH 标准溶液滴定至溶液呈微红色,并持续30s不褪,即为终点。记录滴定所消耗的NaOH 标准溶液的读数,平行做3次。根据NaOH 标准溶液的浓度和滴定消耗的体积,计算试样中氮的含量和测定结果的相对偏差。
【实验结果及数据处理】
表1 0.1 mol/L NaOH溶液的标定
记录项目
KHC8H4O4质量(g)
消耗NaOH溶液体积VNaOH/mL
CNaOH / mol/L
1 2 3
表2 硫酸铵中含氮量的测定(甲醛法) 项目
m(试样)(g) (NH4)2SO4溶液总体积(mL) 滴定时移取V(NH4)2SO4(mL)
CNaOH (mol·L-1) VNaOH(mL)
试样的含氮量(%)
含氮量的平均值(%) 相对标准偏差
1 2 3
第二篇:实验四 铵盐中含氮量的测定(甲醛法)
实验四 铵盐中氮含量的测定(甲醛法)
重点:容量瓶的使用;NaOH标液的配制和标定;甲醛法测定氨态氮的原理和操作方法;试验结果的记录和铵盐的含氮量计算。
难点:弱酸强化的基本原理;酸碱指示剂的选择原理和指示剂突变的判断。
一、 实验目的
1、掌握甲醛法测定铵盐中氮含量的基本原理
2、复习滴定及称量操作
二、实验原理
铵盐NH4Cl和(NH4)2SO4是常用的氮肥,系强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),故无法用NaOH标准溶液直接滴定。生产和实验室中广泛采用甲醛法测定铵盐中的含氮量。甲醛法是基于如下反应:
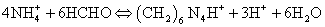
生成的H+和(CH2)6N4H+(Ka=7.1×10-6)可用NaOH标准溶液滴定,计量点时产物为(CH2)6N4,其水溶液显微碱性,可选用酚酞作指示剂。
三、仪器和试剂
邻苯二甲酸氢钾(KHP)分析纯;酚酞2g·L-1乙醇溶液;甲基橙1 g·L-1水溶液;(NH4)2SO4;0.1mol·L-1NaOH标准溶液(同实验3);40%甲醛;甲基红2g·L-1乙醇溶液。
四、实验内容
1.配制0.1mol.L-1NaOH500mL(称取2gNaOH配制成500mL溶液)。
2.将称量瓶洗涤并烘干,称取0.4~0.5g邻苯二甲酸氢钾三份分别放于锥形瓶中。
3.将称量得到的邻苯二甲酸氢钾用20-30mL水温热溶解,冷却后,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至溶液呈微红色,半分钟内不褪色,即为终点。
4.称取0.10~0.20g(NH4)2SO4 三份于锥形瓶中。
5.将称量得到的(NH4)2SO4用20-30mL水溶解后,加入5mL中性甲醛溶液,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至淡红色,半分钟内不变色,即为终点。
五、数据记录及处理
1.数据记录表格
2. 含氮量的计算
含氮量N%=CNaOH×VNaOH×M(N)×100%/m
六、注意事项
1.如果铵盐中含有游离酸,应事先中和除去,先加甲基红指示剂,用NaOH溶液滴定至溶液呈橙色,然后再加入甲醛溶液进行测定。
2.甲醛中常含有微量甲酸,应预先以酚酞为指示剂,用NaOH溶液中和至溶液呈淡红色。
3.滴定中途,要将锥形瓶壁的溶液用少量蒸馏水冲洗下来,否则将增大误差。
七、实验讨论
1、铵盐中氮的测定为何不采用NaOH直接滴定法?
答:铵盐NH4Cl和(NH4)2SO4是常用的氮肥,系强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),用NaOH标准溶液直接滴定,在滴定曲线上已无明显突跃,此时反应的完全程度很低,难以用指示剂来确定滴定终点。故不采用NaOH标准溶液直接滴定。
2、为什么中和甲醛试剂中的甲酸以酚酞作指示剂;而中和铵盐试样中的游离酸则以甲基红作指示剂?
答:选择指示剂是根据滴定终点溶液的酸碱性和指示剂的变色范围来决定的。酚酞指示剂的变色范围是8.0-9.6,甲基红指示剂的变色范围是4.4-6.2,中和铵盐试样中的游离酸时其滴定终点溶液显酸性,中和甲醛试剂中的甲酸时其滴定终点溶液显弱碱性,所以,中和甲醛试剂中的甲酸以酚酞作指示剂;而中和铵盐试样中的游离酸则以甲基红作指示剂。
3. NH4HCO3中含氮量的测定,能否用甲醛法?
答:不能用甲醛法测定。
NH4HCO3是弱酸弱碱盐,在水中的水解常数K=KW/(Ka×Kb)=1.31×10-3,因为Ka<Kb,溶液显碱性,可以加入1-2滴甲基橙,用0.1mol.L-1HCl溶液滴定溶液由黄色至橙色,加入5ml中性甲醛溶液,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至淡红色,半分钟内不变色。
