实验三 硫酸铵肥料中含氮量的测定(甲醛法)
【实验目的】
1. 了解弱酸强化的基本原理
2. 掌握甲醛法测定氨态氮的原理和操作方法。
3. 熟练掌握酸碱指示剂的选择原理。
【实验原理】
1.NaOH标准溶液的标定
用基准物质(邻苯二甲酸氢钾,草酸)准确标定出NaOH溶液的浓度 本实验所用基准物为邻苯二甲酸氢钾
邻苯二甲酸氢钾:优点:易制得纯品,在空气中不吸水,易保存,摩尔质量大,与NaOH反应的计量比为1:1。
KHC8H4O4在100~125℃下干燥1~2h后使用。
化学计量点时,溶液呈弱碱性(pH≈9.20),可选用酚酞作指示剂。
2.铵盐中氮含量的测定:
将甲醛与一定量的铵盐作用,生成相当量的酸(H)和质子化的六次甲基四铵盐(Ka=7.1×10),反应如下:
4NH4 + 6HCHO = (CH2)6N4H + 3H + 6H2O
生成的H和质子化的六次甲基四胺(Ka=7.1×10),均可被NaOH标准溶液准确滴定(弱酸NH4被强化)。
(CH2)6N4H+3H+4NaOH = 4H2O + (CH2)6N4 + 4Na
4mol NH4 相当于4mol的 H 相当于4mol的 OH 相当于4mol的 N。所以氮与NaOH 的化学计量数比为1。
化学计量点时溶液呈弱碱性(六次甲基四胺为有机碱),可选用酚酞作指示剂。 终点:无色→微红色(30S内不褪色)
注意:(1)若甲醛中含有游离酸(甲醛受空气氧化所致,应除去,否则产生正误差),应事先以酚酞为指示剂,用NaOH溶液中和至微红色(pH≈8) (2)若试样中含有游离酸(应除去,否则产生正误差),应事先以甲基红为指示剂,用NaOH溶液中和至黄色(pH≈6)(能否用酚酞指示剂?)
【仪器和试剂】
碱式滴定管(50 ml); 移液管(25ml);锥形瓶(250ml);烧杯(50ml);容量瓶(250 ++-+++++-6+++-6+
ml)
NaOH 溶液(0.1mol/L); 浓HCl; 甲基红指示剂(2g/L,60%乙醇溶液或其钠盐的水溶液);酚酞指示剂(2g/L乙醇溶液);甲醛(18%即1:1)。 【实验步骤】
1.0.1mol·LNaOH溶液的标定
用差减法准确称取0.4~0.6g已烘干的邻苯二甲酸氢钾三份,分别敲入三个已编号的250mL锥形瓶中,加40~50mL水溶解(可稍加热以促进溶解),2~3d酚酞,用NaOH溶液滴定至微红色(30S内不褪),记录VNaOH,计算C NaOH和标定结果的相对偏差(应小于或等于±0.2%,否则需重新标定)。
2.试样中含氮量的测定
(1)准确称取2-3 g的(NH4)2SO4于小烧杯中,用适量蒸馏水溶解,定量地转移至250 ml 容量瓶中,用蒸馏水稀释至刻度,摇匀。
(2) 用移液管移取试液25.00 ml于250 ml锥形瓶中,加1滴甲基红指示剂, 用0.1 mol/L的 NaOH溶液中和至黄色。加入10ml已中和的(1:1)甲醛溶液,再加入1~2滴酚酞指示剂摇匀,静置一分钟后(强化酸),用0.1 mol/L NaOH 标准溶液滴定至溶液呈微橙色,并持续半分钟不褪,即为终点(终点为甲基红的黄色和酚酞红色的混合色)。记录滴定所消耗的NaOH 标准溶液的读数,平行做3次。根据NaOH 标准溶液的浓度和滴定消耗的体积,计算试样中氮的含量和测定结果的相对偏差。 【实验结果】
表1 0.1 mol/L NaOH溶液的标定
记录项目
KHC8H4O4质量(g)
消耗NaOH溶液体积VNaOH/mL CNaOH / mol/L
1
2
3
-1
表2 硫酸铵中含氮量的测定(甲醛法)
项目 m(试样)(g)
(NH4)2SO4溶液总体积(mL) 滴定时移取V(NH4)2SO4(mL) CNaOH (mol·L-1) VNaOH(mL)
试样的含氮量(%) 含氮量的平均值(%) 相对偏差 平均相对偏差
1
2
3
思考题
1. NH4+为NH3的共轭酸,为什么不能直接用NaOH溶液滴定? 2.NH4NO3, NH4CI或NH4HCO3中的含氮量能否用甲醛法测定?
3.为什么中和甲醛中的游离酸用酚酞指示剂,而中和(NH4)2SO4试样中的游离酸用甲基红指示剂?
第二篇:氯化铵的制备及氮含量的测定
氯化铵的制备及氮含量的测定
一、实验原理
1、氯化铵的制备:
本实验用氯化钠与硫酸铵作用来制备氯化铵:
2NaCl +(NH4)2SO4 ==== Na2SO4 + 2NH4Cl
根据它们的溶解度及其受温度影响差别的原理,采取加热、蒸发、冷却等措施,使溶解向结晶转化,从而达到分离。
反应涉及物质在不同温度下的溶解度值

由表可知,氯化铵、氯化钠、硫酸铵在水中的溶解度均随温度的升高而增加。不过,氯化钠溶解度受温度的影响不大;硫酸铵的溶解度无论在低温还是高温都是最大的。硫酸钠的溶解度有一转折点。十水硫酸钠的溶解度也是随温度的升高而增加,但达一定温度时脱水变成Na2SO4。Na2SO4的溶解度随温度的升高而减小。所以,只要把氯化钠、硫酸铵溶于水,加热蒸发,Na2SO4就会结晶析出,趁热过滤。然后再将滤液冷却,NH4Cl晶体随温度的下降逐渐析出,在35℃左右抽滤,即得NH4Cl产品。
2、氮含量的测定
NH4Cl是常用的氮肥,系强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),故无法用NaOH标准溶液直接滴定。生产和实验室中广泛采用甲醛法测定铵盐中的含氮量。甲醛法是基于如下反应:
4NH4+ + 6HCHO ====(CH2)6N4H+ + 6H2O + 3H+
(CH2)6N4H+ + 4OHˉ ==== H2O +(CH2)6N4
生成的H+和(CH2)6N4H+(Ka=7.1×10-6)可用NaOH标准溶液滴定,计量点时产物为
(CH2)6N4,其水溶液显微碱性,可选用酚酞作指示剂。
二、实验仪器及试剂
1、仪器:
锥形瓶(3个250ml);电子分析天平;碱式滴定管(25ml);烧杯(100ml两个,50ml一个);普通漏斗;蒸发皿;水浴锅;真空泵;量筒(50ml,5ml各一个);玻璃棒;铁架台;电子天平;布氏漏斗;滤纸;温度计(100℃);试管;试管夹:精密PH试纸;酒精灯。
2、药品:
酚酞;甲基红;NaOH标准溶液;1:1的甲醛水溶液;NaCl固体(分析纯);
(NH4)2SO4固体(分析纯)。
三、实验内容
a)氯化铵的制备
1.称取11gNaCl,放入100mL烧杯内,加入30—40mL蒸馏水。加热、搅拌使之溶解。若有不溶物,则用普通漏斗过滤分离,滤液用蒸发皿盛。
2.在NaCl溶液中加入13g(NH4)2SO4。水浴加热、搅拌,促使其溶解。在浓缩过程中,有大量Na2SO4结晶析出。当溶液减少到35mL(提前作记号)左右时,停止加热,并趁热抽滤。
3.将滤液迅速倒入100mL烧杯中,静置冷却,NH4Cl晶体逐渐析出,冷却至35℃左右,抽滤。
4.把滤液重新置于水浴上加热蒸发,至有较多Na2SO4晶体析出,抽滤。倾出滤液于小烧杯中,静置冷却至35℃左右,抽滤。如此重复二次。
5.把三次所得的NH4Cl晶体合并,一起称重,计算产率。
6.产品的鉴定:
取1gNH4Cl产品,放于一干燥试管的底部,加热。
NH4Cl杂质含量=(G灼烧后-G空试管)g/1g´×100%
b)氮含量的测定
1.用NaOH处理甲醛溶液,使甲醛溶液呈中性。
2.称取0.08—0.10gNH4Cl三份于锥形瓶中。
3.将称量得到的NH4Cl用20—30mL水溶解后,加入5mL中性甲醛溶液,加入1—2滴酚酞,用0.1mol.L-1NaOH滴定至淡红色,半分钟内不变色,即为终点
四、产品质量鉴定及氮含量测定
1.数据记录表格

2NaCl +(NH4)2SO4 ==== Na2SO4 + 2NH4Cl
2×58.44 132.16 2×53.49
m(NaCl)m((NH4)2SO4) 10
m(NaCl)=10×58.44/53.49=10.93(g)
m((NH4)2SO4)=10×132.16/(2×53.49)=12.35(g)
2.氮含量测定数据记录
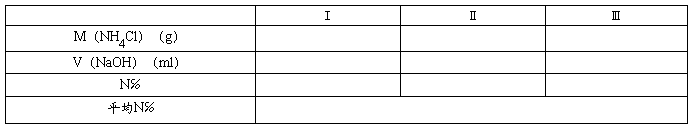
M(NH4Cl)=11×53.49/58.44=10.07(g)
产率=M(实)/M(NH4Cl)×100%
2.含氮量的计算:
含氮量N%=CNaOH×VNaOH×M(N)×100%/m
五、注意事项
1.用水溶解的溶质量较多时,溶液体积与水的体积不等。
2.水量30-40mL即可,浓缩时要提前作好记号,浓缩不能过度,以防NaCl、(NH4)2SO4析出,趁热抽滤时要预热仪器。多次浓缩分离(NH4)2SO4与NH4Cl。
3.如果铵盐中含有游离酸,应事先中和除去,先加甲基红指示剂,用NaOH溶液滴定至溶液呈橙色,然后再加入甲醛溶液进行测定。
4.甲醛中常含有微量甲酸,应预先以酚酞为指示剂,用NaOH溶液中和至溶液呈淡红色。
5.滴定中途,要将锥形瓶壁的溶液用少量蒸馏水冲洗下来,否则将增大误差。
六、参考资料
《大学化学基础实验》科学出版社(第二版)
《无机及分析化学实验》科学出版社(第一版)
《无机化学实验化学》工业出版社(第一版)
《分析化学》华南理工大学四川大学编(第六版)
GB 2946-92 氯化铵
HG/T 2843-1997 化肥产品 化学分析常用标准滴定溶液、标准溶液、试剂溶液和指示剂溶液
费强沈成欢刘玲佩丁海滨
