硫酸铜晶体结晶水含量的测定
1. 实验原理
CuSO4·5H2O受热时逐步失去结晶水的过程可表示如下:
113℃ 250℃ 102℃ CuSO4·5H2OCuSO4·3H2OCuSO4·H2OCuSO4
蓝色 蓝白色 白色
根据加热前后的质量差,可推算出其晶体的结晶水含量。
2. 实验仪器
。
3. 操作步骤
(1)研磨:在研钵中将硫酸铜晶体研碎。(防止加热时可能发生迸溅)
(2)称量:准确称量一干燥洁净的瓷坩锅质量(m1g)。
(3)再称:称量瓷坩埚+硫酸铜晶体的质量(m2g)。
(4)加热:小火缓慢加热至蓝色晶体全部变为白色粉末(完全失水),并放入干燥器中冷却。
(5)再称:在干燥器内冷却后(因硫酸铜具有很强的吸湿性),称量瓷坩埚+硫酸铜粉末的质量(m3g)。
(6)再加热:把盛有硫酸铜的瓷坩埚再加热,再冷却。
(7)再称重:将冷却后的盛有硫酸铜的瓷坩埚再次称量(m4g 两次称量误差≤0.1g)。
(8)计算:根据实验测得的结果计算硫酸铜晶体中结晶水的质量分数。
简称:“一磨”、“四称”、“两热”、“一算”。
⊿计算过程
4. 注意事项★ ① 称前研细; ② 小火加热; ③ 在干燥器中冷却;
④ 不能用试管代替坩埚; ⑤ 加热要充分但不“过头”(温度过高CuSO4也分解)。 CuSO4
- 1 - △ CuO+SO3↑ 2SO3催化剂 加热 SO2+O2 总反应:2CuSO4 △ 2CuO+2SO2↑+O2↑
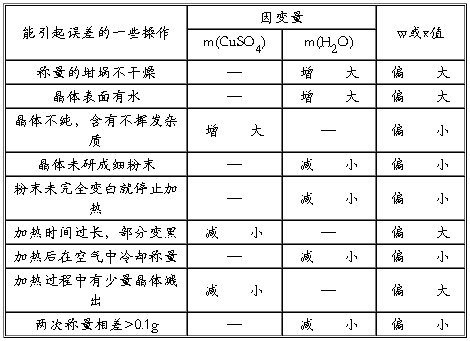
5. 误差分析(填“偏高”或“偏低”或“无影响”)
①加热温度过高或时间过长,固体部分变为灰白色(CuO)
②晶体中含有(或坩埚上附有)受热易分解或易挥发的杂质
③加热温度过低(<100℃)或时间不够
④加热时质量未至恒重就停止加热
⑤加热时搅拌不当使晶体溅出坩埚外或被玻璃带走少量
⑥瓷坩埚内有不挥发性杂质
⑦两次称量相差0.12g
⑧加热后坩埚放在空气中冷却
⑨实验前晶体有吸潮现象或加热前所用的坩埚未完全干燥
⑩晶体中含有受热不分解或难挥发的杂质
练习
1、根据测定硫酸铜晶体中结晶水含量的实验,填写下列空白:
(1)本实验中除需要下面所给出的仪器外,还需要的三种仪器是、、(填仪器名称)。
A.三角架 B.干燥器 C.坩埚钳 D.酒精灯 E.坩埚 F.泥三角 G.药匙
(2)某学生实验得到以下数据:加热前容器的质量为m1、容器和晶体的总质量为m2,加热后容器和无水硫酸铜的总质量为m3。请写出CuSO4·nH2O中n的值(用含ml、m2、m3代数式表示):n=__________________________。
(3)下列情况会使实验中测得的n值偏大的是(填写字母。
A.加热前称量盛硫酸铜晶体的容器未完全干燥
B.加热后容器未放在干燥器中冷却
C.加热前没用滤纸把晶体表面的水分吸干
D.加热后的粉末中有少量黑色固体
2、0.80 g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
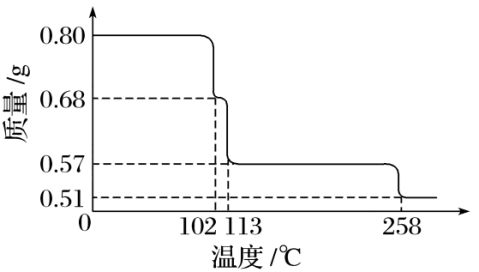
请回答下列问题:
(1)试确定200 ℃时固体物质的化学式________________;
(要求写出推断过程)。
(2)取270 ℃所得样品,于570 ℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为 ;把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为________,其存在的最高温度是________。
- 2 -
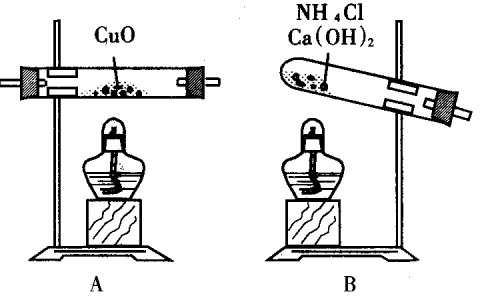
3、实验室用氨气还原氧化铜的方法测定铜的相对原子质量,反应的化学方程式为:
2NH3十3CuO △
N2十3Cu十3H2
O
。
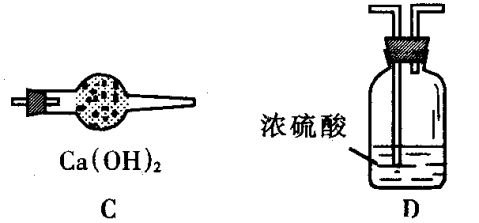
(1)如果选用测定反应物CuO和生成物H2O的质量m(CuO)、m(H2O)时,请用上图所示的仪器设计一个简单的实验方案。
①仪器连接的顺序(填编号;仪器可重复使用)是____________________________ D中浓硫酸的作用是______________________
②列出计算Cu的相对原子质量的表达式:______________
③下列情况将使测定结果偏大的是_________
a.CuO未全部还原为Cu b.CuO受潮 c.CuO中混有Cu
(2)如果仍采用如图所示的实验装置,设计其他方案,还可测定的物理量有______________
A.m(Cu) m(CuO) B.m(N2) m(H2O)
C.m(Cu)和m(H2O) D.m(NH3)和m(H2O)
4、实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N
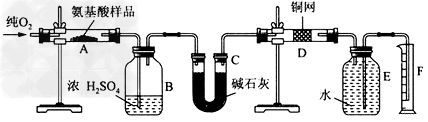
2。现按下图所示装置进行实验。


④实验中测得N2的体积为VmL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据为

- 3 -

- 4 -
答案

1、(1) (2)80(m2-m3)/9(m3-m1)
(3) A C D
2、(1)CuSO4·H2O
CuSO4·5H2O=====CuSO4·(5-n)H2O+nH2O
250 18n
0.80 g 80 g-0.57 g=0.23 g
25018n=,求得n≈4。200 ℃时产物为CuSO4·H2O 晶体。 0.80 g0.23 g
(2)CuSO4=====CuO+SO3↑ CuSO4·5H2O 102 ℃
3、(1)①BCACD 吸收未反应的氨;防止空气中水分进入。
②570 ℃200 ℃18m(CuO)
m(H2O)?16 ③a c (2)AC
4、①排除体系中的N2。
②吸收未反应的O2,保证最终收集的气体是N2。
③量筒内液面与广口瓶中的液面相持平,视线与凹液面最低处相切。
④二氧化碳气体的质量、生成水的质量、氨基酸的相对分子质量
- 5 -
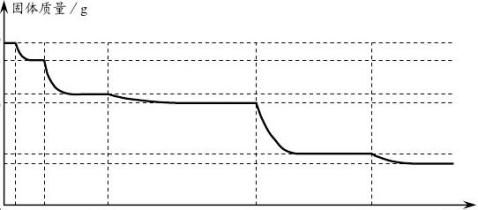
将25.0 g胆矾晶体放在坩埚中加热测定晶体中结晶水的含量,固体质量随温度的升高而变化的曲线如下图。
温度/℃
请认真分析上图,填写下列空白:
? 30℃~110℃间所得固体的化学式是____________,650℃~1000℃间所得固体的化学式是_____________,温度高于1000℃后所得固体的化学式是______________;
? 常温下无水硫酸铜____________(选填“可以”或“不可以”)用作干燥剂,进行硫酸铜晶体结晶水含量测定实验时,温度应控制在_________________范围内。
- 6 -
第二篇:硫酸铜晶体里结晶水含量的测定及水晶知识
水晶常识
紫水晶
水晶是一种无色透明的石英结晶体矿物。它的主要化学成分是二氧化硅,跟普通砂子是同一娘胎的物质。当二氧化硅结晶完美时就是水晶;二氧化硅胶化脱水后就是玛瑙;二氧化硅含水的胶体凝固后就成为蛋白石;二氧化硅晶体粒子小于几微米时,就组成玉髓、燧石、次生石英岩。
结晶完美的水晶晶体属于六方晶系,常呈六棱柱状,柱体为一头尖或两头尖,多条长柱体连结在一块,通称晶族,美丽而壮观。二氧化硅结晶不完整,形状可谓是千姿百态。当你到海南水晶陈列馆去瞧一瞧,可以大开眼界:除了常见的长柱状外,还似宝剑形,有的若板状,有的如短柱形,有的像双锥。有的小如手指,有的大如巨石,有的不足半两,有的重达300多公斤。
水晶为什么能受得起一般性摔打?这是因为它有强健的“筋骨”,宝石学称之为硬度,硬度是指宝石抵抗外力刻划的强度。
水晶的硬度如何测得?
很早以前,当铺的老板对他们认为可疑的水晶仿制品,利用一个硬的尖物或钢锉在不明显的翻面作硬度检测,他们在面上刻划,留下一点不显眼痕迹,以便提醒其它典当同行注意。很显然这是一种最原始、最笨拙的测试手段,它有可能导致水晶破损。
1824年,一位叫弗里希.摩斯的奥地利矿物学家,从许多矿物中抽出10个品种,经过科学实验测出它们的相对硬度,由此得出水晶硬度为摩氏7。尽管后来美国国家标准局使用、推广更科学的诺普硬度测试器,但世界上许多国家的珠宝商,仍习惯于摩氏硬度表。
水晶的硬度相当于钢锉一般坚硬,这使得脆且易碎的黄玉、钻石、欧泊石、祖母绿之类的宝石相形见拙。
水晶解理:无。
解理,俗称辟开。某些宝石(如黄玉、钻石)在外力敲打、挤压或碰撞后,会沿着一个平面裂开,宝石的这种性质称为解理。
水晶破口:贝壳状。
破口,矿物学称为断口。它是指宝石在一定外力撞击下,不按一定的结晶方向破裂,而是形成一个断开的面。换一种解释,是说宝石的裂口可以沿着任何方向延伸,而不是沿着解理而发展。
结晶完好的水晶,常有好的人字形断口;在紫晶和热处理的黄晶中,多呈不平坦到薄片状破口。
水晶比重:2.56-2.66克/立方厘米。
这意味着一定体积水晶的重量,是相同体积水的重量的2.56-2.66倍。块状变种水晶密度可能稍高些。
水晶条痕:无色。
条痕,通常说的颜色,是人眼对一定波长的光线感觉的结果。
水晶透明度与透过它的光的质与量有关。
透明标准为:光线透明过厚度为1厘米以上的水晶碎片或薄片时,可以清晰地看到映出的图像。如是底像不够清楚,仅见轮廓,那便是半透明。
水晶光泽:玻璃光泽。无论在抛光面上还是在破口,都是如此。
光泽,指宝石表面对光线反射的一种光学性质。水晶既不像星光蓝宝石那样反射出绮丽的星光形条纹,又不像月光石那样发出淡蓝色波形光彩,更不像乘欧泊石那样闪烁着五颜六色。
观察水晶的光泽,可用手握着它,以灯光或窗户投进来的光线看表面反射,透明水晶亮度与光泽强弱有关。
水晶折射率:1.544-1.553,几乎不超出此范围。
折射率,是当光由空气中透入宝石晶体,并产生折射现象,其入射角正弦与折射角正弦之比值。
水晶重折射率:0.009(最大),此值非常稳定。
水晶光性特征:一轴晶正光性。
水晶色散:0.013。
色散是说宝石的折射率随照明光的不同而有一定的变化。例如钻石对红光折射为2.405;对绿光为2.427;紫光为2.449。
水晶熔点为1713摄氏度。其受热易碎的特性,是在实验时发现的。将水晶放在喷焰器的烈焰燃烤,除非有很好的保护,且慢慢冷却,否则晶体容易碎裂。这一脾性,古人已摸透。《博物要览》提醒道:“凡用水晶器物,不可用热汤滚水注之,即粉裂如击破者。”
水晶另一脾性就是怕碱不怕酸(氢氟酸除外),这是由于氧化硅特性所决定的。
像玛瑙一类宝石,当受热、摩擦、吹气或受打击时,往往散发一种特殊气味,使人联想到大蒜、马肉、萝卜、松香味儿,然而,水晶在上述情况下,绝无异味。
附:
水晶的化学成分及性质:
化学式为SiO2。纯净的无色透明的水晶是石英的变种。化学成分中含Si—46.7%,O—53.3%。由于含有不同的混入物而呈多种颜色。紫色和绿色等颜色是由金属离子所致。在水晶中含有砂状、碎片状针铁矿、赤铁矿、金红石、磁铁矿、石榴石、绿泥石等包裹体;发晶中则含有肉眼可见的似头发状的针状矿物的包裹体形成。含锰和铁者称紫水晶;含铁者( 呈金黄色或柠檬色 )称黄水晶;含锰和钛呈玫瑰色者称蔷薇石英;烟色者称烟水晶;褐色者称茶晶;黑色透明者称为墨晶;呈浅绿色者称为石髓。
水晶晶体结构及形态:
属三方晶系。晶体呈棱柱状并带六边形锥,柱面有横纹,紫水晶中常有角状色带。在自然界中,水晶常呈晶簇产出,造型美观。
水晶的物理性质:
水晶呈无色、紫色、黄色、绿色及烟色等。玻璃光泽。透明至半透明。硬度7。性脆。比重2.65。无解理。贝壳状断口,也有人字形断口。紫水晶具有清楚的二色性,黄水晶和茶水晶具有弱的二色性。发光水晶具有强烈的磷光性。带绿色的砂金水晶在长、短波紫外线照射下发灰绿色荧光。具有猫眼、虹彩和砂金效应。水晶具压电性。
硫酸铜晶体里结晶水含量的测定
一、“相似相溶”原理
在水、四氯化碳中分别加入蔗糖、磷酸、碘和萘(C10H8)晶体,试观察这四种分子晶体在上述两种溶剂中的溶解性。
几种分子晶体在水和四氯化碳中的溶解情况:(见下表)
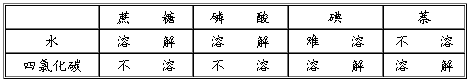
可以看出,蔗糖和磷酸易溶于水,不易溶于四氯化碳;而萘和碘却易溶于四氯化碳,不易溶于水。这说明,有些分子晶体在溶解性上差异很大,并且同一分子晶体在不同的溶剂中溶解性也有很大的差别。若分析这几种晶体和溶剂的结构就可以知道,蔗糖、磷酸、水是极性分子,而碘、萘和四氯化碳是非极性分子。通过对该实验和其他许多实验的观察和研究,人们得出了一个经验性的“相似相溶”结论:非极性溶质一般能溶于非极性溶剂;极性溶质一般能溶于极性溶剂。
二、硫酸铜晶体里结晶水含量的测定
1.实验原理
硫酸铜晶体中结晶水的质量分数=
(硫酸铜晶体和瓷坩埚的质量—无水硫酸铜和瓷坩埚的质量=结晶水的质量)。
2.实验步骤
①研磨:在研钵中将硫酸铜晶体研碎。
②称量;准确称量干燥的瓷坩埚的质量,并用此坩埚准确称取一定质量已研碎的硫酸铜晶体。
③加热:加热晶体,并用玻璃棒轻轻搅拌晶体,使其失去全部结晶水(由蓝色完全变为白色)。加热装置如下图所示(加热时去掉坩埚上盖)。
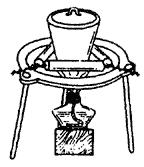
④称量:在干燥器内冷却后称量,并记下瓷坩埚和无水硫酸铜的质量。
⑤再加热、再称量至恒重:把盛有无水硫酸铜的瓷坩埚再加热,再放入干燥器里冷却后再称量,记下质量。到两次称量的质量相差不超过0.1g为止。
⑥计算:根据实验测得的结果求硫酸铜晶体中结晶水的质量分数。
3.注意事项
①晶体加热后先放在石棉网上稍冷却,之后一定要放在干燥器内冷却,以保证无水硫酸铜不会从空气中吸收水分而引起测得值偏低(相当于水没有完全失去)。
②晶体要在坩埚底上摊开加热,有利于失去全部结晶水,以免引起测得值偏低。
③加热时间不充分、加热温度过低(未全变白),都会使测得值偏低。
④加热过程中,应慢慢加热(可改垫石棉网),以防因局部过热而造成晶体溅失,引起测量值偏高。
⑤加热温度过高或时间过长,会导致硫酸铜少量分解,使测得值偏高。
4.讨论题解答:分析实验中产生误差的原因
设硫酸铜晶体组成CuSO4·xH2O,m1为坩埚和晶体的质量,m2为加热后冷却称量所得坩埚与粉末的质量。
原理: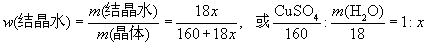
产生误差的原因及误差分析:
(1)称量的坩埚不干燥:加热后水分蒸发,这样实验过程减少的质量包括晶体中结晶水的质量和坩埚带有水的质量两部分,因计算时将实验过程减少的质量看作结晶水的质量,这样该过程计算时代入的m1—m2的值偏大,则计算出的w或x偏大。
(2)晶体表面有水:加热后水分蒸发,原理同(1),使得m1—m2的值偏大,则w或x偏大。
(3)晶体不纯,含有不挥发杂质:加热后不挥发性杂质不分解,只有其中的硫酸铜晶体分解,使得m1—m2的值偏小,则w或x偏小。
(4)晶体未研成细粉末:加热时由于晶体颗粒太大,使得颗粒内部的结晶水不能失掉,导致m1—m2的值偏小,则w或x偏小。
(5)粉末未完全变白就停止加热:粉末未完全变白说明结晶水未完全失掉,导致m1—m2的值偏小,则w或x偏小。
(6)加热时间过长,部分变黑:晶体变黑说明CuSO4已发生分解:CuSO4 CuO+SO3↑,使得m1—m2的值偏大,则w或x偏大。
CuO+SO3↑,使得m1—m2的值偏大,则w或x偏大。
(7)加热后在空气中冷却:加热后在空气中冷却,会使CuSO4又结合空气中的水蒸气,使得m1—m2的值偏小,则w或x偏小。
(8)加热过程中有少量晶体溅出:晶体溅出,使得m1—m2的值偏大,则w或x偏大。
(9)两次称量相差>0.1g:两次称量相差>0.1g,说明结晶水未完全失掉,使得m1—m2的值偏小,则w或x偏小。
以上分析可归结为下表:
硫酸铜晶体结晶水含量测定实验误差分析