实验三 氢氧化钠溶液的配制和酸碱溶液的比较滴定
实验者姓名 班级 学号 实验地点 实验日期
预习报告
一、实验目的:
1. 学会和掌握常用玻璃仪器的洗涤方法、操作要点和洗净的评判。
2. 学会NaOH标准溶液的配制方法及具体操作。
3. 学会并掌握滴定管的使用、指示剂的加入、终点的判断和数据记录等基本操作的方法和技巧。
二、实验原理:
三、实验内容与步骤
1. 500mL 0.1mol/L NaOH溶液的配制: 用台称称取氢氧化钠固体2g于小烧杯中→ 从500mL量筒中取适量水溶解 → 转移到500mL试剂瓶中 → 加完量筒中的水,盖上塞后摇匀即可。
2. 比较滴定练习:用0.1mol/L NaOH溶液滴定0.1mol/L HCl溶液 酚酞做指示剂,平行测定2~3次。
用0.1mol/L HCl溶液滴定0.1mol/L NaOH溶液 甲基橙做指示剂,平行测定2~3次。
3. 进行数据记录与处理。
四、原始数据记录:
mNaOH = g


 甲基橙指示剂 酚酞指示剂
甲基橙指示剂 酚酞指示剂
V(HCl)初读数: 、 、 ; 、 、
/mL 终读数: 、 、 ; 、 、
V(NaOH)初读数: 、 、 ; 、 、
/mL 终读数: 、 、 ; 、 、
五、思考题的回答
如何洗涤滴定管、容量瓶、移液管、锥形瓶、量筒等玻璃仪器?玻璃洗干净的标准是怎样的?
指导教师签名
实验报告 实验者姓名 班级 学号 实验日期
一、实验结果及数据处理
1. 酸碱溶液的比较滴定
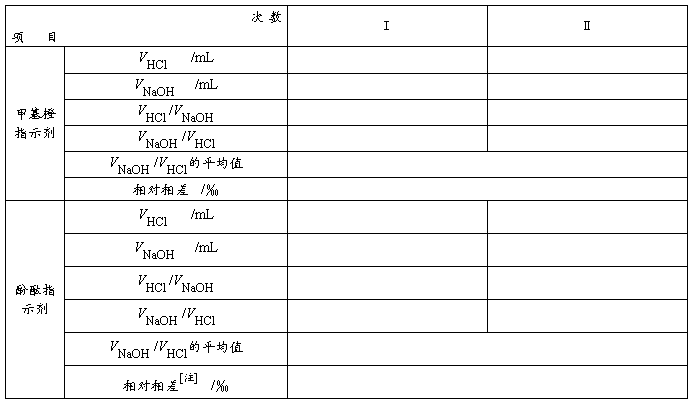
注: 只要取测定结果中你认为最好的两组数据进行计算。以后各个实验均按此方法处理实验报告数据。
二、问题与讨论
实验中所用的锥形瓶、容量瓶、滴定管、量筒要不要用操作液淋洗,为什么?
三、批阅教师评语
第二篇:实验十七 氢氧化钠标准滴定溶液的配制和标定哦哦哦哦哦普
实验十七 氢氧化钠标准滴定溶液的配制和标定
一、预习要点
1.基准物质、标准溶液的配制和标定。
2.滴定管的使用与滴定基本操作技术。
3.有关反应原理。
二、目的要求
1.练习溶液的配制和滴定的准备工作,训练滴定操作进一步掌握滴定操作。
2.学习用邻苯二甲酸氢钾标定氢氧化钠的方法。
3.了解强碱弱酸盐滴定过程中 pH的变化。
4.熟悉指示剂的变色观察,掌握终点的控制。
三、实验原理
由于 NaOH容易吸收空气中的水分和 CO2,故不能直接配制成标定溶液,必须经过标定以确定其准确的浓度。标定NaOH 溶液的基准物质主要有邻苯二甲酸氢钾 (KHC8H4O4,摩尔质量为204.2 g ·mol -1 )、草酸 (H2C2O4 ·2H2O,摩尔质量126.07 g ·mol -1 )等,其中以邻苯二甲酸氢钾使用最广泛。邻苯二甲酸氢钾,容易制得纯品,不含结晶水,在空气中不吸水,容易保存,摩尔质量大,比较稳定,是较好的基准物质。它与氢氧化钠的反应式为


反应物之间的摩尔比为 1 : 1。化学计量点的产物邻苯二甲酸钾钠是二元弱碱( Kb1 =2.6×10 -9),因此化学计量点时的溶液为弱碱性, pH ≈ 9。选用酚酞作指示剂,滴定终点由无色变为浅红色。
四、实验用品
分析天平(感量0.01mg/分度),量筒,称量瓶,50mL碱式滴定管,250mL锥形瓶,塑料量筒。
工作基准试剂邻苯二甲酸氢钾:先置于105℃~110℃电烘箱中干燥至恒重,保存于干燥器中。
浓HCl(浓或0.1mol/L),、NaOH(固或0.1mol/L),
酚酞指示液(10 g/L)、
五、实验步骤
1.氢氧化钠标准滴定溶液的配制
称取110 g氢氧化钠,溶于100 ml无二氧化碳的水(怎样制备?)中,摇匀,注入聚乙烯容器中,密闭放置至溶液清亮。用塑料量筒量取上层清液5.4mL,用无二氧化碳的水稀释至1000 mL,摇匀。
2.氢氧化钠标准滴定溶液的标定
称取于105℃~110℃电烘箱中干燥至恒重的工作基准试剂邻苯二甲酸氢钾4份,每份约0.75g(称准至0.1mg),加无二氧化碳的水50mL溶解,加2滴酚酞指示液(10 g/L),用待标定的氢氧化钠溶液滴定至溶液呈粉红色,并保持30 s。同时做空白试验。
3.计算
氢氧化钠标准滴定溶液的浓度〔c(NaOH)],数值以摩尔每升(mol/L)表示,按下式计算:


式 中 :
m —邻苯二甲酸氢钾的质量的准确数值,单位为克(g);
V1 —氢氧化钠溶液的体积的数值,单位为毫升(mL);
V2一 空白试验氢氧化钠溶液的体积的数值,单位为毫升(mL);
M一 邻苯二甲酸氢钾的摩尔质量的数值,单位为克每摩尔(g/mol)[M(KHC8H4O4)= 204.22 ]。
4.实验报告格式
氢氧化钠标准滴定溶液的标定记录格式自定。
六、问题讨论
1.为什么 NaOH标准溶液配制后,要经过标定 ?
2.若蒸馏水中含有 CO 2对测定有何影响?如何避免?
3.市售的 NaOH试剂中常有少量的 Na2CO3等杂质,它们与酸作用即生成 CO2,这对滴定终点有无影响?在配制 NaOH标准溶液时,应采取什么措施?
4.用邻苯二甲酸氢钾标定氢氧化钠溶液时,为什么用酚酞作指示剂而不用甲基红或甲基橙作指示剂?
5.称取NaOH及邻苯二甲酸氢钾各用什么天平?为什么?
6.标定时用邻苯二甲酸氢钾比用草酸有什么好处?
7.试分析实验中产生误差的原因。
七、参考文献
1.GB/T 601-2002化学试剂 标准滴定溶液的制备
2.GB/T11792-1989测试方法的精密度
3.GB/T603-2002化学试剂 实验方法中所用制剂及制品的制备
4.JJF1059-1999中华人民共和国国家计量技术规范 测量不确定度评定与表示
