【课题】第三节化学平衡 课时三 化学平衡常数
【学习目标】
1、通过观察分析图表,了解化学平衡常数的概念,并明确其意义。
2、通过自学例题,学会运用化学平衡常数进行相关的计算,如物质的平衡浓度及转化率。
【学习过程】
【问题探究】观察分析P29图表中的实验数据,你能得出哪些结论?
一、化学平衡常数
1、定义:
在一定温度下,当一个可逆反应达到______时,生成物________与反应物___________的比值是一个常数。这个常数就是该反应的化学平衡常数(简称平衡常数),用________表示
2、表达式:
对于一般的可逆反应:mA(g)+nB  pC(g)+qd(g),当在一定温度下达到平衡时,K=__________
pC(g)+qd(g),当在一定温度下达到平衡时,K=__________
3、特点:K只受_______影响,与反应物或生成物的无关。
4、意义:
(1)平衡常数的大小反映了化学反应进行的程度
①K值越大,说明平衡体系中生成物所占比例_________。它的正向反应进行的程度________,即该反应进行得越_____,反应物的转化率_______。
②K值越小,说明平衡体系中生成物所占比例_________,它的正向反应进行的程度_______,即该反应进行的程度越_____,反应物的转化率___________。
(2)一般当K>______时,该反应进行得基本完全。
5、反应的的转化率
某个指定反应物的转化率=____________________________________
二、使用化学平衡平衡常数应注意的事项
(1)必须指明温度,反应必须达到平衡状态;
(2)平衡常数表示反应进行的程度,不表示反应的快慢,即速率大,K值不一定大。
(3)反应物或生成物中有固体或纯液体存在时,由于其浓度可看作“1”,而不代入公式。
【课堂练习】
1、一定温度下,C(s)+H2O(g) CO(g)+H2(g),K=
CO(g)+H2(g),K=
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g),K=
2Fe(s)+3CO2(g),K=
2SO2(g)+O2(g)  2SO3(g) K=
2SO3(g) K=
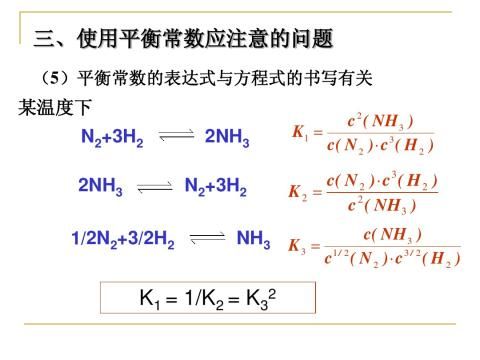
(4)平衡常数的表达式与方程式的书写有关
【思考题】某温度下①N2(g)+3H2(g) 2NH3(g)的平衡常数为K1=__________,
2NH3(g)的平衡常数为K1=__________,
②2NH3(g)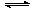 N2(g)+3H2(g)的平衡常数为K2=__________,
N2(g)+3H2(g)的平衡常数为K2=__________,
【问题思考】通过K1 、K2 书写,它们的表达式相同吗?K1 与K2之间存在什么关系?
二、化学平衡常数的应用
1、判断反应进行的程度
K 值越大,说明平衡体系中________所占比例越大,正向反应进行的程度______,即该反应进行得越完全,反应物转化率_______;反之,就越不完全,转化率就越小。
2、利用K可判断反应的热效应
若升高温度,K值增大,则正反应为 反应(填“吸热”或“放热”)。
若升高温度,K值减小,则正反应为 反应(填“吸热”或“放热”)。
【问题思考】不同温度时,反应:H2(g)+I2(g)  2HI(g),的浓度平衡常数与温度的关系如下:
2HI(g),的浓度平衡常数与温度的关系如下:

根据平衡常数随温度的大小变化趋势,可以判断上述可逆反应的正方向是______反应
3、判断正在进行的可逆反应是处于平衡状态及反应向何方向进行
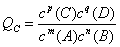 对于可逆反应:mA(g)+ nB(g)
对于可逆反应:mA(g)+ nB(g) pC(g)+ qD(g),在一定的温度下的任意时刻,反应物的浓度和生成物的浓度有如下关系: ,Qc是该反应的浓度商。
pC(g)+ qD(g),在一定的温度下的任意时刻,反应物的浓度和生成物的浓度有如下关系: ,Qc是该反应的浓度商。
Qc<K ,未达到平衡,反应向 进行,
Qc=K ,反应处于平衡状态
Qc>K ,未达到平衡,反应向 进行
【温馨提示】化学平衡常数(K)与浓度商(Qc)的表达式相同,但在表达式中各物质的浓度不同,K值中各物质的浓度必须是平衡状态下的浓度,而Qc值中是在任一时刻的浓度。
【课堂练习】
2、在某温度下,在一容积不变的容器中,反应2A(g)+B(g)  2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol,保持温度和体积不变,对平衡混合物中三者的物质的量做如下调整,试用平衡常数分析平衡移动的方向。
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol,保持温度和体积不变,对平衡混合物中三者的物质的量做如下调整,试用平衡常数分析平衡移动的方向。
A.均减半 B.均加倍 C.均增加1mol D.均减少1mol
4、计算转化率或平衡浓度
依据起始浓度(或平衡浓度)和平衡常数可以计算平衡浓度(或起始浓度),从而计算反应物的转化率。
【阅读】课本30页例1、例2
【课后习题】
1. 在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:

下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大浓度使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
2.氨在国民经济中占有重要的地位,请参与下列探究。
(1)已知在400℃时,N2 (g)+ 3H2(g) 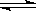 2NH3(g) △H<0的K1=0.5
2NH3(g) △H<0的K1=0.5
400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正 V(N2)逆(填:>、<、=、不能确定)。
(2)已知反应:CO(g)+2H2(g) 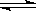 CH3OH (g) △H<0
CH3OH (g) △H<0
a.该反应在一定条件下达到平衡后,在保证H2浓度不变的情况下,增大容器的体积,试根据平衡常数,判断平衡_____________
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
3.在一定温度下,反应1/2H2(g)+ 1/2X2(g) 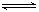 HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)达到平衡时的转化率为多少?
HX(g)的平衡常数为10。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)达到平衡时的转化率为多少?
参考答案
一、化学平衡常数
1、平衡 浓度幂之积 浓度幂之积 K
2、cp(C)·cq(D)/cm(A)·cn(B)
3、温度
4、(1)①越大 越大 完全 越大 ②越小 越小 越小 越小(2)105
5、[指定反应物的起始浓度—指定反应物的平衡浓度]/指定反应物的起始浓度×100%
【问题思考】不相同 K2 =1/K3
三、化学平衡常数的应用
1、正反应方向 逆反应方向
2、吸热 放热
【课堂练习2】
解析:温度不变,化学平衡常数为定值。设容器体积为V,则 K=(4/V)2/[(4/V)2·2/V]=V/2

【课后作业】
1、解析:A项,X的转化率=[(0.1-0.05 )mol/L]/ 0.1 mol/L×100%=50%,A正确;根据表中数据(0.1-0.05)∶(0.2-0.05)∶(0.1-0)=1∶3∶2,可推导出反应式为X+3Y 2Z,将表格的数据代入平衡常数公式进行计算,可知B正确。C项,平衡常数只受温度影响,与浓度或压强无关,C错。
2Z,将表格的数据代入平衡常数公式进行计算,可知B正确。C项,平衡常数只受温度影响,与浓度或压强无关,C错。
答案:C
2.解析:(1)此时体系的QC=c2(NH3)/c(N2).c3(H2)=42/4×23=0.5=K1,故反应处于化学平衡状态,得V(N2)正=V(N2)逆。
(2)此反应的平衡常数公式K=c(CH3OH)/c(CO).c2(H2),H2浓度不变时,增大容器的体积,CH3OH 、CO的浓度减小的倍数相同,故K不变,化学平衡不移动,故答案选C。
答案:(1)= (2)C
3、解析:1/2H2(g)+ 1/2X2(g) 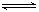 HX(g)的平衡常数K1为10,
HX(g)的平衡常数K1为10,
则HX(g) 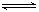 1/2H2(g)+ 1/2X2(g) 的平衡常数K2为1/10,
1/2H2(g)+ 1/2X2(g) 的平衡常数K2为1/10,
设HX(g)分解xmol/L,
HX(g) 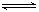 1/2H2(g) + 1/2 X2(g)
1/2H2(g) + 1/2 X2(g)
起始量: 1 0 0
变化量: x 1/2x 1/2 x
平衡量: 1—x 1/2x 1/2 x
则K3= [1/2x·1/2x]/(1—x)= 0.1,得x=0.17,故该温度时HX(g)达到平衡的转化率约为17%.
第二篇:k化学平衡常数