废铝片制备明矾晶体
实验目的
1、 学习实际物品做为原料的处理方法
2、 学习无机制备的基本步骤,称量、加热、
3、 理解晶体生长的条件
实验原理:
(1) 制备明矾的原理
铝屑溶于浓氢氧化钾溶液,可生成可溶性的四羟基合铝(Ⅲ)酸钾K[Al(OH)4],用稀硫酸调节溶液的pH值,将其转化为氢氧化铝,使氢氧化铝溶于硫酸,溶液浓缩后经冷却有较小的同晶复盐,此复盐称为明矾
[KAl(SO4)2·12H2O]。制备中的化学反应如下:
2Al + 2KOH + 6H2O ═ 2 K[Al(OH)4] + 3H2↑
2K[Al(OH)4] + H2SO4 ═ 2Al(OH)3↓ + K2SO4 + 2H2O
2Al(OH)3 + 3H2SO4 ═ Al2(SO4)3 + 6H2O
Al2(SO4)3 + K2SO4 + 24 H2O ═ 2 KAl(SO4)2·12H2O
(2) 晶体生长的条件:适当的浓度,适当的温度
(3) 净水原理
明矾溶于水后电离产生了Al3+,Al3+与水电离产生的OHˉ结合生成了氢氧化铝,氢氧化铝胶体粒子带有正电荷,与带负电的泥沙胶粒相遇,彼此电荷被中和。失去了电荷的胶粒,很快就会聚结在一起,粒子越结越大,终于沉入水底。这样,水就变得清澈干净了。此外氢氧化铝也是一种空隙很多的物质,表面的吸附能很大,可以吸附水里面的沙子,灰尘等。
实验步骤:
明矾的制备:
废铝(2g)加入到盛有50mL 1.5mol?L-1 KOH溶液(自己配!)的烧杯中,加热加快反应*。不再有气泡产生后抽滤,取滤液。将滤液预热后,边加热边滴加9 mol?L-1 H2SO4溶液(1:1 H2SO4,实验室提供!)至沉淀全部溶解,浓缩溶液至50mL左右(过多损失,过少会形成聚铝。32ml溶剂+16ml结晶水=50ml溶液)。放入一次性杯子,自然冷却至室温后一周后观察晶体形貌。
抽滤,用乙醇淋洗后将食盐状晶体粉末放置于空气中晾干,即可得到明矾。(如得到白色聚铝可再加水加热溶解后重新结晶。)
提示:
1、 准备废铝片(易拉罐,药品包装,口服液的瓶盖子,食品包装细致,医用生理盐水玻璃瓶的盖子上的
1
金属等等)废铝片有保护膜或表面氧化,所以需要打磨
2、 两个人一组
3、 调好pH特别重要,请仔细操作
4、*处有氢气生成,同时带有酸气,注意小火加热。
思考题:
1、 整个实验过程中实验现象都有哪些,请你根据化学反应预测一下
2、 用NaOH固体配制50mL 1.5mol?L-1 KOH溶液的方案是什么,是否需要用容量瓶?为什么?
3、 铝片需要剪碎和NaOH溶液反应,为什么?预测一下铝片的大小和反应速度有怎样的关系。
4、 沉淀溶解后浓缩的过程中有什么注意事项?
5、 抽滤装置是什么样的,为什么抽滤速度快,溶液中什么样的固体适合用抽滤的办法进行分离?
6、 用乙醇淋洗固体的目的是什么?不淋洗会怎样呢?
7、 根据溶解度曲线,分析说明析出的固体全是明矾吗?还可能是什么物质?如果要得到纯度高的明矾
的固体,还得怎样的操作呢?(图1 溶解度曲线,注意0℃=273K)
8、 明矾有啥用途呢?举出几个实例。
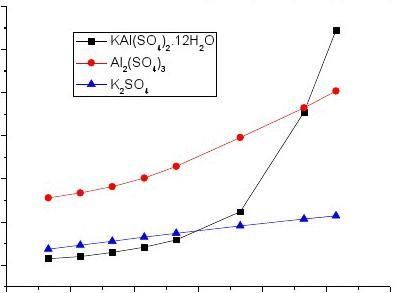
Solubility Curves of KAl(SO).12HO, Al(SO) and KSO4
12010080
Solubility/g6040
20
T/K
图1 K2SO4、Al2(SO4)3和明矾的溶解度曲线
2
第二篇:明矾制备
实验:明矾的制备及其单晶培养
一、 前言:明矾的基本性质与用途
明矾,学名为十二水合硫酸铝钾,又称明矾、白矾、钾矾、钾铝矾、钾明矾,是含有结晶水的硫酸钾和硫酸铝的复盐。其分子式是KAl(SO4)2·12H2O,加合式是K2SO4·Al2(SO4)3·24H2O,相对分子质量为474.39,无色立方,单斜或六方晶体,有玻璃光泽,密度为1.757g/cm3,熔点92.5℃。在64.5℃时失去9个分子结晶水,200℃时失去12个分子结晶水,溶于水,不溶于乙醇。
明矾性味酸涩,寒,有毒。故有抗菌作用、收敛作用等,可用做中药。明矾还可用于制备铝盐、发酵粉、油漆、鞣料、澄清剂、媒染剂、造纸、防水剂等。
明矾净水是过去民间经常采用的方法,它的原理是明矾在水中可以电离出两种金属离子:KAl(SO4)2= K+ + Al3+ + 2SO42-,而Al3+很容易水解,生成胶状的氢氧化铝Al(OH)3:Al3+ + 3H2O = Al(OH)3(胶体)+ 3H+,氢氧化铝胶体的吸附能力很强,可以吸附水里悬浮的杂质,并形成沉淀,使水澄清。所以,明矾是一种较好的净水剂。
二、 实验目的
(1)学会利用身边易得的废铝材料制备明矾的方法;
(2)巩固溶解度概念及其应用;认识铝和氢氧化铝的两性性质;
(3)练习和掌握溶解、过滤、结晶以及沉淀的转移和洗涤等无机制备中常用的基本操作和测量产品熔点的方法。
(4)学习从溶液中培养晶体的原理和方法。
三、实验原理
(1)明矾的制备
将废铝样品溶解于稀氢氧化钾溶液中,值得偏铝酸钾:

在偏铝酸钾溶液中加入过量的浓硫酸,使其生成溶解度较小的复盐明矾(KAl(SO4)2·12H2O)反应式为:

在不同温度下明矾、硫酸铝、硫酸钾的溶解度(单位:g/100gH2O)如下表所示:
表1.1 明矾、硫酸钾、硫酸铝在不同温度下的溶解度

(2)单晶的培养
要使晶体从溶液中析出,从原理上有两种方法。溶解度曲线下方为不饱和区域,若从处于不饱和区域的状态出发,要使晶体析出,一种方法是保持浓度一定,降低温度;另一方法是保持温度一定,增加浓度。
(3)制备工艺路线
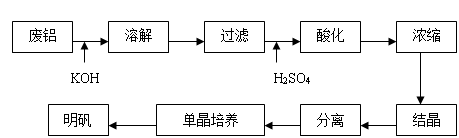
图2.1 明矾制备流程图
三、 仪器和试剂
(1) 仪器:电子天平、烘箱、布氏漏斗、抽滤瓶、分光光度计、滴定管、容量瓶。
(2) 试剂:氢氧化钾(1.5 mol/L)、硫酸(f)、氨水(1+1)、盐酸(1+1)、EDTA(0.02205mol/L)、ZnAc2(0.01974mol/L)、二甲酚橙指示剂、20%六次甲基四胺。
四、实验步骤及数据处理
1、明矾的制备
 首先清除废铝表层的污染物,洗净,干燥,称重。用1.5mol/L的KOH溶液约50mL溶解2.0842g的废铝,抽滤,按化学计量关系滴加的3 mol/L硫酸,适当加热至沉淀溶解,浓缩,冷却结晶,抽滤,得到明矾晶体25.2280g。
首先清除废铝表层的污染物,洗净,干燥,称重。用1.5mol/L的KOH溶液约50mL溶解2.0842g的废铝,抽滤,按化学计量关系滴加的3 mol/L硫酸,适当加热至沉淀溶解,浓缩,冷却结晶,抽滤,得到明矾晶体25.2280g。
产品回收率为
2、产品定量鉴定
2.1铝离子的定量检测
称取1.0182产品,溶解,用蒸馏水定容至250mL,摇匀。取三个洁净的锥形瓶,分别移取上述产品溶液20mL,0.02205mol?L-1EDTA溶液15mL及2滴二甲酚橙指示剂,小心滴加(1+1)NH3?H2O调至溶液恰呈紫红色,然后滴加2滴(1+1)HCl。将溶液煮沸1min,冷却,加入20mL 20%六次甲基四胺溶液,此时溶液应呈黄色,用醋酸锌标准溶液(0.01974mol?L-1)滴定至溶液由黄色恰变为紫红色即为终点。根据醋酸锌标准溶液所消耗的体积,计算明矾中Al3+的百分含量。
表1.2 产品中Al的定量检测
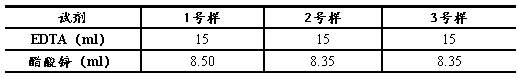
由于Al3+和Zn2+同EDTA的络合反应,计量系数比均为1∶1,由此可用公式如下公式计算产品中Al3+含量:

根据上述公式计算产品中铝离子含量为:
表1.3 产品中Al3+的质量百分比

2.2 硫酸根离子的定量检测
采用比浊法测定硫酸根离子的含量,首先,称取0.091g硫酸钾固体,配置成100mL浓度为500μg/mL的标准硫酸钾溶液。称取1.018gKAl(SO4)2·12H2O晶体配置成250mL的样品溶液。分别量取0、1.0、2.0、3.0、4.0mLK2SO4标准溶液以及0.5、1.0mL产品溶液移入10mL的比色管中,然后分别加入5ml浓度为1g/mL的 BaCl2溶液,用蒸馏水定容。用分光光度计测量标准系列以及样品的吸光度(波长采用420nm)。
表1.3 产品中硫酸根离子的定量检测

硫酸钡悬浊液的吸光光谱图绘制如下:
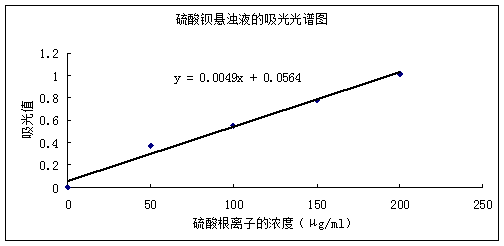
图2.2 硫酸钡悬浊液的吸光光谱图
由表2.3的结果可计算出样品中硫酸根离子的质量百分比为:
表2.4产品中SO42-的质量百分比

五、实验相关注意事项
1、 抛光铝片时,小心割伤手。
2、 溶解铝片时,有氢气产生,应在通风橱中进行,实验室中严禁明火!
3、 加硫酸制氢氧化铝时,反应放热,可以在冰水中进行。
4、 溶液最终体积不易太大,以免溶液未达到饱和,晶体难以析出。
5、 比色法测定硫酸钡时,波长任选,测定前摇匀溶液,确保硫酸钡均匀分散在溶液中。
6、 建议硫酸根标准溶液浓度为500μg/mL。
7、 在晶体培养时,细绳系好晶钟后,液面以下的绳表面要涂上少许凡士林,有利于晶体以晶种为中心开始生长。
