物 理 化 学 实 验 报 告

实 验 名 称: 液体饱和蒸气压的测定
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级:
姓 名: 学 号:
指 导 教 师:
日 期:
一、实验目的
1、掌握用等位计测定乙醇在不同温度下的饱和蒸汽压。
2、学会用图解法求乙醇在实验温度范围内的平均摩尔蒸发焓与正常沸点。
二、实验原理
1、纯物质的蒸气压随温度的变化可用克拉贝龙方程来表示:
dp/dT =△vapHm /T△Vm (1)
将(1)式积分得克劳修斯-克拉贝龙方程:
㏑(P/Pa) = (-△vapHm /R)×(1/T)+ C (2)
由(2)式可见,实验测定不同温度T下的饱和蒸气压p,以ln(p/[p])对1/T作图,得一直线,求得直线的斜率m和截距C,则乙醇的平均摩尔蒸发焓为:
△vapHm =-m×R×[△H]/[R] (3)
3、习惯上把液体的蒸气压等于101.325kPa时的沸腾温度定义为液体的正常沸点,由(2)式还可以求乙醇的正常沸点。本实验采用静态法直接测定乙醇在一定温度下的蒸气压。
三、实验仪器与试剂
1、主要仪器:DPCY-2型饱和蒸汽压教学实验仪一套,HK-1D型恒温水槽一套,WYB-1型真空稳压包一个,稳压瓶一个,安全瓶一个。
2、主要试剂:无水乙醇(A.R)。
四、实验装置图
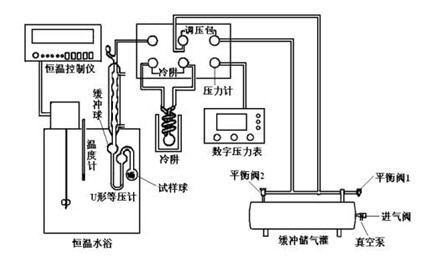
DPCY-2C型饱和蒸气压教学实验仪面板
五、实验步骤
1、读取并记录下室温和大气压。
2、装样:从加样口加2/3体积的无水乙醇,并在U型管内装入一定体积的无水乙醇.
3、教学实验仪置零:打开教学实验仪电源,预热5分钟,选择开关打到kPa,按下板上的置零键,显示值为00.00数值。
4、系统气密性检查:除真空泵前的安全活塞通大气外,其余活塞都关上,抽真空4~5分钟,关闭三通活塞,若数字压力计上的数字基本不变,表明系统不漏气,可进行下步实验否则应逐段检查,消除漏气因素。
5、排除球管上方空间内空气:用WYB-1型真空稳压包控制抽气速度,抽气减压气泡逸出的速度以一个一个地溢出为宜至液体轻微沸腾3~5分钟,压力显示约-94kPa。
6、饱和蒸汽压的测定:旋转稳压瓶上的直通活塞H,缓缓放入空气,直至B、C管中液面平齐,关闭H,记录温度与压力。再将恒温槽升高5℃,当待测液再次沸腾,再放入空气使B、C液面再次平齐,记录温度和压力。依次测5个值。
7、结束实验:实验结束后再读一次大气压。关闭电源,打开真空稳压包上中间阀门,将体系放入空气,待等位计内乙醇冷却后,关掉冷凝器的冷却水。整理好仪器装置,但不要拆装置。
六、数据记录与处理
室温: 14℃ ;
大气压(实验前): 101.14 kPa , 大气压(实验后): 101.18 kPa ;
大气压(平均值): 101.16 kPa 。
表6-1 不同温度下乙醇的蒸气压
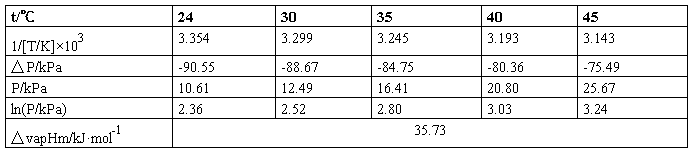
2、以㏑(P/kPa)—1/(T/K)×103作图,

6-2、乙醇的温度-蒸气压关系图
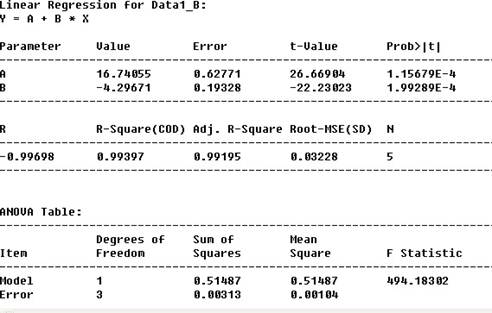
由图6-2可知,直线的斜率m为-4.29671,截距为16.74055。
所以-△vapHm /R= -4.29671,即得△vapHm =35.73kJ·mol-1
3、当液体的蒸气压为101.325 kPa时,代入一次性函数
㏑(P/KPa) = (-△vapHm/R)×(1/Tb*10^3)+ C,
即㏑101.325 = -4.29671×(1/T*10^3) +16.74055,
得:Tb = 354.45K ,即tb=81.30℃
4、误差分析 :
△vapHm的相对误差=|(35.73-42.59)/42.59︳=0.1611
T的相对误差=|(78.4-81.30)/78.4|=0.0370
七、注意事项
1、抽真空前后,与真空泵连接的安全瓶,都要通大气。抽真空只要一次,第一次抽真空就要压力显示大约为-94kPa;
2、严格控制抽真空速度,不可过快。观察U型管气泡不要成串。
3、第一次液体要沸腾,但不能爆沸,之后的每一次改变温度不需要沸腾,每次记录压力时应使液面平齐后再等2~3min再读数。
4、实验结束后,一定要用真空稳压包上中间阀门缓慢通大气,防止封闭液过多流入球内。
八、结果与讨论
1、U型管中的乙醇液体,由于挥发等作用,其量偏少,使的实验时的真空度读数偏小,从而影响实验结果,造成数据的误差。
2、本次实验,测得的乙醇饱和蒸汽压与理论值相比,是比较偏小的,造成误差的主要原因是操作的准确性、仪器气密性等;而测得的乙醇沸点也是偏高的,造成此误差的原因主要来自操作准确性、数据拟合等。
第二篇:饱和蒸汽压的测定实验报告



实验题目:液体饱和蒸汽压的测定
学 院: 化学与化工学院
专 业: 生物工程
年 级: 112班
学 号: 1108110358
学生姓名: 孙宇
指导教师: 吴玉娟
20## 年 3月 30 日
(一) 实验目的
1. 明确液体饱和蒸气压的定义,了解纯液体的饱和蒸气压与温度的关系以及克劳修斯-克拉佩龙方程的意义。、
2. 掌握用静态法测定液体饱和蒸气压的方法,学会用图解法求被测液体在试验温度的范围内的平津摩尔气化焓。
3. 初步掌握真实试验技术,了解恒温槽及等压计的使用方法。
(二) 基本原理
饱和蒸汽压:蒸气分子向液面凝结和液体分子从液面逃逸的速度相等,此时液面上的蒸气压力就是液体再此温度时的饱和蒸气压。
摩尔汽化焓:一定温度下,蒸发1mol液体所吸收的热量称为该温度下液体的摩尔汽化焓。
液体的蒸汽压与温度有关。温度升高,蒸气压增大。
沸点:当蒸气压等于外界压力时,液体便沸腾。此时的温度称为沸点。
外压不同时,液体的沸点亦不同。当外压为1atm是液体的沸点称为该液体的
正常沸点。
液体的饱和蒸汽压与温度的关系可用克劳佩龙方程表示:
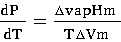
积分上式得:

【P】为压力的量纲,即pa; C为积分常数。由式可以看出,测定不同温度T
液体的蒸汽压P,以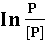 对1/T作图,应为一直线,直线的斜率为
对1/T作图,应为一直线,直线的斜率为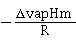 ,
,
由直线斜率可求算液体的摩尔蒸发焓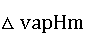 。
。
本实验采用静态法利用等压计测定乙醇在不同温度下的饱和蒸气压。
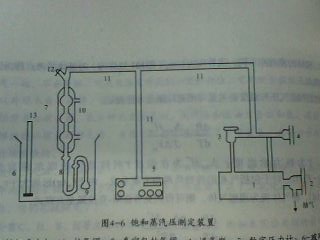
本实验采用静态法利用等压计测定乙醇在不同温度下的饱和蒸。实验装置如
所示。U型管内用样品本身做液封。在某一温度下若小球液面上方仅有被测物
的蒸气,那么在等压计U型管右支液面上所受到的压力就是其蒸汽压。当这
压力与U型管左支液面上的空气的压力达平衡时,就可以与等压计相接的压
机测出被测样品在此温度下的饱和蒸气压。
(三) 实验主要仪器及名称
饱和蒸气压测量装置教学试验仪1套(包括恒温水槽1台、等压计1支、数字压力计1台);真空泵1台及附件;精密温度温差测量仪(JTD-2A)1台;乙醇(AR)
(四)实验步骤
1.读取实验室的大气压和室温,记录。
2. 打开饱和蒸气压测定教学试验仪电源开关,预热5min后,调量纲旋钮至“kpa”档。使饱和蒸气压测定教学试验仪通大气,再按下“清零”键。
3.关闭大气阀,打开减压阀,设定温度30℃,进行加热。当发现气泡成串冒出时,乙醇开始沸腾,关闭减压阀,沸腾一会后,缓慢开启大气阀(增压阀),直至等压计U型管倆端液面平齐,迅速关闭增压阀,记录此时饱和蒸汽压教学以上的压差值△p。
4.调节恒温水浴槽的温度,市值上升5℃,待系统恒温后,液体将再次沸腾;在缓慢开启增压阀,缓缓放入空气,直至等压计U型管俩端液面平齐。迅速关闭旋塞,记录此时饱和蒸气压教学试验仪上的压差值△p。
5.重复4中的操作,直至温度上升至60℃,则停止加热。
6.实验结束后,打开减压阀和增压阀,关闭教学实验仪,恒温水浴槽的开关,将系统排空,然后关闭真空泵,切断电源。
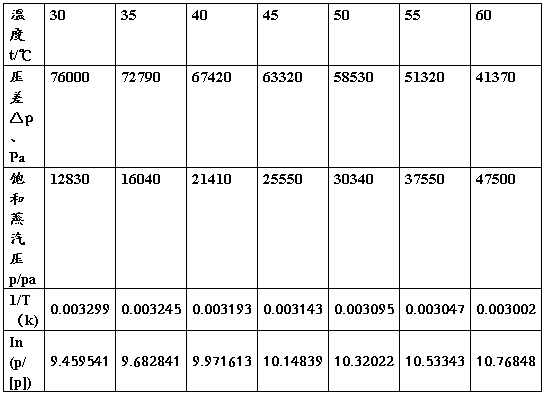
(五)数据记录表
1.温度: 18.1℃ 大气压:88.83KPa
2.以In(p/[p])对1/T(k)作图,有直线的斜率求出△vapHm。
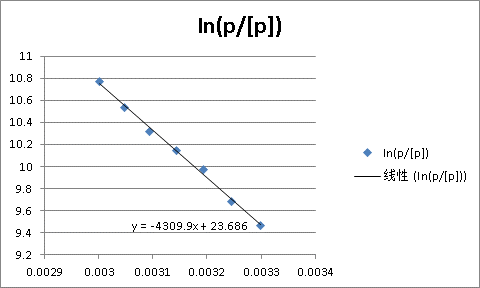
根据Inp= +C得
+C得
斜率=-4309.9=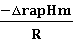
所以△rapHm =4309.9R=35834.66355J/mol
(六)问题讨论
1.本实验产生误差的因素有哪些?
答:当地大气压,判断液面是否相平的标准,液面相平时数据的采集都会对实验结果造成影响。
2.数字压力计中所读的压差数值是否就是纯液体的饱和蒸气压?
答:不是,压差值是外压减去内压,即饱和蒸气压。
3.为什么实验完毕后必须使体系和真空泵与大气相通才能关闭真空泵?
答:如果不与大气相通,球管内的液体可能会被吸入到缓冲储气罐。
4.为什么等压中的U型管内要用样品本身做液封?
答:等压计中的U形管用样品本身作液封,使得系统中液体所受压力只与大气压有关。
5.开启旋塞将空气放入系统时,放的过多应如何办?
答:放的过多可以打开减压阀,进行减压。
6.稳压包的作用是什么?
答:稳压包的作用是稳定蒸气压力,缓冲作用。
7.气化热与温度有无关系?
答:使物体气化,没气化1克材料所需的热量叫该材料的气化热,所以跟物体的初温度有关。
8.等压计的原理是什么?为什么要等到等压计俩端液面平齐时,才能记录此时温度及压差值?
答:等压计原理是等压原理。等到等压计俩端液面平齐时,代表俩侧的压力相等,此时液面俩侧的压力才相等。
9.克-克方程在什么条件下才应用(即由克拉佩龙方程导出克-克方程的条件)
答:可由克拉佩龙方程导出克-克方程,克-克方程是在克拉佩龙方程基础上作了近似处理而得到的,只适用于凝聚相(液相或固相)与气相两相平衡。
