矿泉水硬度的测定
姓名:祖广权 专业:应 化 班级:101 学号:2010014032
实验日期:2013年 06 月19日 成绩:
摘要:水是人类最为宝贵的自然资源,也是人类以及所有动植物生存的基础。现阶段水污染却成了全世界的主要问题。污染水给工业、农业及生命健康带来了很大的危害。本实验介绍了以EDTA络合滴定对矿泉水总硬度,钙、镁硬度的测定方法。
关键词:水 硬度 EDTA 滴定
1引言
水硬度是水质的一个重要监测指标,通过监测可以知道其是否可以用于工业生产及日常生活,如硬度高的水可使肥皂沉淀使洗涤剂的效用大大降低,纺织工业上硬度过大的水使纺织物粗造且难以染色;烧锅炉易堵塞管道,引起锅炉爆炸事故;高硬度的水,难喝、有苦涩味,饮用后甚至影响胃肠功能等;喂牲畜可引起孕畜流产等。因此水硬度的测定方法研究是不容忽视的。目前的分析测定方法很多,主要可分为化学分析法和仪器分析法,其中化学分析法以EDTA络合滴定法为主。[1]
EDTA络合滴定法是一种普遍使用的测定水的硬度的化学分析方法。它是在一定条件下,以铬黑T为指示剂,NH3·H2O—NH4Cl为缓冲溶液,EDTA与钙、镁离子形成稳定的配合物,从而测定水中钙、镁总量。但是该方法易产生指示剂加入量、指示终点与计量点、人工操作者对终点颜色的判断等误差。
在分析样品时,如水样的总碱度很高时,滴定至终点后,蓝色很快又返回至紫红色,此现象是由钙、镁盐类的悬浮性颗粒所致,影响测定结果。可将水样用盐酸酸化、煮沸,除去碱度。冷却后用氢氧化钠溶液中和,再加入缓冲溶液和指标剂滴定,终点会更加敏锐。[2]由于指示剂铬黑T易被氧化,加铬黑T后应尽快完成滴定,但临终点时最好每隔2~3 s滴一滴并充分振摇;并且在缓冲溶液中适量加入等当量EDTA镁盐,使终点明显;滴定时,水样的温度应以20~30℃为宜。[3]
通常采用间接法配制EDTA标准溶液。标定EDTA溶液的基准物有Zn、ZnO、CaCO3、Bi、Cu、MgSO4 · 7H2O、Ni、Pb 等。选用的标定条件应尽可能与测定条件一致,以免引起系统误差。如果用被测元素的纯金属或化合物作基准物质,就更为理想。本实验采用MgSO4 · 7H2O作基准物标定EDTA,以铬黑T(EBT)作指示剂,用pH ≈10 的氨性缓冲溶液控制滴定时的酸度。因为在pH ≈10 的溶液中,铬黑T 与Mg2+ 形成比较稳定的酒红色螯合物(Mg—EBT),而EDTA与Mg2+能形成更为稳定的无色螯合物。因此,滴定至终点时,EBT 便被EDTA 从Mg—EBT中置换出来,游离的EBT 在pH = 8~11 的溶液中呈蓝色。
测定水的总硬度就是测定水中钙、镁离子的总含量,滴定时,Fe3+、Al3+等干扰离子可用三乙醇胺予以掩蔽;Cu2+、Pb2+、Zn2+等重属离子,可用KCN、Na2S或巯基乙酸予以掩蔽。[4-6]
水的硬度有多种表示方法,本实验要求以每升水中所含Ca2+、Mg2+总量(折算成CaO的质量)表示,单位mg·L-1。[7]
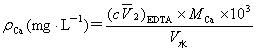
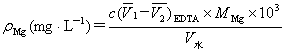
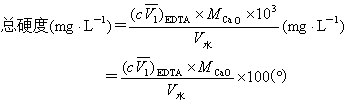
2实验
2.1仪器与试剂
电子天平(0.1mg);容量瓶(100mL);移液管(20mL);酸式滴定管(50mL);锥形瓶(250mL)等。
EDTA;MgSO4?7H2O;NH3-NH4Cl缓冲溶液(pH=10.0);1mol?L-1NaOH;铬黑T指示剂;钙指示剂等。
2.2实验步骤
2.2.1 0.01mol ?L-1 EDTA 标准溶液的配制
称取1.8 ~ 2g固体EDTA于烧杯中,用少量水溶解,冷却后转置500ml试剂瓶,加去离子水,稀释至500ml,摇匀,备用。
2.2.2 镁标准溶液的配制
准确称取MgSO4?7H2O基准试剂0.25~0.3g(或称取无水MgSO4;所配制基准试剂的浓度最好为0.01 mol ?L-1,或在0.01~0.02 mol ?L-1之间),置于小烧杯中,加30 mL蒸馏水溶解,定量转移到100mL 容量瓶中,加水稀释至刻度,摇匀。计算其准确浓度。
2.2.3 EDTA 标准溶液浓度的标定
用移液管吸取镁标准溶液25.00mL 置于250mL 锥形瓶中,加5mL pH ≈10 的NH3-NH4Cl缓冲溶液,加入铬黑T指示剂少许,用EDTA 标准溶液滴定至溶液由酒红色恰变为蓝色,即达终点,平行测定三次。根据消耗的EDTA标准溶液的体积,计算EDTA的浓度。
2.2.4 水的总硬度测定
2.2.4.1 EDTA的稀释
用移液管取40mlEDTA溶液于250ml容量瓶中,定容,备用。
2.2.4.2 水总硬度测定
用100mL移液管或量筒取50mL水样于250mL锥形瓶中,加氨性缓冲溶液5mL, EBT指示剂少许,用EDTA标准溶液滴定,至溶液由酒红色变为蓝色即为终点,记录所消耗EDTA的体积V1。平行测定3次(现测现配)。
2.2.5 钙的测定
取与步骤4等量的水(50ml)量于250mL锥形瓶中,加5mL 1mol?L-1NaOH,[8-9] 钙指示剂少许,用EDTA标准溶液滴定至溶液由酒红色变为蓝色即为终点,记录所消耗EDTA的体积V2。平行测定3次。
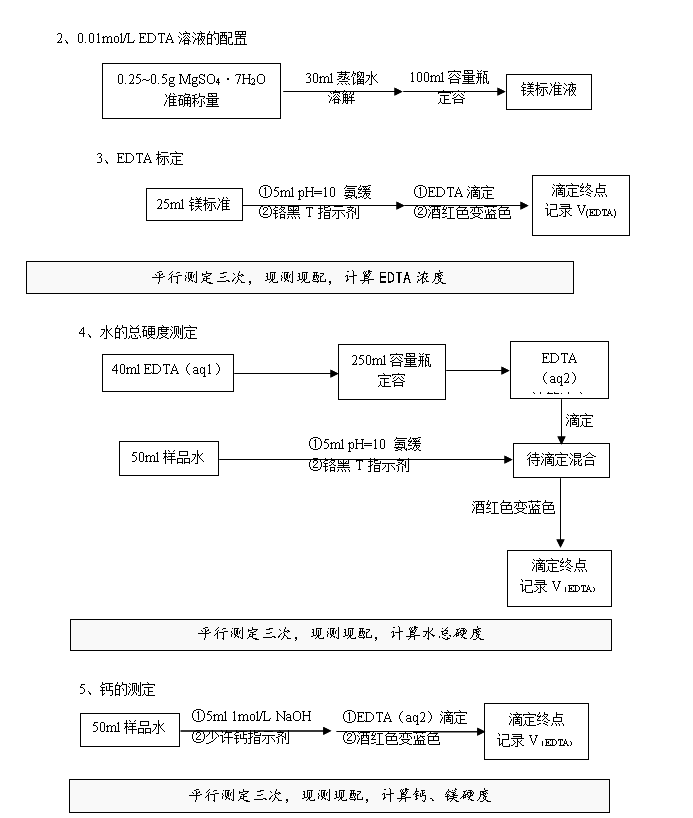
3 实验流程
(见附表1)
4 数据记录与处理
4.1 数据记录
(原始数据见附表图2)
mEDTA = 1.86g
1、EDTA的标定(V(MgSO4)=25ml)
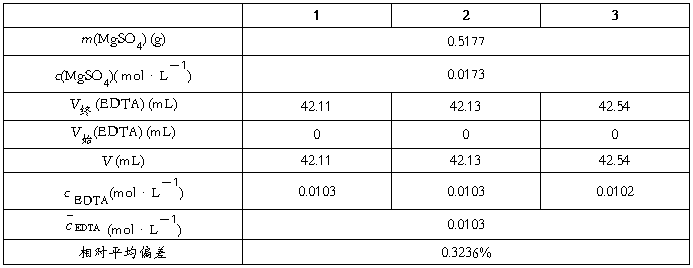
2、水的硬度的测定
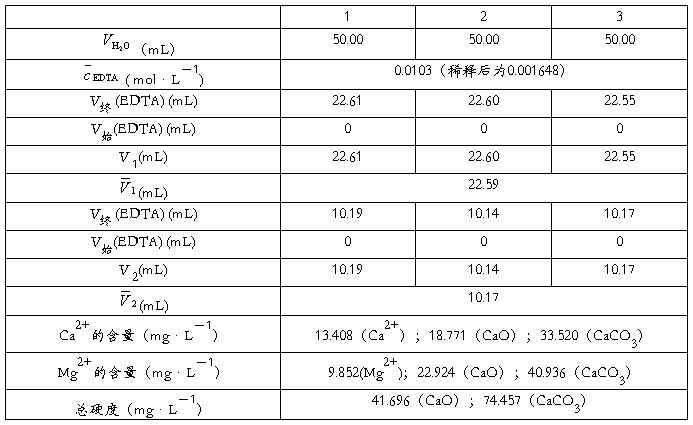
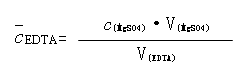 4.2 数据处理
4.2 数据处理
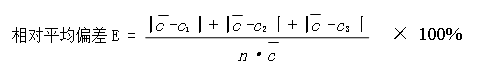
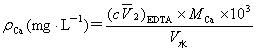
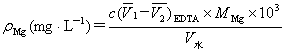
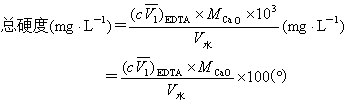
5 结果与讨论
5.1 结果
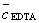 = 0.0103(mol/L) 稀释后:
= 0.0103(mol/L) 稀释后: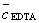 = 0.001648(mol/L)
= 0.001648(mol/L)
总硬度:74.457(CaCO3);41.696(CaO)
Ca2+含量:13.408(Ca2+);18.771(CaO);33.520(CaCO3)
Mg2+含量:9.852(Mg2+);22.924(CaO);40.936(CaCO3)
5.2 讨论
(1)镁标准溶液最好是0.01mol/L,与EDTA等浓度,会较准确。
(2)本实验样品水中Ca2+、Mg2+含量较少,0.01mol/L EDTA溶液相对来说浓度较大,所以需要稀释,一般稀释后滴定时所消耗的V(EDTA)在20-30ml之间最佳。
(2)滴定终点时要慢,因为络合比较慢,过快会使结果偏高。
(3)指示剂要适量,一般3-4滴。
(4)加入NaOH是为了屏蔽Mg2+,使其只测Ca2+。
(5)平行实验时,样品混液需现测现配。因为在NH4+存在下,Mg2+与CO32-生成沉淀影响测定,所以现测现配。
6 注意事项
(1)络合滴定速度不能太快,特别是近终点时要逐滴加入,并充分摇动。因为络合反应速度较中和反应要慢一些;
(2)在络合滴定中加入金属指示剂的量是否合适对终点观察十分重要,应在实践中细心体会;
(3)络合滴定法对去离子水质量的要求较高,不能含有Fe3+、Al3+、Cu2+、Mg2+等离子。
(3)平行实验时,样品混液需现测现配。
7 参考文献
【1】沈永玲,吴泓毅,水硬度的测定方法,广州化工,2011:39(20),20-21,45
【2】宋永乐,徐衍忠,王均乐等,测定水中总硬度应该注意的几个问题[J].环境检测管理与技术,1998,10(1):47-48.
【3】金中华等.[J].内蒙古环境保护,2000,12(1):20-21.
【4】侯吾爱,滴定速度对水硬度测定结果准确度影响的探讨,河北化工,2011:18,52-55
【5】宋建华,李黄达,水硬度测定时铁(III)离子干扰现象的探讨,上海轻工业高等专科学校学报,1996:17(1),50-51
【6】韦寿莲,叶泽龙,林泽卯,影响水硬度测定的若干因素,肇庆学院学报,2009:30(5),58-62
【7】陈西伟,酿造工艺水硬度的测定,安徽教育学院学报,2003:21(3),48-49
【8】范福南,马有臣,王治科等,EDTA容量法连续测定钙和镁的改进[J].2002.14(4):254-255.
【9】金中华,刘海洋,内蒙古环境保护,2000:12(1),20-21
 附表1:
附表1:
第二篇:水的总硬度及钙、镁含量的测定
实验名称:水的总硬度及钙、镁含量的测定
实验试剂:
(1)以CaCO3为标准物质所用的试剂。
乙二胺四乙酸钠(固体,A.R.) (分析纯/500ml的一瓶); CaCO3(固体,A.R.或G.R.) (分析纯/500g的一瓶) HCl溶液(1:1) (分析纯/500ml的一瓶); 氨水(1:1) (分析纯/500ml的一瓶); 镁溶液(溶解1gMgSO4·7H2O于水中,稀释至 200ml) (分析纯/500ml的一瓶);
钙指示剂(固体指示剂,1g钙紫红与100g NaCl 混合均匀)
-1 NaOH溶液(100g·L) (分析纯/500ml的一瓶);
(2 )以ZnO为基准物质时所用的试剂
ZnO(A.R.或G.R.) (分析纯/500g的一瓶) HCl溶液(1:1) (分析纯/500ml的一瓶); 氨水(1:1) (分析纯/500ml的一瓶); 二甲酚橙指示剂 (分析纯/500ml的一瓶);
-1 六亚甲基四胺溶液(200g·L) (分析纯/500ml的一瓶);
实验仪器: 托盘天平 细口瓶 表面皿
容量瓶 锥形瓶 酸式滴定管
特能:实验共分16个小组,因此以上玻璃仪器均为16套。 环境:实验共分20个小组,因此以上玻璃仪器均为20套。
.
