 宁 波 工 程 学 院
宁 波 工 程 学 院
物理化学实验报告
专业班级 姓 名 序 号
同组姓名 指导老师 实验日期 2012.3.20
实验名称 实验四 蔗糖水解反应速率常数的测定
一、实验目的
1. 了解蔗糖水解反应体系中各物质浓度与旋光度之间的关系。
2. 测定蔗糖水解反应的速率常数和半衰期。
3.了解旋光仪的基本原理,掌握其正确的操作技术。
 二、实验原理
二、实验原理
反应速率只与某反应物浓度的一次方成正比的反应称为一级反应,速率方程可由下式表示:
—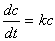
式中c为时间t时的反应物浓度,k为反应速率常数。
积分可得: lnc=-kt + lnc0
c0为反应开始时反应物浓度。
当c= c0/2时,对应t可用t1/2表示,称为反应的半衰期,即反应物浓度反应掉一半所用时间,得一级反应的半衰期为: t1/2=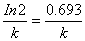
蔗糖在水中转化成葡萄糖与果糖,其反应为:
C12H22O11 + H2O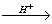 C6H12O6 + C6H12O6
C6H12O6 + C6H12O6
(蔗糖) (葡萄糖) (果糖)
它属于二级反应,在纯水中此反应的速率极慢,通常需要在H+离子催化作用下进行。由于反应时水大量存在,尽管有部分水分子参与反应,仍可近似地认为整个反应过程中水的浓度是恒定的,而且H+是催化剂,其浓度也保持不变。因此蔗糖转化反应可看作为一级反应。
蔗糖及其转化产物,都具有旋光性,而且它们的旋光能力不同,故可以利用体系在反应进程中旋光度的变化来度量反应进程。
测量物质旋光度所用的仪器称为旋光仪。溶液的旋光度与溶液中所含旋光物质的旋光能力,溶剂性质,溶液浓度,样品管长度及温度等均有关系。当其它条件均固定时,旋光度α与反应物浓度c呈线性关系,即
α=Kc
式中比例常数K与物质旋光能力,溶剂性质,样品管长度,温度等有关。
物质的旋光能力用比旋光度来度量,比旋光度用下式表示:
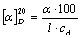
式中“20”表示实验时温度为20℃,D是指用纳灯光源D线的波长(即589毫微米),α为测得的旋光度,l为样品管长度(dm),cA为浓度(g/100mL)。
作为反应物的蔗糖是右旋性物质,其比旋光度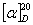 =66.6°;生成物中葡萄糖也是右旋性物质,其比旋光度
=66.6°;生成物中葡萄糖也是右旋性物质,其比旋光度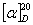 =52.5°,但果糖是左旋性物质,其比旋光度
=52.5°,但果糖是左旋性物质,其比旋光度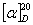 =-91.9°。由于生成物中果糖的左旋性比葡萄糖右旋性大,所以生成物呈左旋性质。因此随着反应的进行,体系的右旋角不断减小,反应至某一瞬间,体系的旋光度可恰好等于零,而后就变成左旋,直至蔗糖完全转化,这时左旋角达到最大值α∞。
=-91.9°。由于生成物中果糖的左旋性比葡萄糖右旋性大,所以生成物呈左旋性质。因此随着反应的进行,体系的右旋角不断减小,反应至某一瞬间,体系的旋光度可恰好等于零,而后就变成左旋,直至蔗糖完全转化,这时左旋角达到最大值α∞。
设最初系统的旋光度为 α0=K反cA,0 (t=0,蔗糖尚未水解) (1)
最终系统的旋光度为 α∞=K生cA,0 (t=∞,蔗糖已完全水解) (2)
当时间为t时,蔗糖浓度为cA,此时旋光度为αt
αt= K反cA+ K生(cA,0-cA) (3)
联立(1)、(2)、(3)式可得:
cA,0=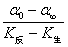 =K′(α0-α∞) (4)
=K′(α0-α∞) (4)
cA= = K′(αt-α∞) (5)
= K′(αt-α∞) (5)
将(4)、(5)两式代入速率方程即得:
ln(αt-α∞)=-kt+ln(α0-α∞)
我们以ln(αt-α∞)对t作图可得一直线,从直线的斜率可求得反应速率常数k,进一步也可求算出t1/2。
三、实验仪器、试剂
仪器:旋光仪,停表,恒温水浴一套,移液管(50mL),磨口锥形瓶(100mL),烧杯(100mL),台秤,洗耳球
试剂:蔗糖(AR),盐酸 (3mol/L,AR)
四、实验仪器装置

五、实验步骤
(一)旋光仪的校正
1.了解旋光仪的构造、原理,掌握其使用方法(见附录)。
2.开启水浴恒温水槽的电源开关,并将水浴恒温槽的温度控制在60℃。
3.蒸馏水为非旋光性物质,可用来校正仪器的零点(即α=0时,仪器对应的刻度)。洗净样品管,将样品管一端盖子打开,转入去离子水,然后盖上玻璃片,此时管内不应有空气泡存在,再旋上套盖,使玻璃片紧贴旋光管,勿使漏水。但必须注意旋紧套盖时,不能用力过猛,以免压碎玻璃片,用滤纸擦干样品管,再用擦镜纸将样品管两端的玻璃片擦干净。放入旋光仪,打开电源,预热5-10min,钠灯发光正常。调目镜聚焦,使视野清晰;调检偏镜至三分视野暗度相等为止,记录游标(右边)刻度为检偏镜旋角,记录仪器零点。读数注意0度以下的实际旋光度(读数-180)。读数三次取平均值,即为零点,用来校正仪器的系统误差。
(二)测定
1、 配制蔗糖溶液:用天平称取10克蔗糖放入烧杯中,加蒸馏水溶解后转移到50ml容量瓶中,稀释至刻度。
2、用50ml移液管移取50mlHCL溶液放入蔗糖水溶液,边放边振荡,当HCL溶液放出一半时按下秒表开始计时(注意:秒表一经启动,勿停直至实验完毕)。迅速用反应混合液将样品管洗涤三次后,将反应混合液装满样品管,擦净后放入旋光仪,测定规定时间的旋光度。测得第一个数据时间应该为反应开始的前三分钟内。测量时先将三分视场调节到全暗,再记录时间(注意时间要记录准确,以实际反应时间为准),后读数。分别记录5min、10min、15min、20min、25min、30min、40min、50min、60min的旋光度。
3、α∞的测量:测定过程中,可将剩余的反应混合物放入60℃恒温槽中加热30min,使反应充分后,冷却至室温后测定体系的旋光度,连续读数三次平均值。
由于反应液的酸度很大,因此样品管一定要擦干净后才能放入旋光仪内,以免酸液腐蚀旋光仪,实验结束后必须洗净样品管。
五、数据记录与处理
HCl浓度: 3mol/L ;零点:-0.05 ;α∞: -3.20 。

以ln(αt—α∞)对t作图,并由直线斜率求速率常数k1。
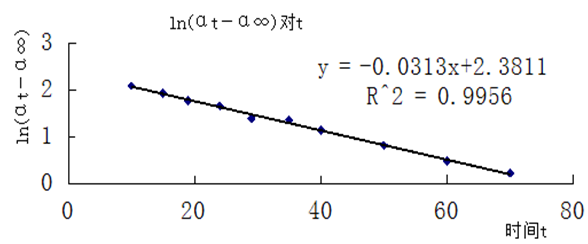
由图可得,斜率k=-0.032316,所以k1=0.0313min -1=5.217×10-4s-1
t1/2= ln 2 /k1 =0.693 / k1 = 0.693 / 5.217×10-4=1.328×10-3s
六、结果讨论
本实验是测定蔗糖水解反应速率常数,实验过程中应该注意:
1、 装样品时,旋光管管盖旋至不漏液体即可,不要用力过猛,以免压碎玻璃片。
2、 在测定α∞时,通过加热使反应速度加快转化完全。但加热温度不要超过60℃。
大约60min后基本分解完全。
3、由于酸对仪器有腐蚀,操作时应特别注意,避免酸液滴漏到仪器上,实验结束后必须将旋光管洗净。
实验过程中可能出现的误差原因分析:
1、在最开始旋光仪的调解时不准确,导致读数不准确。
2、由于蔗糖没有水解完全,测量无限水解时的旋光度偏高。
3、仪器自身存在一定的误差。
第二篇:实验八__蔗糖水解反应速率常数的测定
物理化学实验报告
序号:
学生姓名:
学号:
学院: 化学化工学院
班级: 10级 制药班
专业: 制药工程
指导老师: 张建策
实验名称: 蔗糖水解反应速率常数的测定
实验日期: 20##年5月9日
实验室: 7408
同组者:
实验八 蔗糖水解反应速率常数的测定
一、实验目的
1. 根据物质的光学性质研究蔗糖水解反应,测定其反应速率常数。
2. 了解旋光仪器仪的基本原理,掌握其使用方法。
二、实验原理
蔗糖在水中转化成葡萄糖与果糖,其反应为:
C12H22O11 + H2O C6H12O6 + C6H12O6
C6H12O6 + C6H12O6
(蔗糖) (葡萄糖) (果糖)
它属于二级反应,在纯水中此反应的速率极慢,通常需要在H+离子催化作用下进行。由于反应时水大量存在,尽管有部分水分子参与反应,仍可近似地认为整个反应过程中水的浓度是恒定的,而且H+是催化剂,其浓度也保持不变。因此在一定浓度下,反应速度只与蔗糖的浓度有关,蔗糖转化反应可看作为一级反应。
一级反应的速率方程可由下式表示:
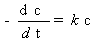

式中:c为蔗糖溶液浓度,k为蔗糖在该条件下的水解反应速率常数。
令蔗糖开始水解反应时浓度为c0,水解到某时刻时的蔗糖浓度为ct,对上式进行积分得:
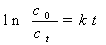
该反应的半衰期与k的关系为:
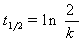
蔗糖及其转化产物,都具有旋光性,而且它们的旋光能力不同,故可以利用体系在反应进程中旋光度的变化来度量反应进程。
测量物质旋光度所用的仪器称为旋光仪。溶液的旋光度与溶液中所含旋光物质的旋光能力,溶剂性质,溶液浓度,样品管长度及温度等均有关系。当温度、波长、溶剂一定时,旋光度的数值为:
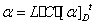 或
或 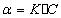
式中L为液层厚度,即盛装溶液的旋光管的长度;C为旋光物质的体积摩尔浓度;[α]Dt为比旋光度;t为温度;D为所用光源的波长。
在其他条件不变的情况下,旋光度α与反应物浓度C呈正比。即
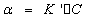
比例常数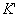 与物质旋光能力,溶剂性质,样品管长度,光源的波长,溶液温度等有关。可见,旋光度与物质的浓度有关,且溶液的旋光度为各组分旋光度之和。
与物质旋光能力,溶剂性质,样品管长度,光源的波长,溶液温度等有关。可见,旋光度与物质的浓度有关,且溶液的旋光度为各组分旋光度之和。
作为反应物的蔗糖是右旋性物质,其比旋光度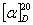 =66.6;生成物中葡萄糖也是右旋性物质,其比旋光度
=66.6;生成物中葡萄糖也是右旋性物质,其比旋光度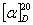 =52.5,但果糖是左旋性物质,其比旋光度
=52.5,但果糖是左旋性物质,其比旋光度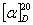 =-91.9。由于生成物中果糖的左旋性比葡萄糖右旋性大,所以生成物呈左旋性质。因此随着反应的进行,体系的右旋角不断减小,反应至某一瞬间,体系的旋光度可恰好等于零,而后就变成左旋,直至蔗糖完全转化,这时左旋角达到最大值α∞。
=-91.9。由于生成物中果糖的左旋性比葡萄糖右旋性大,所以生成物呈左旋性质。因此随着反应的进行,体系的右旋角不断减小,反应至某一瞬间,体系的旋光度可恰好等于零,而后就变成左旋,直至蔗糖完全转化,这时左旋角达到最大值α∞。
反应过程浓度变化转变为旋光度变化:
C12H22O11 + H2O C6H12O6 + C6H12O6
C6H12O6 + C6H12O6
t=0 C0 0 0
t=t Ct C0-Ct C0-Ct
t=∞ 0 C0 C0
当t=0时,溶液中只有蔗糖,溶液的旋光度值为:
α0=K蔗糖C0 (1)
当t=∞时,蔗糖完全水解,溶液中只有葡萄糖和果糖。旋光度为:
α∞=(K葡+K果)C0 (2)
当t=t时,溶液中有蔗糖、果糖和葡萄糖,此时旋光度为:
αt= K蔗糖Ct+(K葡+K果)(C0-Ct) (3)
联立(1)、(2)、(3)式可得:
C0=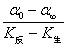 (4)
(4)
Ct=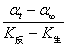 (5)
(5)
将(4)、(5)两式代入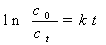 即得:
即得:

即ln(αt-α∞)=-kt+ln(α0-α∞)
我们以ln(αt-α∞)对t作图可得一直线,从直线的斜率可求得反应速率常数k。
可通过作图求的α0 。
三、仪器与试剂
旋光仪(1台);50ml容量瓶(1个);5mL移液管(1支);25ml移液管(1支);锥形瓶(3个);恒温水水浴(1台);秒表 (1个);蔗糖;分析台秤(1台);蔗糖;HCL溶液(2mol/L)。
四、实验步骤
1.溶液配制:
称取10克蔗糖放在烧杯中,加蒸馏水溶解,移至50ml容量瓶,加水稀释至刻度。
用25ml移液管移取蔗糖溶液于2个锥形瓶,准确加入5ml 2mol/L的HCl溶液,按下秒表开始计时(注意:秒表一经启动,勿停直至实验完毕)。将其中一份放入恒温水浴中加热,另一份用另一个锥形瓶相互倾倒2~3次,使溶液混合均匀。
2. ɑt测定:
迅速用反应混合液将旋光管管洗涤1次后,将反应混合液装满旋光管,擦净后放入旋光仪,测定规定时间的旋光度。反应前期可2min测一次,反应速度变慢后可5 ~10min测一次,测至60min即可。
3. α∞的测量:
将放入恒温水浴中加热的溶液使反应充分后拿出,冷却至室温后测定体系的旋光度。
五、实验数据记录和处理
1. 将实验数据记录于下表。
室温: 27.1℃ 大气压: 100.816kPa
反应温度: 27.1℃ CHCl = 2mol/L
α∞ = -7.67
表1 蔗糖反应液所测时间与旋光度原始数据

2.根据上表数据,算出相应的ln(αt-α∞)的数值计入表格,并以In(αt-α∞)对t作图。
表2 In(αt-α∞)与t数据
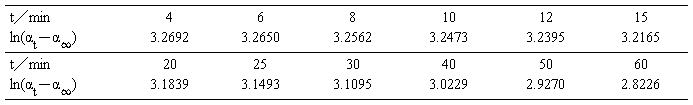
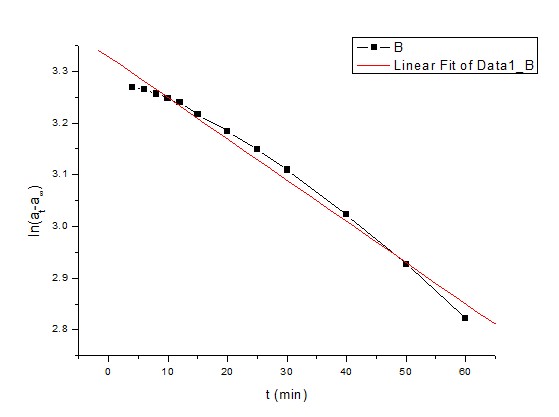
Linear Regression for Data1_B:
Y = A + B * X
Parameter Value Error
----------------------------------
A 3.32801 0.00854
B -0.00795 2.92634E-4
----------------------------------
R SD N P
----------------------------------
-0.9933 0.01774 12 <0.0001
----------------------------------
ln(αt-α∞)=-kt+ln(α0-α∞)
即 ln(αt-α∞)=-0.00795t+3.32801
3.由直线斜率求出反应速率常数k(直线斜率的相反数即为速率常数k),并计算反应的半衰期t1/2。
即: -k=-0.00795
则速率常数: k=7.95*10-3 min-1
半衰期: t1/2=ln2/k=5.53 min
六、思考题
1. 蔗糖水解反应速率常数和哪些因素有关?
与反应温度和反应活化能有关
2. 反应开始时,为什么将盐酸倒入蔗糖溶液,而不是相反?
因为盐酸与蔗糖溶液反应是个放热的过程,盐酸的比重比蔗糖溶液的比重大,如果将蔗糖溶液倒入盐酸中会由于热量不能及时散发而发生溶液飞溅。
3. 记录反应开始的时间迟点或早点,是否影响值的测定?
影响值的测定
九、文献参考值
[H=]=1.8 mol/L
k298=11.16*10-3 min-1
K308=46.76*10-3 min-1
K398=148.8*10-3 min-1
