
实验四 铵盐中氮含量的测定(甲醛法)
重点:容量瓶的使用;NaOH标液的配制和标定;甲醛法测定氨态氮的原理和操作方法;试验结果的记录和铵盐的含氮量计算。 难点:弱酸强化的基本原理;酸碱指示剂的选择原理和指示剂突变的判断。
一、 实验目的
1、掌握甲醛法测定铵盐中氮含量的基本原理
2、复习滴定及称量操作
二、实验原理
铵盐NH4Cl和(NH4)2SO4是常用的氮肥,系强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),故无法用NaOH标准溶液直接滴定。生产和实验室中广泛采用甲醛法测定铵盐中的含氮量。甲醛法是基于如下反应:
生成的H+和(CH2)6N4H+(Ka=7.1×10-6)可用NaOH标准溶液滴定,计量点时产物为(CH2)6N4,其水溶液显微碱性,可选用酚酞作指示剂。
三、仪器和试剂
邻苯二甲酸氢钾(KHP)分析纯;酚酞2g·L-1乙醇溶液;甲基橙1 g·L-1水溶液;(NH4)2SO4;0.1mol·L-1NaOH标准溶液(同实验3);40%甲醛;甲基红2g·L-1乙醇溶液。
四、实验内容
1.配制0.1mol.L-1NaOH500mL(称取2gNaOH配制成500mL溶液)。
2.将称量瓶洗涤并烘干,称取0.4~0.5g邻苯二甲酸氢钾三份分别放于锥形瓶中。
3.将称量得到的邻苯二甲酸氢钾用20-30mL水温热溶解,冷却后,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至溶液呈微红色,半分钟内不褪色,即为终点。
4.称取0.10~0.20g(NH4)2SO4 三份于锥形瓶中。
5.将称量得到的(NH4)2SO4用20-30mL水溶解后,加入5mL中性甲醛溶液,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至淡红色,半分钟内不变色,即为终点。
五、数据记录及处理
1.数据记录表格
2. 含氮量的计算
含氮量N%=CNaOH×VNaOH×M(N)×100%/m
六、注意事项
1.如果铵盐中含有游离酸,应事先中和除去,先加甲基红指示剂,用NaOH溶液滴定至溶液呈橙色,然后再加入甲醛溶液进行测定。
2.甲醛中常含有微量甲酸,应预先以酚酞为指示剂,用NaOH溶液中和至溶液呈淡红色。
3.滴定中途,要将锥形瓶壁的溶液用少量蒸馏水冲洗下来,否则将增大误差。
七、实验讨论
1、铵盐中氮的测定为何不采用NaOH直接滴定法?
答:铵盐NH4Cl和(NH4)2SO4是常用的氮肥,系强酸弱碱盐,由于NH4+的酸性太弱(Ka=5.6×10-10),用NaOH标准溶液直接滴定,在滴定曲线上已无明显突跃,此时反应的完全程度很低,难以用指示剂来确定滴定终点。故不采用NaOH标准溶液直接滴定。
2、为什么中和甲醛试剂中的甲酸以酚酞作指示剂;而中和铵盐试样中的游离酸则以甲基红作指示剂?
答:选择指示剂是根据滴定终点溶液的酸碱性和指示剂的变色范围来决定的。酚酞指示剂的变色范围是8.0-9.6,甲基红指示剂的变色范围是4.4-6.2,中和铵盐试样中的游离酸时其滴定终点溶液显酸性,中和甲醛试剂中的甲酸时其滴定终点溶液显弱碱性,所以,中和甲醛试剂中的甲酸以酚酞作指示剂;而中和铵盐试样中的游离酸则以甲基红作指示剂。
3. NH4HCO3中含氮量的测定,能否用甲醛法?
答:不能用甲醛法测定。
NH4HCO3是弱酸弱碱盐,在水中的水解常数K=KW/(Ka×Kb)=1.31×10,因为Ka<Kb,溶液显碱性,可以加入1-2滴甲基橙,用0.1mol.L-1HCl溶液滴定溶液由黄色至橙色,加入5ml中性甲醛溶液,加入1-2滴酚酞,用0.1mol.L-1NaOH滴定至淡红色,半分钟内不变色。
-3
第二篇:甲醛法测定铵盐影响终点的探讨
甲醛法测定硝酸铵影响终点的探讨
前言:
我公司是建于二十世纪六十年代末的中型氮肥企业,硝酸铵是柳化的支柱产品。我公司在硝酸铵产品质量检测中,采用GB/T3600—2000《肥料中氨态氮含量的测定—甲醛法》测定硝酸铵含量。甲醛法最初于1907年提出,1933年应用于肥料分析,我国从50年代起,先后将其应用于硫酸铵、硝酸铵、氯化铵等产品的检验上,规定为标准分析方法,该法具有操作简便,测定快捷,结果准确等优点,但该法也存在着滴定终点不稳定,测定结果容易偏低等问题,主要是由于所用试剂甲醛中含有甲醇的影响,使用蒸馏分离法将甲醛中甲醇脱除以后,问题就算解决了,本文通过实验对这些问题进行讨论证和探讨,使该方法得到更好的应用。
一、甲醛法测定原理
甲醛与铵盐作用生成六次甲醛四胺和相当于铵盐含量的酸,以酚酞作指示剂,用氢氧化钠标准溶液滴定,根据消耗的氢氧化钠标准溶液的体积可计算出铵盐含量。甲醛与铵盐的反应方程式如下:
6HCHO+4NH4+=(CH4)6N4+4H++6H2O
二、仪器与试剂
酸度计 25%甲醛溶液(用多聚甲醛配制),36%~38%甲醛(含甲醛8%~12%),1%酚酞指示剂,氢氧化钠标准溶液C(NaOH)=0.5mol/L、硫酸标准溶液 C(1/2H2SO4)=0.1mol/L、甲醛溶液 250g/L、甲基红指示剂 1g/L、酚酞指示剂10g/L、C(HCl)=0.5mol/L标准溶液,甲醇(含量99.5%),六次甲基四胺(固体),以上均为分析纯试剂。
PH8.5的颜色参比溶液在250mL锥形瓶中加入15.15mL0.1mol/L氢氧化钠标准溶液、37.50mL 0.2mol/L硼酸-氯化钾溶液(称取6.138g硼酸和7.455g硫化钾溶液,用少量水溶解后,移入500mL容量瓶中,加水定容),再加入1滴甲基红指示剂和3滴酚酞指试剂,加水稀释至150mL。
三、测试步骤
按GB/T3600-2000《肥料中氨态氮含量的测定—甲醛法》进行。称取1g试样(精确至0.001g),置于250mL容量瓶中,加入100~120mL水溶解,再加1滴甲基红指示剂,用0.1mol/L硫酸溶液或0.5mol/L氢氧化钠溶液调节至溶液成橙色。加入15mL甲醛溶液,再加入3滴酚酞指示剂,混匀,放置5min,用0.5mol/L氢氧化钠标准试剂溶液滴定至PH8.5的颜色参比溶液所呈现的颜色,经1min不消失为终点。
硝酸铵产品中硝酸铵含量按下式计算:

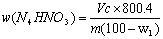 式中w(NH4NO3) 试样中硝酸铵的质量分数(以干基计),%;
式中w(NH4NO3) 试样中硝酸铵的质量分数(以干基计),%;
V 滴定用去氢氧化钠标准溶液的体积,ml;
c 滴定用氢氧化钠标准溶液的浓度,mol/L;
m 试样质量,g;
0.08004 与c(NaOH)=1.000mol/L的1.00ml氢氧化钠溶液相当的硝酸铵的质量,g;
w1 样品中游离水的质量分数,%。
四、试验结果与讨论
1、甲醛中甲醇含量对测定结果的影响
按照GB/T3600规定的方法,用甲醛法测定硝酸铵含量,测定不同甲醇含量的甲醛溶液对分析结果的影响,制表1,

由表1可以看出,甲醇含量越高测定结果越低,当甲醇含量由微量增至10%,测定硝酸铵含量由99.8%降至99.1%,绝对误差0.7%,当甲醇含含量小于1%时,对测定结果影响甚小<0.1%,可以认为基本没有影响。
2、甲醛与铵盐反应过程的酸度变化:
主要试验含与不含甲醇与硝酸铵试样反应过程中酸度(PH)变化。因为一般试剂甲醛溶液中含量有8%~12%甲醇作阻聚剂以防止甲醛聚合,这种甲醛聚合,这种甲醛溶液中可能含有缩醛。
试验方法,准确称取数份硝酸铵试样(每份约1.5g称准至0.0002g)于烧杯中,分别加入约100ml水溶解,再分别加入预先用碱中和过的不同组份甲醛溶液的15ml混合均匀后立即用酸度计测量溶液的PH值,以每隔10分钟测量一次,同时以不含试样但含有试剂组份以及反应产物六次四基胺和盐酸(实际反应产物为硝酸)的空白溶液作对照(含量与试样测定液相近)。
甲醛与硝酸铵反应要经历较长的时间,约1小时才能趋于平稳,即达到化学平衡,温度高反应加快,但仍不能进行完全,证明此为可逆反应,另一方面,向甲醛中加入一定量甲醇,这种甲醇的甲醛溶液与铵盐反应后,溶液的酸度有较大的变化,PH值升高了(4.8~3.4),这也说明反应进行不完全这是另外一类副反应的影响,这一类副反应是由甲醇引起的。
3、滴定终点的稳定性试验:
将配制甲醛溶液中含不同组分甲醇,分别与一定量硝酸铵试样反应后,用0.5mol/L氢氧化钠滴定,用酚酞指示剂和酸度指示剂同时指示终点(PH≈8.5),到达终点时,观察溶液颜色和PH值的变化,并加以测量,然后制表2

由表2可以看出,加入不含或含微量甲醇的甲醛试剂与硝酸铵试样反应后,滴定终点稳定,30分钟内溶液颜色和PH值变化很少<0.05,而加入含10%甲醇的甲醛溶液,在0.5mol/L氢氧化钠标准溶液滴定接近滴定终点,会出现几个不稳定的假终点,经多次反复滴定才达到最后一个稳定的真终点,无论是从观察溶液颜色变化还是酸度变化均是这样说明甲醇对滴定终点的影响是很大的,甲醇含量越高,稳定性越差。
4、终点前滴定对滴定终点的影响
使用不含甲醇的甲醛溶液滴定终点突越PH值变化,溶液颜色变化明显清晰,到达滴定终点后PH值和颜色均很稳定。而使用含甲醇的甲醛溶液,滴定时则出现几个假终点,稍经放置PH降低,颜色变浅,甚至褪去,须经3~4次反复滴定(每次约加1~2滴)才能到达真正终点,即滴定到溶液PH=8.5,溶液为浅红色,放置5分钟PH值下降,颜色变浅,再滴定PH=8.5,放置5分钟后又下降,直至最后才能达到稳定。
5、其他组分的影响:
① 分别用试剂甲醛、甲醇作空白,以酚酞为指示剂,用氢氧化钠标准溶液中和至浅红色,观察和测量颜色及PH值变化,结果在10分钟内均比较稳定。
② 在滴定至浅红色含试样和甲醛的溶液中分别加入一定量中和过的甲醇、六次甲基四胺,结果终点任然比较稳定,变化很小。六次甲基四胺如不中和则溶液PH值略有升高。
③ 在不含试样但含水、甲醛、甲醇和六次甲基四胺及25ml0.5mol/L盐酸标准溶液中,以酚酞为指示剂用0.5mol/L氢氧化钠标准溶液滴定,同时用酸度计确定终点,结果证明滴定终点很稳定,而且所用酸碱标准溶液的毫升数相等。
以上实验充分证明,当溶液中没有铵盐时,各有关组分包括六次甲基胺在内,对滴定终点并没有什么影响。
五,影响机理探讨
1、反应机理
一般认为,甲醛与铵盐反应,生成等当量的酸,包括氢离子和质子化的六次甲基四胺,如下式所示:
6HCHO+4NH4+=(CH4)6N4H++3H++6H2O (1)
生成的酸包括质子化的六次甲基四胺,可用碱标准溶液滴定,以酚酞作指示剂。由于六次甲基四胺是极弱的有机碱,它的存在使等当点时溶液呈微碱性。又由于它是可逆反应,在酸性溶液中不能定量地完成;但是,当NaOH标准溶液滴定时反应都能进行到底,这这和我们的实验结果完全相符。如以甲醛法测定硝酸铵为例,包括滴定在内的测定总反应方程式为:
4NH3NO3+6HCHO+4NaOH=(CH2)6N4+4NaNO3+6H2O (2)
2、甲醇影响机理
实验表明,当测定溶液中含有甲醇时,反应后溶液的PH值较不含甲醇的溶液偏高,即酸度降低;在用碱滴定时出现终点不稳定并导致滴定结果偏低。只是什么缘故呢?文献认为,在在酸的催化下,醛能与一分子醇加成,生成半缩醛,半缩醛不稳定,可与另一分子醇进一步缩合生成缩醛。在有机化学中,常利用缩醛的生成和水解来保护醛(羰)基。试验和分析表明,在含甲醇的甲醛溶液中含有一定量的缩醛和半缩醛。因此,我们根据醛醇缩合的反应式为;
HCHO+CH3OH=CH3OCH2OH (3)
CH3OH2OH+CH3OH=CH3OCH2OCH3+H2O (4)
(3)、(4)也是可逆反应,由于该反应的存在降低了测定溶液中甲醛的浓度和活性,使甲醛与铵盐的反应速度减慢,反应更不完全。在用NaOH标准溶液滴定时,因为生成的酸被中和,化学平衡被打破,(1)、(2)主反应向右进行,甲醛继续与铵盐作用;随着溶液中甲醛浓度降低,(3)、(4)副反应向左进行,即缩醛、半缩醛水解出更多的甲醛再与铵盐反应。当不间断地进行滴定时,(1)、(2)正向反应和(3)、(4)反向反应交替进行,直至达到新的化学平衡;接近滴定终点时,参与正向主反应和逆向副反应的物质浓度越来越低,反应速度变慢;同时因被滴定液逐步接近于微碱性,副反应趋于稳定,释放出来的甲醛更少,主反应难以加速,从而出现假终点并使测定结果偏低。这可以说是(3)(4)副反应对(1)、(2)主反应影响的结果。这样的判断和推理是否正确,希望得到化学分析界同行们的指教。
通过以上实验,分析可知,我们找到了使用甲醛法测定硝酸铵产品中硝酸铵含量时影响测定结果原因,并对分析方法进行了改进。
应注意几个问题:
①使用多聚甲醛配制成25%甲醛溶液。一定要控制甲醛含量。
②因甲醛溶液通常呈弱酸性,未经中和的甲醛溶液自己接与硝酸铵反应,也会消耗一部分氢氧化钠标准溶液,使测定结果偏高,所以甲醛溶液在使用前先用氢氧化钠滴定中和至微红色,经0.5~1分钟不退色为止。
③中和过的甲醛溶液与硝酸铵溶液混合后,静置5分钟后再用氢氧化钠标准溶液滴定至微红PH=8.5
参考文献
1 山添文雄等著、肥料分析方法详解(修订本),化学工业出版社,1988,56~57
2 胡哲生.尿素国家标准分析方法学习班讲义(第三讲),化工部化肥监测中心,1982
3 GB/T3600-2000
4 张志贤等编著.有机官能团定量分析、化学工业出版社,1990,215~216
5 徐寿昌编、有机化学,1988,248~24
