����е������IJⶨ
ʵ�����ڣ�
ʵ��Ŀ�ģ�
���������ü�ȩ���ⶨ����е���ԭ���ͷ�����
���������ζ������͵ζ��յ���жϡ�
һ������ԭ��
����dz����������ʣ���ǿ�������Σ��������ζ����ⶨ�京����������NH4+������̫����Ka��5.6×10-10����ֱ����NaOH����Һ�ζ������ѣ�������ʵ�����й㷺���ü�ȩ���ⶨ����еĺ�������
��ȩ���ǻ��ڼ�ȩ��һ����������ã������൱������(H+)�����μ�����Σ�Ka��7.1×10-6����Ӧ���£�
��NH4+ �� ��HCHO �� (CH2)6N4H+ �� ��H2O �� ��H+

�����ɵ�H +�����μ��İ���,���Է�̪Ϊָʾ��,��NaOH����Һ�ζ����ٰ���ʽ���㺬����
ʽ��MN����ԭ�ӵ�Ħ������(14.01 g/mol)��
������Ҫ�Լ�
����0.1 mol/L NaOH��Һ ����0.2����̪��Һ
����0.2������ָʾ�� ������ȩ��Һ������
�����ⶨ���裺
1��NaOH��ҺŨ�ȵı궨��
ϴ����ʽ�ζ��ܣ���鲻©ˮ���������Ƶ�NaOH��Һ��ϴ2��3�Σ�ÿ������5��10mL��Ȼ��Һװ��ζ���������0���̶����ϣ��ų��ܼ�����ݣ�����Һ����0.00�̶Ȼ�������´�������1min��ȷ��ȡ�ζ�����Һ��λ�ã�����¼�ڱ��汾�ϡ���
�ò����ȷ��ȡ0.4��0.6g�Ѻ�ɵ��ڱ�������������ݣ��ֱ���������ѱ�ŵ�250mL��ƿ�У���20��30mLˮ�ܽ�(�����ܿ��Լ��ȣ���ȴ��)������1��2�η�ָ̪ʾ������0.1mol·L-1NaOH��Һ�ζ�������ɫ������Ӳ���ɫ����Ϊ�յ㡣����NaOH����Һ��Ũ�ȡ�
2����ȩ��Һ�Ĵ�������ȩ�г��������������ɼ�ȩ�ܿ����������£�Ӧ��ȥ������������������������£�ȡԭװ��ȩ(��)(40��)���ϲ���Һ���ձ���,��ˮϡ��һ��,���룱������0.2����ָ̪ʾ��,��0.1 mol/LNaOH ��Һ�к�����ȩ��Һ�ʵ���ɫ��
3�������к������IJⶨ�� ȷ��ȡ0.4��0.5 g��NH4Cl��1.6��1.8 g���ҵ�(NH4)2SO4���ձ��У�����������ˮ�ܽ⣬Ȼ����������250 ml ����ƿ�У����������ˮϡ�����̶ȣ�ҡ�ȡ� ����Һ����ȡ��Һ25 ml����ƿ�У��ӣ������μ���ָʾ������Һ�ʺ�ɫ����0.1 mol/L NaOH��Һ�к�����ɫתΪ���ɫ��Ȼ�����8 ml���к͵ģ�������ȩ��Һ���ټ��룱�����η�ָ̪ʾ��ҡ��,����һ���Ӻ�,��0.1 mol/L NaOH ����Һ�ζ�����Һ����ɫ��������Ӳ���,��Ϊ�յ㡣(2)��¼������ƽ����2��3�Ρ�����NaOH ����Һ��Ũ�Ⱥ͵ζ����ĵ���������������е��ĺ�����
�ġ�ʵ�鱨��
������¼

NaOH����Һ�ζ�(NH4)2SO4
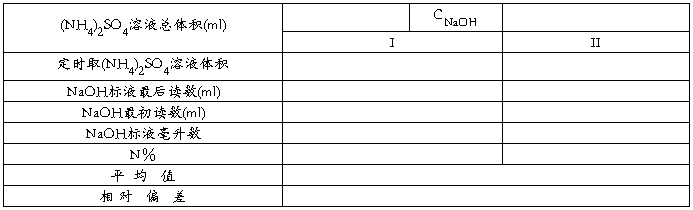
����������ȩ����ɫ�ۺ�״̬���ڣ���Ϊ��ۼ�ȩ����ȩ��Һ�к���������ۼ��Ӱ��ζ���
��������������Һ���Ѿ��м��죬���÷�̪Ϊָʾ�����������ֱ�ɫ��ͬ��ָʾ��,��NaOH�ζ�ʱ,��Һ��ɫ���ɺ�ת��Ϊdz��ɫ��pHԼΪ6.2������ת��Ϊ����ɫ��pHԼΪ8.2�����յ�Ϊ����Ļ�ɫ�ͷ�̪��ɫ�Ļ��ɫ��
һ��ʵ��ԭ��

����ʵ�鲽��
1����ȡ(NH4)2SO4����0.13-0.16g����
2��ɨ��������
a. ��ȩ�к��е�������Է�̪Ϊָʾ������0.10mol.L-1NaOH�к�����Һ�ʵ���ɫ���ɡ�
b. (NH4)2SO4�����к���HSO4-.H2SO4������Ӧɨ����
����������ƿ�м���2�μ���ָʾ��������Һ�ʺ�ɫ����ɫ����0.10mol.L-1NaOH��Һ�к������ɫ��
3��ת����
����5mL���Լ�ȩ��Һ��2�η�̪��ҡ�ȣ�����1min����ΪNH4+��ȫת����(CH2)6N4H+��
4���ζ�
��NaOH����Һ�ζ���ָʾ���ı�ɫΪ��
(NH4)2SO4��N����������ֵΪ21.21%
����ʵ��ע������
1 ʵ���г�ȡ(NH4)2SO4��������Ϊ0.13-0.16g�������ȷ���ģ���
2�������ļ��㹫ʽΪ ��������Ƶ��õ��ģ�
��������Ƶ��õ��ģ�
�ġ�˼����
1.����е��IJⶨΪ�β�����NaOHֱ�ӵζ�����
����NH4+��Ka=5.6×10-10������̫������Cka<10-8�����Բ�����NaOHֱ�ӵζ���
2.Ϊʲô�кͼ�ȩ�Լ��еļ����Է�̪��ָʾ�������к���������е����������Լ�����ָʾ����
�𣺼�ȩ�Լ��еļ����Է�̪Ϊָʾ����NaOH����ȫ�������кͣ����Լ���Ϊָʾ������NaOH�ζ���ָʾ����Ϊ��ɫʱ����Һ��pHֵΪ4.4�����������ȫ�к͡���������е����������Է�̪Ϊָʾ������NaOH��Һ�ζ����ۺ�ɫʱ����ξ����ٲ��ֱ��ζ���ʹ�ⶨ���ƫ�ߡ�
3. NH4HCO3�к������IJⶨ���ܷ��ü�ȩ����
��NH4HCO3�к������IJⶨ�����ü�ȩ��������NaOH��Һ�ζ�ʱ��HCO3-�е�H+ͬʱ���ζ������Բ����ü�ȩ���ⶨ��
�ڶ�ƪ���Ȼ�淋��Ʊ����������IJⶨ
�Ȼ�淋��Ʊ����������IJⶨ
һ��ʵ��ԭ��
1���Ȼ�淋��Ʊ���
��ʵ�����Ȼ�����������������Ʊ��Ȼ�泥�
2NaCl +��NH4��2SO4 ==== Na2SO4 + 2NH4Cl
�������ǵ��ܽ�ȼ������¶�Ӱ�����ԭ������ȡ���ȡ���������ȴ�ȴ�ʩ��ʹ�ܽ���ᾧת�����Ӷ��ﵽ���롣
��Ӧ�漰�����ڲ�ͬ�¶��µ��ܽ��ֵ

�ɱ���֪���Ȼ�李��Ȼ��ơ��������ˮ�е��ܽ�Ⱦ����¶ȵ����߶����ӡ��������Ȼ����ܽ�����¶ȵ�Ӱ�첻������淋��ܽ�������ڵ��»��Ǹ��¶������ġ������Ƶ��ܽ����һת�۵㡣ʮˮ�����Ƶ��ܽ��Ҳ�����¶ȵ����߶����ӣ�����һ���¶�ʱ��ˮ���Na2SO4��Na2SO4���ܽ�����¶ȵ����߶���С�����ԣ�ֻҪ���Ȼ��ơ����������ˮ������������Na2SO4�ͻ�ᾧ���������ȹ��ˡ�Ȼ���ٽ���Һ��ȴ��NH4Cl�������¶ȵ��½�����������35�����ҳ��ˣ�����NH4Cl��Ʒ��
2���������IJⶨ
NH4Cl�dz��õĵ��ʣ�ϵǿ�������Σ�����NH4+������̫����Ka=5.6×10-10����������NaOH����Һֱ�ӵζ���������ʵ�����й㷺���ü�ȩ���ⶨ����еĺ���������ȩ���ǻ������·�Ӧ��
4NH4+ + 6HCHO ====��CH2��6N4H+ + 6H2O + 3H+
��CH2��6N4H+ + 4OH�� ==== H2O +��CH2��6N4
���ɵ�H+�ͣ�CH2��6N4H+��Ka=7.1×10-6������NaOH����Һ�ζ���������ʱ����Ϊ
��CH2��6N4����ˮ��Һ�����ԣ���ѡ�÷�̪��ָʾ����
����ʵ���������Լ�
1��������
��ƿ��3��250ml�������ӷ�����ƽ����ʽ�ζ��ܣ�25ml�����ձ���100ml������50mlһ��������ͨ©����������ˮԡ������ձã���Ͳ��50ml��5ml��һ������������������̨��������ƽ������©������ֽ���¶ȼƣ�100�棩���Թܣ��ԹܼУ�����PH��ֽ���ƾ��ơ�
2��ҩƷ��
��̪�����죻NaOH����Һ��1��1�ļ�ȩˮ��Һ��NaCl���壨����������
��NH4��2SO4���壨����������
����ʵ������
a���Ȼ�淋��Ʊ�
1.��ȡ11gNaCl������100mL�ձ��ڣ�����30��40mL����ˮ�����ȡ�����ʹ֮�ܽ⡣���в����������ͨ©�����˷��룬��Һ��������ʢ��
2.��NaCl��Һ�м���13g��NH4��2SO4��ˮԡ���ȡ����裬��ʹ���ܽ⡣��Ũ�������У��д���Na2SO4�ᾧ����������Һ���ٵ�35mL����ǰ���Ǻţ�����ʱ��ֹͣ���ȣ������ȳ��ˡ�
3.����ҺѸ�ٵ���100mL�ձ��У�������ȴ��NH4Cl��������������ȴ��35�����ң����ˡ�
4.����Һ��������ˮԡ�ϼ������������н϶�Na2SO4�������������ˡ������Һ��С�ձ��У�������ȴ��35�����ң����ˡ�����ظ����Ρ�
5.���������õ�NH4Cl����ϲ���һ����أ�������ʡ�
6.��Ʒ�ļ�����
ȡ1gNH4Cl��Ʒ������һ�����Թܵĵײ������ȡ�
NH4Cl���ʺ���=��G���պ�-G���Թܣ�g/1g´×100%
b���������IJⶨ
1.��NaOH������ȩ��Һ��ʹ��ȩ��Һ�����ԡ�
2.��ȡ0.08��0.10gNH4Cl��������ƿ�С�
3.�������õ���NH4Cl��20��30mLˮ�ܽ����5mL���Լ�ȩ��Һ������1��2�η�̪����0.1mol.L-1NaOH�ζ�������ɫ��������ڲ���ɫ����Ϊ�յ�
�ġ���Ʒ�����������������ⶨ
1.���ݼ�¼����

2NaCl +��NH4��2SO4 ==== Na2SO4 + 2NH4Cl
2×58.44 132.16 2×53.49
m��NaCl��m����NH4��2SO4�� 10
m��NaCl��=10×58.44/53.49=10.93��g��
m����NH4��2SO4��=10×132.16/��2×53.49��=12.35��g��
2.�������ⶨ���ݼ�¼
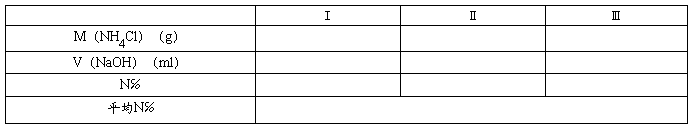
M��NH4Cl��=11×53.49/58.44=10.07��g��
����=M��ʵ��/M��NH4Cl��×100%
2.�������ļ��㣺
������N��=CNaOH×VNaOH×M��N��×100%/m
�塢ע������
1.��ˮ�ܽ���������϶�ʱ����Һ�����ˮ��������ȡ�
2.ˮ��30-40mL���ɣ�Ũ��ʱҪ��ǰ���üǺţ�Ũ�����ܹ��ȣ��Է�NaCl����NH4��2SO4���������ȳ���ʱҪԤ�����������Ũ�����루NH4��2SO4��NH4Cl��
3.�������к��������ᣬӦ�����кͳ�ȥ���ȼӼ���ָʾ������NaOH��Һ�ζ�����Һ�ʳ�ɫ��Ȼ���ټ����ȩ��Һ���вⶨ��
4.��ȩ�г����������ᣬӦԤ���Է�̪Ϊָʾ������NaOH��Һ�к�����Һ�ʵ���ɫ��
5.�ζ���;��Ҫ����ƿ�ڵ���Һ����������ˮ��ϴ����������������
���������
����ѧ��ѧ����ʵ�顷��ѧ�����磨�ڶ��棩
������������ѧʵ�顷��ѧ�����磨��һ�棩
������ѧʵ�黯ѧ����ҵ�����磨��һ�棩
��������ѧ������������ѧ�Ĵ���ѧ�ࣨ�����棩
GB 2946-92 �Ȼ��
HG/T 2843-1997 ���ʲ�Ʒ ��ѧ�������ñ��ζ���Һ������Һ���Լ���Һ��ָʾ����Һ
��ǿ��ɻ�������������
