实验3 食用白醋的总酸度、电离度和电离常数的测定
教学目的与要求:
1.学习食用白醋的总酸度、电离度和电离常数的的原理和方法;
2.学习酸度计的原理和方法;
3.熟练掌握移取,称量,配制一定浓度标准溶液等操作;
4.进一步熟练掌握滴定操作;
5.学会如何合理的设计实验并培养学生的动手操作能力及创新意识。
教学重点与难点:
重点:1.食用白醋的总酸度、电离度和电离常数的的原理和方法;
2.培养学生的动手操作能力及创新意识。
难点:1.酸度计的使用方法;
2.滴定操作的终点控制。
教学方法与手段:板书,学生操作,现场指导。
学时分配:3学时。
教学内容:
食用白醋是人们日常生活常用的调味品之一,白醋的质量安全与人们的日常生活息息相关。总酸度是测定食醋品质的主要指标,食用醋中的总酸度可以通过多种实验方法测定,如电位滴定法、酸碱滴定法、微型滴定法、连续分析技术定量测定等。综合各方面的因素,通常采用酸碱滴定法测定醋的总酸度,此方法可行性强,易操作,误差小,实验过程安全。
食用醋的主要成分是醋酸(HAc),此外还含有少量的其他弱酸,如乳酸等。醋的总酸度指所有的酸性成分的总量,包括已离解的酸浓度和未离解的酸浓度。采用酸碱滴定法,以邻苯二甲酸氢钾为基准物质,此物质易得,在空气中不吸水,容易保存,是一种较好的基准物质,反应产物为二元弱碱,水溶液呈碱性,以酚酞作为指示剂,30S 不褪色,为终点。再以标定的碱滴定醋,反应式如下:NaOH+HAc=NaAc+H2O ,产物为弱碱,以酚酞作指示剂,30S 不褪色,即为终点。由消耗的碱量计算总酸度,用g/100mL表示。
问题1:实验中需要的教学用品?
1、仪器:电子称、酸度计、容量瓶、移液管、滴定管等。
2、试剂:邻苯二甲酸氢钾(KHP)、食用白醋、氢氧化钠、酚酞。
问题2:如何测定食醋总酸含量?
醋酸为一弱酸,其离解常数Ka=1.76×10-5,利用滴定分析法(容量分析),用已知浓度的氢氧化钠溶液滴定待测食醋样品溶液,反应如下:
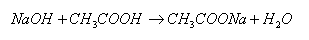
即待测溶液中酸的总量跟所消耗的NaOH的物质的量相等
m(CH3COOH)/M(CH3COOH)=c(NaOH) × v(NaOH)
然后换算成100mL食醋中含醋酸的质量
问题3:如何选择指示剂?
(1)用量:2~3滴。因指示剂本身也是弱酸弱碱,若用量过多,会使中和滴定中需要的酸或碱的量会增多或减少。
(2)常用指示剂:酚酞、甲基橙(一般不用石蕊)
(3)选择原则:
指示剂恰好变色时溶液的pH值与恰好完全反应后,所得溶液的pH值要尽可能接近。
强酸+强碱——酚酞或甲基橙
强碱+弱酸 ——酚酞
强酸+弱碱 ——甲基橙
问题4:滴定终点颜色如何变化?

中和滴定曲线
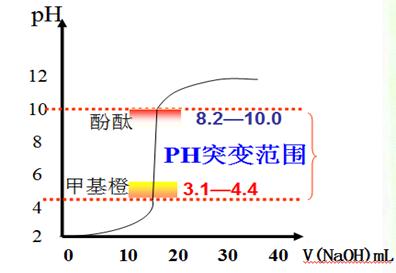
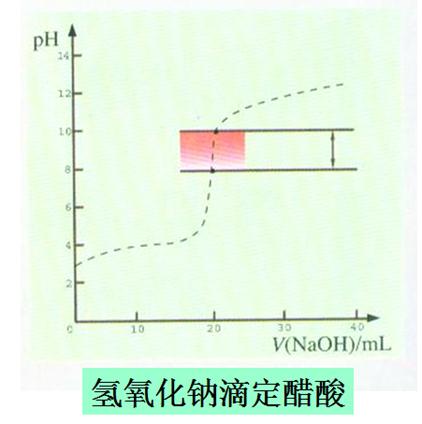
滴定突跃:7.74—9.70
指示剂选择:酚酞
能力拓展:当用盐酸滴定氨水时,应选择什么作为指示剂?

 刚好到滴定终点时酚酞显示的颜色 多滴了一滴NaOH时酚酞显示的颜色
刚好到滴定终点时酚酞显示的颜色 多滴了一滴NaOH时酚酞显示的颜色
问题5:如何测定白醋的电离度和电离常数?
醋酸是弱电解质,在水溶液中存在着下列电离平衡:
HAc === H+ +Ac-
其电离常数表达式为:
Ki = [H+ ][Ac-] / [HAc] (1)
设HAc的起始浓度为c,如果忽略水电离所提供H+离子的量,则达到平衡时溶液中[H+ ]≈[Ac-],式(1)可改写为:
Ki = [H+]2 /( c- [H+] ) (2)
如果我们配制一系列的已知浓度的醋酸溶液,并用酸度计测定其pH值,再换算成[H+](实际上酸度计所测的pH值是反映了溶液中H+离子的有效浓度,即H+离子的活度值)。利用(2)式,可求得一系列Ki值,取其平均值,即为该测定温度下醋酸的电离常数。
电离度a定义为: a = [H+] / c (3)
能力拓展:弱酸的酸度、电离度和电离常数之间有什么关系?
四、操作步骤
1、KHP(0.1000M)的配制:
称取2.0422g的KHP,在小烧杯中加水溶解,转入100mL容量瓶中,加水至标线,摇匀,备用。
2、NaOH(0.1M)溶液的配制:
称取1.2g氢氧化钠于在烧杯中,加300mL水溶解。
3、NaOH溶液的标定
移取25.00mLKHP标准溶液于的250mL锥形瓶中,各加入20mL水,滴加1~2滴0.2%酚酞指示剂。用待标定的NaOH溶液分别滴定至无色变为微红色,并保持半分钟内不褪色即为终点。记录滴定前后滴定管中NaOH溶液的体积。
4、食用醋的稀释:
用10.00 mL移液管吸取食用醋试液一份置于100 mL容量瓶中,用水稀释至刻度,摇匀。
5、食用醋总酸度的测定
用移液管吸取25.00mL稀释后的试液置于250mL锥形瓶中,加入0.2%酚酞指示剂1~2滴,用NaOH标准溶液滴定,直到加入半滴NaOH标准溶液使溶液呈现微红色,并保持半分钟内不褪色即为终点。重复操作,测定结果的相对平均偏差应小于0.2 mL。根据测定结果计算试样中酸的总含量,以g·L-1表示。
6、配制不同浓度的白醋溶液
用移液管分别取25 mL、10 mL和5mL已标定过的白醋溶液,放入三个洗净的100cm3容量瓶中,用蒸馏水稀释至刻度,摇匀。
7、测定不同浓度白醋溶液的pH值
将上面得到的四种精确浓度的白醋溶液,由稀到浓倒入烧杯中,分别用pH计测定它们的pH值,记录室温。
五、交流与讨论
1、在滴定时为什么要将市售食醋稀释10倍;如何精确的将市售食醋稀释十倍?
为了使量取食醋的体积与氢氧化钠溶液的消耗量相当,提高实验的精确度,同时也有助于减少食醋的颜色对滴定终点的颜色的干扰。用移液管取10mL稀释到100mL容量瓶中。
2、为什么要预先用少量待装溶液润洗滴定管3次?锥形瓶是否用稀食醋溶液润洗?
为了避免装入后的溶液被稀释。
3、如果要测定食醋的总酸含量,但无酸式滴定管,可用什么玻璃仪器来代替?该仪器是否要用待装溶液润洗3次?
移液管,要润洗3次,避免吸入的溶液被稀释。
4、如果滴定的终点没有控制好,即氢氧化钠滴加过量,溶液显红色,你有没有补救的办法?
可用酸式滴定管往锥形瓶里加醋酸,至溶液显粉红色,重新记录醋酸溶液的终读数,最后进行计算和数字处理时,全部考虑在内进行计算。
5、本实验产生的偏差的原因有哪些?你认为采取什么措施可以减少偏差?
(1)从氢氧化钠溶液方面来说:
a.氢氧化钠溶液存放时间过长,产生少量碳酸钠,应现用现配制。
b.配制氢氧化钠溶液时蒸馏水未煮沸,含有CO2;应煮沸并迅速冷却。
c.氢氧化钠溶液配制完成后未标定其准确浓度;应进行标定。
d.氢氧化钠溶液配制过程中操作不当,造成浓度不准确;应规范配制。
e.滴定过程中仰视、俯视读数;应使视线、凹液面最低处、刻度线相切。
(2)从食醋方面来说:
移取食醋溶液体积不准确;应正确使用酸式滴定管或移液管量取其体积
(3)从滴定终点判定不准确:
加入最后一滴NaOH溶液,溶液由无色变为粉红色,且半分钟之内不再褪去,方可为滴定终点,不能过早或过晚估计
六、注意事项
1、酸和碱不同的溶液应分为两台仪器测量。
2、电极在测量前要彻底冲洗干净,以免留有残液.
3、小心轻放,玻璃球易碎。
4、转动各旋钮时,不要用力太大。
5、测量完毕,洗净电极头部,罩好仪器。
6、食醋的选择:白醋:效果较好;香醋:稀释10倍;陈醋: 颜色很深
7、消除CO2对实验的影响
配制NaOH溶液和稀释食醋的蒸馏水在实验前应加热煮沸2~3分钟,以尽可能除去溶解的CO2,并快速冷却至室温。
七、几个关健实验操作
1、移液管尖嘴残留液体的处理
2、滴定前后碱式滴定管中不能有气泡
3、滴定管使用前要用待盛放的溶液润洗锥形瓶不能用待测液润洗
4、滴定终点的判断
5、读数时是否平视
八、课外思考题
1、若所用的醋酸的浓度极稀,醋酸的电离度大于5%时,是否还可以用简化公式计算其电离平衡常数?
2、实验中,醋酸的浓度、醋酸根的浓度是怎样测定的?
3、同温下,不同浓度的醋酸溶液的电离度是否相同?电离平衡常数是否相同?
4、浓度不变,温度变化时,醋酸的电离度和电离平衡常数有何变化?
5、既然电离平衡常数与浓度无关,为何还要测准醋酸的浓度?
6、本实验的关键步骤是什么?
7、已标定的NaOH标准溶液在保存时吸收了空气中的CO2,以它测定溶液HCl的浓度,若用酚酞为指示剂,对测定结果产生何种影响?
九、课外学习网站:
1、http://wenku.baidu.com/view/2be06d5bbe23482fb4da4c3f.html
2、http://wenku.baidu.com/view/6d07ab678e9951e79b892780.html
3、http://wenku.baidu.com/view/7fbcb91a59eef8c75fbfb3e3.html
4、http://wenku.baidu.com/view/d1969d62ddccda38376bafbd.html
5、http://wenku.baidu.com/view/1d7e78d85022aaea998f0fd7.html
6、http://wenku.baidu.com/view/23df5534eefdc8d376ee32fe.html
7、http://wenku.baidu.com/view/9e7cbb9e51e79b8968022614.html
知识拓展:1、邻苯二甲酸氢钾(KHP)简介:
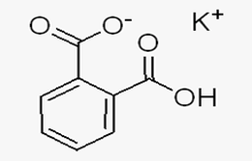 无色单斜结晶或白色结晶性粉末。分子式:KHC8H4O4,缩写为KHP。分子量为204.22。在空气中稳定,能溶于水,微溶于醇。微溶于乙醇。溶液呈酸性。25℃ 0.05mol/L水溶液的pH为4.005。
无色单斜结晶或白色结晶性粉末。分子式:KHC8H4O4,缩写为KHP。分子量为204.22。在空气中稳定,能溶于水,微溶于醇。微溶于乙醇。溶液呈酸性。25℃ 0.05mol/L水溶液的pH为4.005。
滴定分析中的基准物质,用于标定碱性物质,配制缓冲溶液。与氢氧化钠反应生成邻苯二甲酸钾钠。
2、食用白醋的酸度为什么要用总酸度表示?
食用醋的主要成分是醋酸(HAc),此外还含有少量的其他弱酸,如乳酸等。醋的总酸度指所有的酸性成分的总量,包括已离解的酸浓度和未离解的酸浓度。
食醋的总酸含量是指每100mL食醋中含酸(以醋酸计)的质量,也称食醋的酸度。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.
能力拓展:锥形瓶要不要用稀食醋溶液润洗?
能力拓展:如何配制并标定NaOH溶液的浓度?
问题1:NaOH标准溶液在配制时会变质吗?
NaOH+CO2 = NaCO3 +H2O
问题2:可采用哪些措施防止溶液变质?
用来配置溶液的蒸馏水加热煮沸除去二氧化碳,并迅速冷却。
问题3:如果配制NaOH溶液变质了怎么办?
配制NaOH饱和溶液,放置一段时间后,吸取上 层清液,稀释到约0.1mol/L,即可得NaOH标准溶液。
问题4:要精确得知氢氧化钠溶液的浓度可采取什么措施?
标定碱液的基准物质很多,如草酸(H2C2O4·H2O,M=126.07)、苯甲酸(C6H5COOH,M=122.12)、邻苯二甲酸氢钾(HOOCC6H4COOK,M=204.44)等.

用邻苯二甲酸氢钾作为基准物质,以酚酞作为指示剂,标定上述NaOH标准溶液。其中最常用的是邻苯二甲酸氢钾:
滴定终点时由于弱酸盐的水解,溶液呈碱性,采用酚酞为指示剂。
第二篇:实验8HAc电离度和电离常数的测定
实验8 HAc电离度和电离常数的测定
[实验目的]
1、 配制不同浓度的标准HAc溶液。
2、 掌握电导仪的使用方法,学习电导法测定电离度和电离常数的原理及在井穴板上进行溶液电导率测试的操作。
3、 加强对弱酸的电离度,电离常数和溶液的浓度与电导关系的理解。
[实验原理]
HAc在H2O中电离:HAc=H++Ac-,平衡时平衡常数Kc,浓度c和电离度〆间的关系为:Kc=c·〆2/(1-〆) (1)
求得〆,即可由已知的c求出Kc。电解质导电能力由电导(L)(电阻的倒数)来衡量,L=k·A/d (K为电导率,S·m-1)
摩尔电导(便于比较不同电解质溶液的导电能力):1mol电解质溶液置于单位距离(1m)的两个电导池的平行电极间,此时的电导称摩尔电导(∧m),∧m 与电导率k的关系为:
∧m =k·Vm=k/c

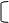 式中Vm为m3时,∧m为s·m2·mol-1,c为mol·m-3;若V为dm3,c为mol·L-1,则∧m为s·dm2·mol-1,此时公式为∧m=K×10-3/c。
式中Vm为m3时,∧m为s·m2·mol-1,c为mol·m-3;若V为dm3,c为mol·L-1,则∧m为s·dm2·mol-1,此时公式为∧m=K×10-3/c。
弱电解质无限稀释时,看作完全电离(〆→1),此时的∧m称极限摩尔电导∧∞,m,T一定,∧∞,m一定。
T一定时,〆=∧m/∧∞ (∧m为浓度c时的摩尔电导)
上式代入(1)式即得:Kc=c·∧m2/[∧∞(∧∞-∧m)],
另:内插法求所需∧∞值:
(∧∞,2-∧∞,1)/(∧∞,x-∧∞)=(T2-T1)/(Tx-T1),代入具体数据即可求出∧∞,x的值。
[结论]
〆随HAc浓度c↗而↘;c↘,k↘,∧∞↗;Kc与HAc的浓度c无关。
μs/cm=10-6s/10-2m=10-4s/m (s=Ω-1)
[注意事项]
1、 电极一定要保护好。
2、 井穴板必须整洁干燥,但不能在烘箱内干燥!
3、 所测溶液从稀到浓。
4、 井穴板中溶液不能注满,电极要完全浸入,每做完一次测定后要用蒸馏水清洗,再用待测液润洗。
实验9 电离平衡
[实验目的]
1、 巩固PH值的概念,掌握测试溶液PH值的基本方法。
2、 加强对盐类水解的认识。
3、 理解电离平衡,水解平衡和同离子效应的基本原理。
4、 学会配制缓冲溶液并试验其性质。
[实验原理]
1、 弱电解质(弱酸、弱碱等)在溶液中存在电离平衡:
HAc+H2O==H3+O+Ac- Ka NH3·H2O==NH4++OH- Kb
化学平衡移动规律同样适用于这种平衡体系。
2、 同离子效应:(弱酸、弱碱等)弱电解质溶液中加入含有相同离子的另一种电解质时,会使弱电解质的电离程度减小。

 H
2O+HAc == H
3
+O + Ac
-
H
2O+HAc == H
3
+O + Ac
-
 NaAc == Na+ + Ac-
NaAc == Na+ + Ac-
3、 盐类的水解:酸碱中和反应的逆过程,组成盐的离子与H2O中的H+或OH-结合生成弱电解质(酸、碱)的过程。盐的性质决定溶液水解后的酸、碱性。
H2O+CO32-==OH-+HCO-3 Kh=[HCO3-][OH-][H+]/([ H2O][CO-3][H+])=Kw/Ka2
4、 缓冲溶液:由浓度较大的弱酸(碱)及其共轭碱(酸)组成(实际为盐),在稀释或加少量酸、碱时,其PH值变化很小。缓冲能力与缓冲溶液的总浓度及配比有关(缓冲能力是有限的!)。
HAc+ H2O==H3O++Ac- K =[H+][ Ac-]/[ HAc]
[H+]=Ka·C酸/C盐==PH=Pka –lgC酸/C盐
对于一元弱碱:POH=PKb-lg C碱/C盐,其比值C酸/C盐或C碱/C盐从0.1→10时,PH(POH)变化只是从0.1→1。
5、 盐效应:加入强电解质而使弱电解质电离程度(或沉淀溶解度)增加的效应,(因离子强度↗,f↘)I=1/2∑(CiZi2);lgr=-0.509|z+·z-|·I/ (I +1);f=rc。
[注意事项]
1、 测溶液酸碱性(自制色阶亦如此)时,事先要将溶液搅匀,否则测出的只是局部酸碱性,出现错误结论。
2、 在缓冲溶液酸碱性测试时,要注意仪器的酸性范围与碱性范围,不能混测,这是事先标定时所决定了的。
3、 在NaAc中加1d酚酞,加热至沸时,可能会有浅红色沉淀生成,这是由于盐析现象所致。
4、 一定要注意保护电极!
