乙酸丁酯的制备
[实验目的]
1、熟悉乙酸正丁酯反应原理,掌握乙酸正丁酯的制备方法;
2、掌握回流和蒸馏操作;
3、掌握洗涤和萃取操作。
[实验内容]
一、实验原理:
以乙酸和正丁醇为原料,酸催化直接酯化制备乙酸正丁酯:

酯化反应一般要用酸进行催化,本实验采用硫酸。为使化学平衡有利于酯的生成,本实验采用乙酸过量的方法。
二、仪器和试剂:
100 mL圆底烧瓶、球形冷凝管、直形冷凝管、25 mL蒸馏烧瓶、分液漏斗、烧杯、锥形瓶、滴管、温度计、电子天平。
正丁醇、乙醇、浓硫酸、10%碳酸钠溶液,无水硫酸镁。
三、实验步骤
在干燥的100 ml圆底烧瓶中,装入正丁醇(9.2 ml,0.1 mol)和冰醋酸(12 ml,0.2 mol),并小心加入3~4滴浓硫酸。混合均匀,投入沸石,然后安装分水器及回流冷凝管,并在分水器中预先加水略低于支管口。在石棉网上加热回流,反应一段时间后把水逐渐分去,保持分水器中水层液面在原来的高度。约40 min后不再有水生成,表示反应完毕。停止加热,记录分出的水量。冷却后卸下回流冷凝管,把分水器中分出的酯层和圆底烧瓶中的反应液一起倒入分液漏斗中。用10 ml 10%的碳酸钠洗涤,分去水层。将酯层再用10ml水洗涤一次,分去水层。将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥。
将干燥后的乙酸正丁酯倒入干燥的25 ml蒸馏烧瓶中(注意不要把硫酸镁倒进去!)加入沸石,安装好蒸馏装置,在石棉网上加热蒸馏。收集124~126℃的馏分。前后馏分倒入指定的回收瓶中。
纯乙酸正丁酯是无色液体,沸点126.5℃,折射率1.3951。
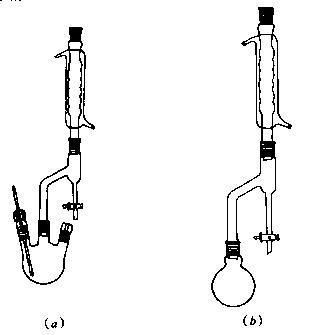
回流分水装置
四、注意事项
1、浓硫酸在反应中起催化作用,故只需少量。
2、本实验利用恒沸混合物除去酯化反应中生成的水。正丁醇、乙酸正丁酯和水形成以下几种恒沸混合物:含水的恒沸混合物冷凝为液体时,分为两层,上层为含少量水的酯和醇,下层主要是水。
[思考题]
1、乙酸正丁酯的合成实验是根据什么原理来提高产品产量的?
2、乙酸正丁酯的粗产品中,除产品乙酸正丁酯外,还有什么杂质?怎样将其除掉?
第二篇:乙酸正丁酯的制备
一、实验目的
掌握乙酸正丁酯的制备方法,重点学习分水器的使用及操作。
二、实验原理
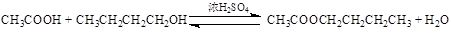 反应:
反应:
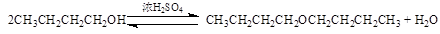 副反应:
副反应:
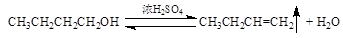
为了促使反应向右进行,通常采用增加酸或醇的浓度或连续地移去产物(酯和水)的方式来达到的。在实验过程中二者兼用。至于是用过量的醇还是用过量的酸,取决于原料来源的难易和操作上是否方便等诸因素。提高温度可以加快反应速度。
三、实验仪器与药品
电热套、蒸馏烧瓶、分水器、直形冷凝管、蒸馏头、温度计、锥形瓶、分液漏斗、滴管、pH试纸、小烧杯、洗瓶、铁圈。
四、物理常数
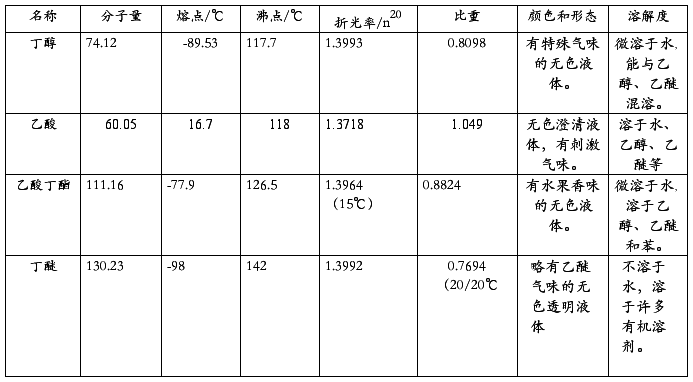
本实验理论产量:42.50g或48.2ml(乙酸过量)。
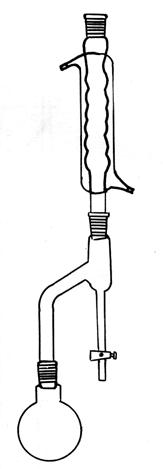 五、仪器装置图
五、仪器装置图
(回流反应装置图)
六、实验步骤
(1)加料。在干燥的圆底烧瓶中加入35mL正丁醇、22mL冰醋酸及10滴浓硫酸,摇匀后,加入几粒沸石,再安装好分水器(先从分水器上端小心加水至分水器支管处,然后再放去9~10mL的水,再安装上去),回流冷凝管。
(2)加热回流至分水器中水位不再上升为止(当水充满时,可以由活塞放出)。蒸汽回流的高度:超过冷凝管进水口高度2~3cm即可。
(3)冷却(不可以拆卸回流冷凝管)后。将烧瓶中的混合物与分水器中的酯层合并,转入分液漏斗中。
(4)依次用10mL水,10mL10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥。
(5)重蒸(略)。
(6)用一干燥的小烧杯称产品重量(或用量筒量取产品体积)。测其产品折光率。
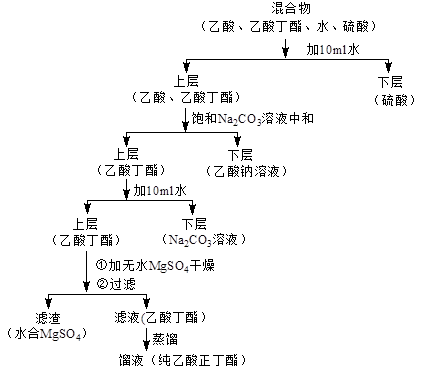 纯化流程:
纯化流程:
产品:乙酸正丁酯,有水果香味的无色液体。产量 g(或 ml),产率 %。
折光率: 。
讨论:
七、实验注意事项
1、在分水器中预先加水量应略低于支管口的下沿。
2、滴加浓硫酸时,要边加边摇,以免局部碳化。
3、本实验中不能用无水氯化钙为干燥剂,因为它与产品能形成络合物而影响产率。
八、思考题
1、酯化反应有哪些特点?本实验中如何提高产品收率?又如何加快反应速度?
2、在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去哪些杂质?若改用氢氧化钠溶液是否可以?为什么?
附:提纯流程图

