无机制备实验报告格式(一)
实验名称:五水合硫酸铜的制备
系 专业 年级 班 学号 姓名 实验日期
一、 实验目的 (略写)
二、 制备反应式及有关计算(原料、产量)(略)
三、 简略实验步骤
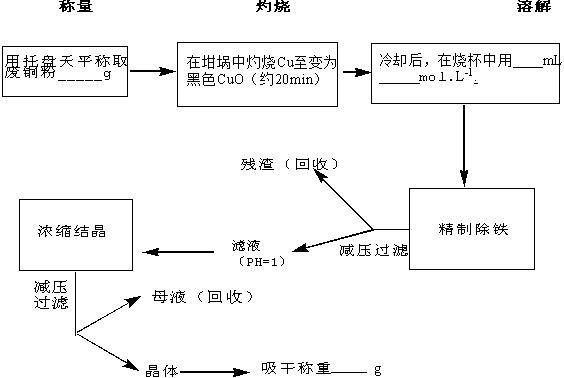
四、 实验结果
产量= ;产率(%)=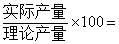 ;
;
产品等级(如果经过检验分析): 。
五、 问题与讨论
无机测定实验报告格式
实验名称:气体常数的测定
系 专业 年级 班 学号 姓名 实验日期
一、 实验目的(略写)
二、 简略实验步骤
1、 称量操作
用托盘天平称表面皿( g)→mol·L-1用电子分析天平称表面皿( g)→用电子天平称表面皿+铝箔共( g)→ 铝箔 g。
2.测气体常数
在反应管内加入3mL 8mol·L-1 的HCl和铝箔→试漏→反应→读书记录→计算。
三、 数据记录与结果处理
1、测量气体常数(R)
反应前量气管中液面读数:V1= mL;
反应后量气管中液面读数:V2= mL;
V(H2)= mL。
铝箔质量 g,n(H2)= mol(计算式)。
室温= ℃,T= K, p(H2O)= Pa;
大气压p= k Pa; p(H2)= kpa。
结果:R= 。
2、相对误差(%)=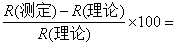 。
。
3、误差分析
无机验证性实验
实验名称:单、多相离子平衡
系 专业 年级 班 学号 姓名 实验日期
一、 实验目的(略写)
二、 实验步骤
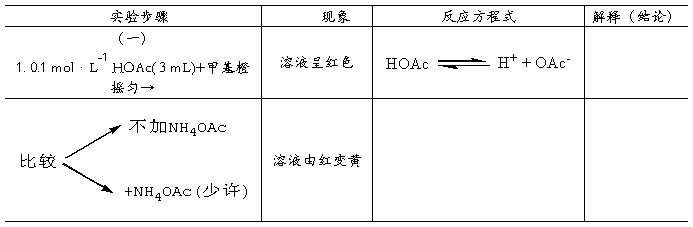
三、问题与讨论
第二篇:无机化学实验报告:常见阳离子的分离与鉴定
实验十二 常见阳离子的分离与鉴定
【学习目标】
认知目标:巩固和进一步掌握一些金属离元素及其化合物的性质。掌握常见阳离子的鉴定反应。 技能目标:常见阳离子鉴定反应的条件控制。
思想目标:培养学生仔细认真、尊重实验事实的良好习惯。
【教学安排】
一 课时安排:3课时
二 实验要点:1、碱金属、碱土金属离子的鉴定
2、p区和ds区部分金属离子的鉴定;
【重点、难点】
常见阳离子的鉴定反应及其反应的条件控制。
【教学方法】 实验指导、演示、启发
【实验指导】
一、碱金属、碱土金属离子的鉴定
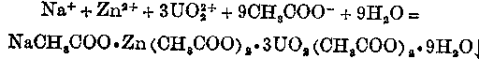
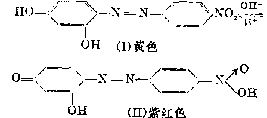
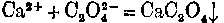
离子 方法、试剂 现象
白色晶形↓
:KSb(OH)6
Na+解释及方程式 (中性)(酸性)
在中性或醋酸性介质中(浅黄绿色) 擦试管壁破坏过饱和
现象,促使↓生成。
淡黄色↓ 95%乙醇和8滴醋酸铀铣锌,用玻棒擦试管壁。
饱和酒石酸氢钠
白色晶形↓
NaHC4H4O6
K+KCl + NaHC4H4O6 = KHC4H4O6↓+ NaCl
:Na3[Co(NO2)6]
亚硝酸钴钠 亮黄色↓ 2K++Na+ + CO(NO2)63- = K2Na[CO(NO2)6]↓
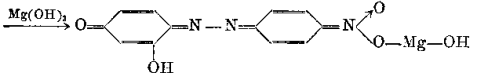
镁试剂在酸性中显黄色,在碱中显紫红色,在NaOH
Mg2+:6 mol·L-1 NaOH
→ 镁试剂1滴 介质中与Mg2+作用生成天蓝色沉淀。大量的NH4+妨碍天蓝色↓ Mg(OH)2的生成会干扰鉴定(对硝基间偶氮苯二酚)。
10 d饱和(NH4)2C2O4
Ca2+→→↓
→6 mol·LHAc
→2 mol·LHCl -1 -1 白色晶形↓ ↓不溶 ↓溶 Ca2+ 在氨性或醋酸性溶液中均能生成 CaC2O4白色沉淀,此沉淀溶于强酸。
黄色↓ Ba2+ 2d 2mol·L-1HAc、 2d 2mol·L-1NaAc→ 2d 1mol·L-1K2CrO4 不溶 NaOH Pb2+也有相同反应 但溶 NaOH HAc-NaAc 调 pH=4~5; BaCrO4 可溶解在稀HCl、稀HNO3 中,但不溶于HAc和 NaOH溶液中。二、p 区和 ds 区部分金属离子的鉴定;离子 方法、试剂 :2d 2mol·L-1HAc、2d 1%铝试剂 1 →水△→ 此沉淀在pH4~5 溶液中呈桃红色,在pH6~7 溶液中呈 可用过量NaOH处理后的试液 (Al3+ 紫红色, 3+有干扰, Fe 变为AlO2-)加HAc酸化后调节pH4~5。 红色絮状↓ (金黄色素三羧酸胺) NH3H2O:降低酸度 现象 解释及方程式mol·L-1 NH3H2O铝试剂又称试铝灵,俗名 为玫红三羧酸三胺,学名 Al3+ 3-(双(3-羧 基-4-羟基苯 基 ) 亚 甲 基 )-6- 氧 -1,4- 环 己烯-1-羧酸三铵盐.它与 铝 盐形成红色内络盐,加 入氨水则则形成红色沉 淀. 性状:棕黄色或棕红色粉 末。易溶于水,溶于乙醇。 Sn2+ 逐滴 0.2 mol·L-1 HgCl2 : 1mol·L K2CrO4 2d Pb2+-1白↓→灰→黑 除强还原剂,一般离 子不干扰。 黄色↓ 溶于 NaOH (Pb2+的鉴定应在中性 或微酸性条件进行。)Hg2Cl2+Sn2++4Cl-= 2Hg↓黑色+ SnCl62- ( Sn2+量多) Hg2+ + Sn2++4Cl-= Hg2Cl2↓白色+SnCl62- ( Sn2+量少) (Sn2+可使红色甲基橙变为无色。) Pb2+ + CrO42-=PbCrO4↓ (溶于HNO3、NaOH不溶醋酸) PbCrO4 +OH-→PbO22-→ → 2 mol·L-1 NaOHBi2+→1d 2.5%硫脲黄色溶液黄色络合物 注意:Bi2+会水解使反应失效,可在强酸介质中反应。Cu2+1d6mol·L-1HAc → K4[Fe(CN)6](亚铁氰化钾)2Cu2+ + [Fe(CN)6]4 红棕↓-→Cu2 [Fe(CN)6]↓红棕Fe3+会与试剂→深蓝色↓干扰。白↓→↓溶解→白Ag+HCl→AgCl ↓ →氨水→↓溶解 →HNO3酸化 2d 2mol·L-1HAc →(NH4)2[Hg (SCN) 4]擦试管壁↓在中性或微酸性条件下: 白↓ Zn2++Hg (SCN) 42-=Zn[Hg (SCN) 4]↓ 相同条件下:Cu2+→黄绿色↓Co2+→蓝色↓Zn2+
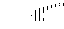
Cd2+ + S2-=Cd S↓
Cd2+2d 0.5mol·L-1 Na2S L亮黄色↓ 弱酸性条件下与H2S反应生成亮黄色↓,一二组阳离子
有干扰,可将硫化物↓用3 mol·L-1 HCl处理,,再取离心液加入3 mol·L-1 NaOH碱化,析出黄色↓。
Hg2+逐滴0.5 mol·L-1
Hg2+ + Sn2++4Cl-= Hg2Cl2↓白色+SnCl62- ( Sn2+量少)白↓→灰→黑 Hg2Cl2+Sn2++4Cl-= 2Hg↓黑色+ SnCl62- ( Sn2+量多) SnCl2
[问题讨论]
1、KCl、Cd(NO3)2、AgNO3、ZnSO4 。用NaOH可区别
KCl
Cd(NO3)2
AgNO3
ZnSO4
2、
Cu2+
Zn2+
Hg2+
Cd2+适量NaOH: 无明显现象√ 白色Cd(OH)2↓ 黑色Ag2O↓√ 白色Zn(OH)2↓ 饱和H2S 黑CuS 白色ZnS↓ 黑色HgS↓ 黄色CdS↓ 过量NaOH 无明显现象 ↓不溶解 √↓不溶解 ↓溶解ZnO22√ -
