实验 水的硬度的测定
姓名: 班级: 学号:
一、 实验目的
1、 掌握水的硬度测定方法及其计算
2、 巩固铬黑T指示剂的终点控制
二、 实验试剂
1、 EDTA标准溶液
2、 氨性缓冲液
3、 铬黑T指示剂
三、 实验步骤
用25的移液管分别移取水样四次放入锥形瓶中,加入10氨性缓冲溶液,再加入2~3滴铬黑T指示剂,用EDTA标准溶液滴定至终点,记录读数,平行测定3次,根据计算公式计算出水样的硬度。
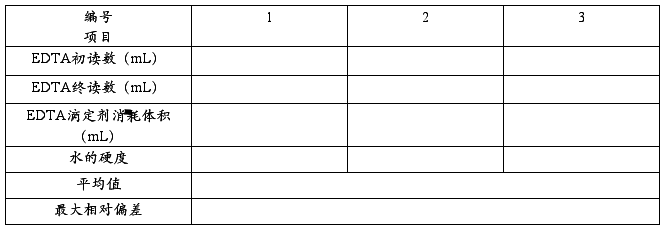
四、数据记录 EDTA浓度 水样
第二篇:实验十 水的硬度测定(修改)
实验十 水硬度的测定
一、目的
1. 了解水硬度的测定意义和常用的硬度表示方法。
2. 掌握EDTA法测定自来水硬度的原理和方法。
3. 掌握铬黑T和钙指示剂的应用,了解金属指示剂的特点。
二、原理
一般含有钙,镁盐类的水叫硬水(硬水和软水尚无明确的界限,硬度小于5、6度的,一般可称软水)。硬度有暂时硬度和永久硬度之分。 暂时硬度——水中含有钙、镁的酸式碳酸盐,遇热即成碳酸盐沉淀而失去其硬性。反应如下:
Ca(HCO3)2 → CaCO3(完全沉淀)+H2O+CO2↑
Mg(HCO3)2→MgCO3(不完全沉淀)+H2O+CO2↑
+H2O
Mg(OH)2↓+CO2↑
永久硬度——水中含有钙、镁的硫酸盐、氯化物、硝酸盐,再加热亦不沉淀(但在锅炉运行温度下,溶解度低的可析出而成为锅垢)。 暂硬和永硬的总和称为“总硬”。由镁离子形成的硬度称为“镁硬”,由钙离子形成的硬度称为“钙硬”。
水中钙、镁离子含量,可用EDTA法测定。钙硬测定原理与以CaCO3为基准物标定EDTA标准溶液浓度相同。总硬则以铬黑T为指示剂,控制溶液的酸度为≈10,以EDTA标准溶液滴定。由EDTA溶液的浓度和用量,可算出水的总硬,由总硬减去钙硬即为镁硬。
水的硬度的表示方法有很多种,随各国的习惯而有所不同。有将水中
的盐类都折算成CaCO3而以CaCO3的量作为硬度标准的。目前常用的表示方法:以度()计,1硬度单位表示十万份水中含1份CaO,1=10ppmCaO(ppm为百万分之几,即为parts per million 的缩写)。
MCaO
CEDTA●VEDTA×———
1000
硬度()= ——————————×105 。。。
V水
式中 CEDTA——EDTA标准溶液的浓度(单位:mol/L);
VEDTA——滴定时用去的EDTA标准溶液的体积(单位:mL),若此量为滴定总硬时所耗用的,则所得硬度为总硬,为滴定钙硬时所耗用的,则所得硬度为钙硬。
V水 ——水样体积(单位:mL);
MCaO——CaO的摩尔质量(单位:g/mol)。
三、试剂
0.02mol/LEDTA标准溶液,NH3-NH4Cl缓冲溶液(pH≈10),10%NaOH溶液,钙指示剂,铬黑T指示剂。
四、实验步骤
1.总硬的测定:准确量取澄清的自来水样100mL,放入锥形瓶中,加入5ml NH3-NH4Cl缓冲液,摇匀。再加入约0.01g铬黑T固体指示剂,再摇匀,此时溶液呈酒红色。以0.02mol/LEDTA标准溶液滴定至纯蓝色,即为终点。
2.钙硬的测定:准确量取澄清的自来水样100mL,放入锥形瓶中,加入
4mL 10%NaOH溶液,摇匀。再加入约0.01g钙指示剂,再摇匀。此时溶液呈淡红色。用0.02mol/L EDTA标准溶液滴定至呈纯蓝色,即为终点。
3.镁硬的确定:由总硬减去钙硬即得镁硬。
