重铬酸钾法
一、实验目的和要求
(1)了解COD测定的意义与方法。
(2)掌握重铬酸钾法测定COD的原理和操作技术。
(3)熟悉密封消解分光光度法测定COD的原理及操作流程。
二、基本原理
在强酸性溶液中,用K2Cr2O7氧化水样中的还原性物质,过量的K2Cr2O7以试亚铁灵做指示剂,用硫酸亚铁铵标准溶液回滴,根据其用量计算水样中还原性物质消耗氧的量。
反应式如下:
Cr2O72- + 14H+ + 6e = 2Cr3+ + 7H2O
(橙红色) (蓝绿色)
Cr2O72- + 14H+ + 6Fe2+ = 6Fe3+ + 2Cr3+ + 7H2O
三、实验仪器
1、500mL全玻璃回流装置。
2、电炉
3、酸式滴定管、锥形瓶、移液管、容量瓶
四、试剂
(1)重铬酸钾标准溶液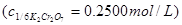 :称取预先在120℃烘干2h的基准或优级纯重铬酸钾12.2580g溶于水中,移入1000mL容量瓶中,稀释至刻线,摇匀。
:称取预先在120℃烘干2h的基准或优级纯重铬酸钾12.2580g溶于水中,移入1000mL容量瓶中,稀释至刻线,摇匀。
(2)亚铁灵指示液:称取1.485g邻啡啰啉(C12H8N2·H2O)、0.695g硫酸亚铁(FeSO4·7H2O)溶于水中,稀释至100mL,贮存于棕色瓶中。
(3)硫酸亚铁铵标准溶液(约0.1mol/L):称取39.5g硫酸亚铁铵溶于水中,边搅拌近缓慢加入20mL浓硫酸,冷却后移入1000mL容量瓶中,加水稀释至标线,摇匀。临用前用重铬酸钾标准溶液标定,标定方法如下:
准确吸取10.00mL重铬酸钾标准溶液于500mL锥形瓶中,缓慢加入30mL浓硫酸,混匀。冷却后,加入3滴试亚铁灵指示剂(约0.15mL),用硫酸亚铁铵溶液滴定,溶液的颜色由黄色经蓝绿色至红褐色即为终点。按照下式计算硫酸亚铁铵的浓度:
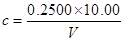
式中:c—硫酸亚铁铵标准溶液的浓度(mol/L);
V—硫酸亚铁铵标准溶液的用量(mL)。
表1-3 硫酸亚铁铵的标定结果

要求:
平行测定3份。
(4)硫酸-硫酸银溶液:于500mL浓硫酸中加入5g硫酸银。放置1~2d,不时摇动使其溶解。
(5)硫酸汞:结晶或粉末。
五、测定步骤
1、水样的采集与保存
水样要采集在玻璃瓶中,应尽快分析。如不能立即分析时,应加入浓硫酸至pH值小于2,置于4以下保存。但保存时间不多于5天。采集水样的体积不得少于100mL。
2、硫酸亚铁铵的标定
准确吸取10.00mL重铬酸钾标准溶液于500mL锥形瓶中,缓慢加入30mL浓硫酸,混匀。冷却后,加入3滴试亚铁灵指示剂(约0.15mL),用硫酸亚铁铵溶液滴定,溶液的颜色由黄色经蓝绿色至红褐色即为终点。
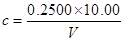
式中:c—硫酸亚铁铵标准溶液的浓度(mol/L);
V—硫酸亚铁铵标准溶液的用量(mL)。
3、水样的测定
取20.00mL水样置于三角瓶中,准确加入10.00mL重铬酸钾和数粒防爆玻璃珠 ,接好磨口回流冷凝管, 从冷凝管上端慢慢加入30mL催化剂(硫酸-硫酸银溶液),轻轻摇动锥形瓶使溶液混匀。 加热回流2h(自开始沸腾时算起)。
冷却后,用20~30mL蒸馏水自冷凝管上端冲洗冷凝管,然后取下锥形瓶,用水稀释至140mL左右。
用硫酸亚铁铵标准溶液滴定溶液,加3滴试亚铁灵指示剂,用硫酸亚铁铵标准溶液滴定,溶液的颜色由黄色经蓝绿色至红色即为终点,记录消耗硫酸亚铁铵的体积V1。
4、空白实验
以20.00mL蒸馏水代替水样,除不回流外,按与水样测定同样操作步骤加试剂,并用硫酸亚铁铵滴定。
六、计算

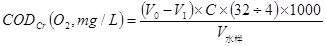
V0——滴定空白时硫酸亚铁铵标准溶液用量;mL
V1——滴定水样时硫酸亚铁铵标准溶液用量;mL
c——硫酸亚铁铵标准溶液浓度;mol/L
V——水样体积;mL
七、注意事项
(1) 使用0.4g硫酸汞络合氯离子的最高量可达40mg,如取用20.00mL水样,即最高可络合2000mg/L氯离子浓度的水样。若氯离子的浓度较低,也可少加硫酸汞,使保持硫酸汞∶氯离子=10∶1(W/W)。若出现少量氯化汞浓淀,并不影响测定。
(2)水样取用体积可在10.00~50.00mL范围内,但试剂用量及浓度需按下表进行相应调整,也可得到满意的结果。
(3)对于化学需氧量小于50mg/L的水样,应改用0.0250mol/LK2Cr2O7溶液。回滴时用武之地0.01mol/L硫酸亚铁铵标准溶液。
(4)水样加热回流后,溶液中重铬酸钾剩余量应为加入量的1/5~4/5为宜。
(5)用邻苯二甲酸氢钾标准溶液检查试剂的质量和操作技术时,由于每克邻苯二甲酸氢钾的理论CODCr为1.176g,所以溶解0.4251g邻苯二甲酸氢钾于重蒸馏水中,转入1000mL容量瓶,用重蒸馏水稀释至标线,使之成为500mg/L的标准溶液。用时新配。
(6)CODCr的测定结果应保留三位有效数字。
(7)每次实验时,应对硫酸亚铁铵标准滴定溶液进行标定,室温较高时尤其注意其浓度的变化。
八、思考题
采用重铬酸钾回流法测定化学需氧量(CODCr)时,加入K2Cr2O7标准溶液后,水样变为绿色,说明什么?遇到这种情况该怎么办?
第二篇:趣味实验实验报告
试验5 趣味实验
(化学化工学院 10级化学三班 李阳 学号:41007115)
一、 化学实验趣味化的的意义
化学实验能够引起学生的认知兴趣,如果把实验作趣味化处理,则更能引起学生的兴趣,产生强烈的学习动机。按照趣味实验在教育中由浅入深的作用,可分为观察性趣味实验,操作性趣味实验,探索性趣味实验和创造性趣味实验,从趣味实验的应用范围来看,是十分广泛的。课堂教学活动用于导入新课、重难点的设疑与解惑,课外活动如游艺表演,生活中的化学,社会中的化学,科学技术中的化学等,通过化学实验的趣味化活动,使学生的思维更加活跃,手脑并用的能力更强,创新意识和创造精神得到充分发挥。
二、实验原理
1.蓝色振荡
亚甲基蓝又名次甲基蓝,是一种指示剂。在氧化态时为蓝色,还原态时为无色。在碱性条件下,葡萄糖将蓝色的亚甲基蓝还原成无色的亚甲基白。当瓶子被振荡时,空气中的氧气又将还原态的亚甲基白氧化成氧化态的亚甲基蓝。所以,溶液由无色又变为蓝色。
如果滴加酚酞试剂的话,我们会发现颜色变化为红色与紫色。原因是当溶液在碱性条件下时,滴加酚酞试剂后溶液显红色。所以:当葡萄糖把亚甲基蓝还原为无色时,由于溶液显强碱性,此时溶液呈红色;搅拌或略微震荡条件下空气会把部分无色产物氧化为蓝色,由于紫色与蓝色相混,由于颜色的混合效应,我们将看到此时溶液显紫色。
2.化学冰袋
几种特殊的铵盐如硝酸铵、硫酸铵等,溶于水时具有强烈吸热降温的性质,它们还可以从与其相接触的晶体盐中夺取结晶水而溶解吸热,利用这种性质,可以通过简单地混合几种盐而制冷,制成化学“冰袋”。该种便携式“冰袋”可应用于需简便制冷的场合,如外出郊游时,对饮料和食品的保鲜、制冷。
3.固体汽水
由于液体汽水运输昂贵,携带不太方便,因此我们将汽水中
加压压缩CO2变为临时释放CO2 。碳酸氢钠俗称小苏打,遇到酸性物质(如醋酸,柠檬酸等)就会产生大量二氧化碳气体。因此固体汽水的制备原理就是是在碳酸氢钠外层包一层明胶,与柠檬酸隔绝,再加些香精、色素、白砂糖等添加剂。明胶遇水溶解即可让碳酸氢钠和柠檬酸发生反应产生二氧化碳气体,所以饮用时用水冲一下便可,喝起来口感和液体汽水相似,味道也很不错。反应方程式:
三、实验药品试剂
碘量瓶、烧杯、NaOH固体、葡萄糖、亚甲基蓝溶液、酚酞、软质塑料袋、托盘天平、药匙、十水硫酸钠、硫酸铵、硫酸氢钠、硝酸铵、量筒、玻璃棒、滴管、酒精灯、三角架、电吹风、明胶、碳酸氢钠、无水柠檬酸、蔗糖、柠檬黄
四、实验步骤
1.蓝色振荡
烧杯中加2.5gNaOH,用120mL蒸馏水溶解,溶解之后向烧杯中加入3.4g葡萄糖,用玻璃棒搅拌溶解;
将上述的溶液移入碘量瓶中,加0.5mL亚甲基蓝溶液,盖上瓶塞,振荡溶液后变蓝,静置碘量瓶片刻,可观察到溶液由蓝色变为无色的现象。再振荡碘量瓶,溶液变蓝,静置溶液又变为无色,若反复进行这样的操作,现象相同。
实验现象:溶液由蓝色变为无色的现象。再振荡碘量瓶,溶液变蓝,静置溶液又变为无色,若反复进行这样的操作,现象相同。
反应实质: 亚甲基蓝 亚甲基白
O
加入酚酞,操作和上面相同,会发现溶液在红色和紫色之间反复。
2.化学冰袋
在托盘天平上称取12十水硫酸钠,10g硫酸氢钠,10g硫酸铵和6.25g硝酸铵,将其混合于一软塑料袋中。对其进行揉搓。
实验现象:揉搓后,感觉温度明显下降。
反应本质:铵盐溶解在结晶水中吸热。
3.固体汽水 2OH- 葡萄糖
(1)配制明胶溶液:用托盘天平称取0.1g的明胶酒精灯加热溶于10mL水中;
(2)给NaHCO3加一层明胶:取2.5g NaHCO3放入研钵中研碎,转移至小烧杯中,向其加入1mL已配好的明胶溶液,搅拌均匀,并用电吹风将其吹干。
(3)称取4g柠檬酸,4g蔗糖,少许柠檬黄与上述固体在研钵中混合均匀,将其转移到大烧杯中,加水即可发现溶液中有大量的气体冒出,溶液显黄色,此气体就是二氧化碳气体,显黄色是因为色素为柠檬黄,此溶液就是简单的碳酸饮料。
实验现象:溶液中有大量的气体冒出,溶液显黄色。 柠檬黄的颜色为黄色,所以溶液显黄色。
五、实验注意事项
1、明胶微热溶解时不可温度太高,烧杯距离火焰需保持一定的距离,原因是明胶是一种蛋白质,高温容易变性。
2、称量NaOH时需用烧杯,纸张要现称现用,这样也会产生潮解。当然由于此实验主要是要一个碱性环境,所以此影响在此实验中可以忽略。
3、冰袋制作不能使用无水碳酸钠(纯减)粉末,必须是含结晶水的晶体碳酸钠或成块状纯碱。可以将无水碳酸钠粉末溶于水,然后加热浓缩至晶体析出,自制晶体碳酸钠。
六、实验反思
1、化学是一门实验科学,化学实验能够引起学生的认知兴趣,如果把实验做趣味化处理,则更能引起学生的兴趣,产生强烈的学习动机。我们本次实验包括观察性趣味实验和操作性趣味实验。
2、作为一名准化学教师,做好演示实验是很重要的一项教
学技术,尤其是趣味实验,它在激发学生学习化学方面起着很重要的作用。而在这次演示实验时,我由于过于紧张,所以出现了小差错,而且讲解实验的方式也不够生动,没有“趣味”,没有很好的达到趣味实验所要求达到的目的。
