广州大学学生实验报告
开课学院及实验室: 室 年 月 日

第二篇:华师11级磁化率报告
学生姓名 学 号
专 业 年级、班级
课程名称 实验项目
实验类型 实验时间 2013年 10 月 15 日
一、实验目的
1.掌握古埃(Gouy)磁天平测定物质磁化率的实验原理和技术。
2.通过对一些配合物磁化率的测定,计算中心离子的不成对电子数.并判断d电子的排布情况和配位体场的强弱。
二、实验原理
(1)物质的磁性
物质在磁场中被磁化,在外磁场强度H(A·m-1)的作用下,产生附加磁场H'。这时该物质内部的磁感应强度B为外磁场强度H与附加磁场强度H'之和:
B=H十H'=H+4πI=H十4πκH (1)
式中,I称为体积磁化强度,物理意义是单位体积的磁矩,式中的κ=I/H称为物质的体积磁化率、表示单位体积物质的磁化能力,是无量纲的物理量。I和κ分别除以物质的密度ρ可以得到σ和χ,σ=I/ρ称为克磁化强度;χ=κ/ρ称为克磁化率或比磁化率。Χm=κM/ρ称为摩尔磁化率(M是物质的摩尔质量)。这些实验数据都可以从实验测得,是宏观磁性质。在顺磁、反磁性研究中常用到χ和χm,铁磁性研究中常用到I、σ。
不少文献中按宏观磁性质,把物质分成反磁性物质、顺磁性物质和铁磁性物质以及亚铁磁性物质、反铁磁性物质几类。其中顺磁性物资的χm>0而反磁性物质的χm<0。
(2)古埃法(Gouy)测定磁化率
古埃法是一种简便的测量方法,主要用在顺磁测量。简单的装置包括磁场和测力装置两部分。调节电流大小,磁头间距离大小,可以控制磁场强度大小。测力装置可以用分析天平。为了测量不同温度的数据,要使用变温、恒温和测温装置。
样品放在一个长圆柱形玻璃管内,悬挂在磁场中,样品管下端在磁极中央处,另一端则在磁场强度为零处。
样品在磁场中受到一个作用力。
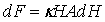
式中,A表示圆柱玻璃管的截面积。
样品在空气中称量,必须考虑空气修正,即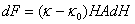
 0表示空气的体积磁化率,整个样品的受力是个积分问题:
0表示空气的体积磁化率,整个样品的受力是个积分问题:
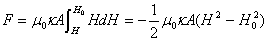
因H0<<H,且忽略 0,则
0,则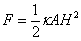
式中,F可以通过样品在有磁场和无磁场的两次称量的质量差来求出。
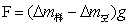
式中,Δm样为样品管加样品在有磁场和无磁场时的质量差;Δm空为空样品管在有磁场和无磁场时的质量差;g为重力加速度。
则有,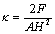
而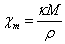 ,
, ,h为样品高度,A为样品管截面积,m样品为样品质量。
,h为样品高度,A为样品管截面积,m样品为样品质量。

 ①
①
只要测量样品重量的变化,磁场强度H以及样品高度h,即可根据公式①计算样品的摩尔磁化率。
在实际工作中是采用已准确知道磁化率数值的校准样品来标定磁场,根据①式:
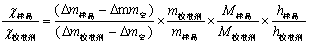 ②
②
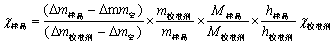 ③
③
常用的校准样品有(NH4)2SO4 FeSO4·6H2O(莫氏盐)、HgCo(CNS)4、Ni(en)3S2O3。其中,(NH4)2SO4 FeSO4·6H2O的磁化率符合公式:
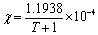 ④ 式中,T是绝对温度。
④ 式中,T是绝对温度。
(3)简单络合物的磁性与未成对电子
对于第一过渡系列元素络合物,它们的磁矩实验值大多符合
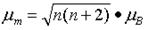 ⑤
⑤
式中,n是分子中未成对电子数;μB是电子磁矩的基本单位,称为波尔磁子。
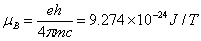 ⑥
⑥
而磁矩μm与摩尔顺磁磁化率χm之间有如下关系:
 ⑦
⑦
式中,NA为阿伏伽德罗常数;K为波兹曼常数;T为绝对温度。
根据⑦式可以利用测量出的物质的摩尔顺磁化率χm计算出μm,然后根据⑤式计算样品的未成对电子数。若测得的χm<0则表示物质是反磁性物质,未成对电子数为零。
三、仪器及试剂
(1)仪器 磁天平一台,样品管一支,直尺一把,温度计一支。
(2)试剂 莫尔氏盐(NH4)2SO4 FeSO4·6H2O,分析纯;硫酸亚铁FeSO4·7H2O,分析纯;亚铁氰化钾K4Fe(CN)6·3H2O,分析纯。
四、实验步骤与数据记录
标定磁场强度方法如下。
1、取一只清洁干燥的样品管悬挂在磁天平的挂钩上,测量得m空。
2、调节电流开关,至1A,测得m空1。
3、继续调大电流,至3A,测得m空2。
4、继续调大电流,至4A,停留一定时间后,调小电流回到3A测得m空2’。
5、继续调小电流到1A,测得m空1’。
6、关闭电流测得m空 ’。
表1 数据记录表(空管)

7、装入已经研细的莫氏盐,装样尽量填实,样品要装至距离管口约1~2cm处,用直尺测量装样的高度,将样品管放入磁天平,按照空管的测量方法测量样品管的重量。
表2 样品:莫氏盐,装样高度:13.40cm
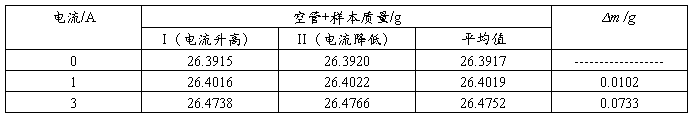
(8)倒出样品管中的莫氏盐,将样品管清洗干净。装入研细的硫酸亚铁,装样高度和莫氏盐尽量相同,用同样的方法测量硫酸亚铁的数据。
表3 样品:硫酸亚铁,装样高度:13.45 cm
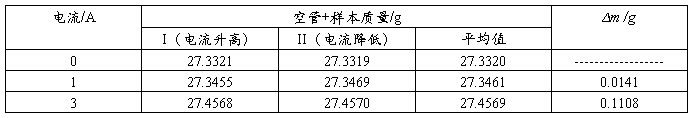
(9)倒出样品管中的硫酸亚铁,将样品管清洗干净。装入研细的亚铁氰化钾,装样高度和莫氏盐尽量相同,用同样的方法测量亚铁氰化钾的数据。
表4 样品:亚铁氰化钾,装样高度:13.35 cm
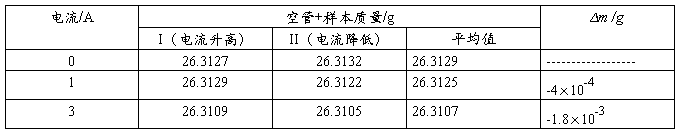
五、数据处理
(1)样品的磁化率
其中 T=31.20℃=328.2K M莫氏盐=392.14 g/mol
莫氏盐的磁化率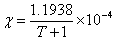 =3.6264×10-7 m3/kg =1.4221×10-7m3/mol
=3.6264×10-7 m3/kg =1.4221×10-7m3/mol
(2)待测样品的摩尔磁化率χm
由公式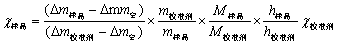 可以分别计算电流强度为1A、3A时,硫酸亚铁、亚铁氰化钾的磁化率和摩尔磁化率。数据处理如下表:(其中M莫氏盐=392.14 g/mol M硫酸亚铁=278.03g/mol M亚铁氰化钾=422.39 g/mol χ校准剂=3.6264×10-7 m3/kg)
可以分别计算电流强度为1A、3A时,硫酸亚铁、亚铁氰化钾的磁化率和摩尔磁化率。数据处理如下表:(其中M莫氏盐=392.14 g/mol M硫酸亚铁=278.03g/mol M亚铁氰化钾=422.39 g/mol χ校准剂=3.6264×10-7 m3/kg)
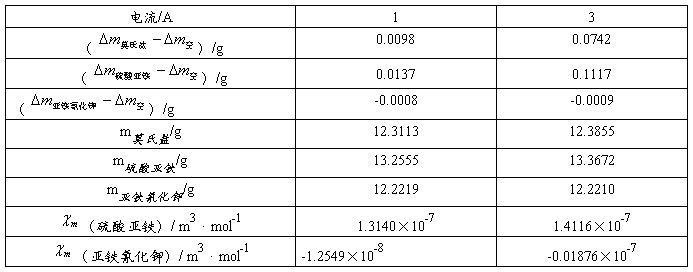
则硫酸亚铁(FeSO4·7H2O)的摩尔磁化率平均值为:
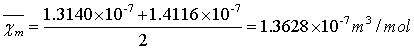
亚铁氰化钾K4Fe(CN)6·3H2O的摩尔磁化率平均值为:
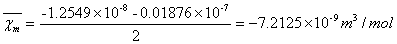
(3)根据χm计算样品的未成对电子数
a、对于硫酸亚铁(FeSO4·7H2O):
由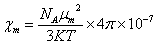 得:
得:
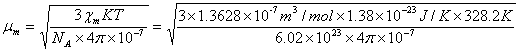

又因为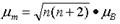 (其中μB=9.274078×10-24)
(其中μB=9.274078×10-24)
所以:
当n=1时,μm=1.6063×10-23 J2/T2;
当n=2时,μm=2.6231×10-23 J2/T2;
当n=3时,μm=3.5918×10-23 J2/T2;
当n=4时,μm=4.5434×10-23 J2/T2;
当n=5时,μm=5.4866×10-23 J2/T2。
由此可以看出,计算硫酸亚铁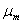
 ,接近μm=4.5434×10-23 J2/T2,因此FeSO4·7H2O的未成对电子数是4。
,接近μm=4.5434×10-23 J2/T2,因此FeSO4·7H2O的未成对电子数是4。
b、对于duK4Fe(CN)6·3H2O
因为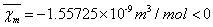 ,故亚铁氰化钾是反磁性物质,未成对电子数为0。
,故亚铁氰化钾是反磁性物质,未成对电子数为0。
六、实验结果与讨论
结果:
(1)实验测得硫酸亚铁摩尔磁化率为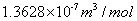 ,亚铁氰化钾摩尔磁化率为
,亚铁氰化钾摩尔磁化率为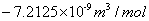 。因此硫酸亚铁磁矩大于0,为顺磁性,硫酸亚铁存在磁矩这说明了存在未成对电子数,计算求得n约等于4。亚铁氰化钾磁矩小于0,为反磁性。
。因此硫酸亚铁磁矩大于0,为顺磁性,硫酸亚铁存在磁矩这说明了存在未成对电子数,计算求得n约等于4。亚铁氰化钾磁矩小于0,为反磁性。
(2)从晶体场理论看,硫酸亚铁中心原子以高自旋排布,亚铁氰化钾中心原子采用低自旋排布,所以亚铁氰化钾磁矩较小。
(3)从分子轨道理论分析,硫酸亚铁中心原子与给电子配体只能形成共价键,推电子的配体形成八面体配合物,磁矩与中心离子的磁矩相近。而亚铁氰化钾中心原子与受电子配体能形成配键和反馈π键,受电子的配体形成八面体配合物,磁矩远小于中心离子的磁矩。
讨论:
通过计算,实验所得结果与文献值比较接近,但还是存在一定的误差,造成误差的可能原因:
1、环境的干扰,实验实际操作过程中周围有很多人走动、说话等等,在干扰磁场因素的环境下进行,空气流动会对称量有影响。
2、样品没有研磨细小均匀,样品与标样的填充高度没有保持一致。
3、装样不紧密也会带来较大误差,高度h就会比理论值偏大,即使很准确地测量出高度h,它还是比理论值有一个误差。因此装在样品管内的样品要均匀紧密、上下一致、端面平整。
3、测量样品高度h的误差严重影响实验的精度,这从摩尔磁化率的计算公式 可以看出来。而由于最上面的那些样品粉末不能压紧压平,测量高度h的误差还是比较大的。因此装样是测量高度要准确。
5、由于样品都是研磨完后一段时间才开始测量的,不排除样品会发生相应的吸水和失水,致使分子量会发生变化,使最后所计算出来的结果存在误差。
6、样品管的底部没有置于电磁铁的极缝中心,没有把样品管底与磁极中心线平行,造成磁场不均匀,这样也会产生误差。
7、读数时因时间间隔不同所造成的误差。
8、本次实验是小组合作的,装样和读数等不同的人操作也会产生误差,还有操作是否规范等。
七、思考题
1、实验操作中应该主要的问题。
(1)所测样品要研磨充分、均匀,注意干燥防止,减少水分吸收
(2)每次加入样品时,应确保样品管干净
(3)空样品管需要干燥洁净,装样时应该使样品均匀填实
(4)称量时,样品管应正好处于两磁极之间,其底部与磁极中心线齐平。悬挂样品管的悬线及样品管不要与任何物件接触
(5)样品倒回试剂瓶时,注意瓶上所贴标志,切记倒错瓶子。
(6)选用合适的标准样品,需根据测量目的选用,一般选取易得的、稳定性好、纯度高、重现性好的标准样品,并且希望标准样品的磁化率和密度尽可能和测试样品相近。在高磁化率范围内,通常采用莫尔盐为标准样品。
?
参考文献:
[1]何广平,男俊民等.物理化学实验[M].北京.化学工业出版社,2008:131-134
[2]柯以侃.大学化学实验[M]. 北京:化学工业出版社,2001
[3]大连理工大学无机化学教研室.无 机化 学 ( 第 三 版 )[M].北 京:高等教育 出 版社,1990
