实验七 溶液表面张力的测定——最大气泡压力法
一. 实验目的
1. 用最大气泡法测定不同浓度乙醇溶液的表面张力。
2. 了解表面张力的性质,表面自由能的意义以及表面张力和吸附的关系。
3. 学会镜面法作切线的方法。
二. 实验原理
1. 用本法测定[乙醇,水]溶液的数据对[σ,c],作图将c-σ曲线在不同浓度的斜率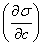 T代入吉布斯等温吸附式:
T代入吉布斯等温吸附式:
Γ=﹣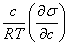 T
T
求出相应的吉布斯吸附量Γ;
按朗格茂尔等温吸附变形公式:
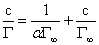
C/Γc-C直线斜率tgβ求出饱和吸附量 ,进而得出乙醇分子横切面积S和分子长度
,进而得出乙醇分子横切面积S和分子长度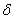 ,结合直线截距得出吸附系数α:
,结合直线截距得出吸附系数α:
 =(tgβ)-1
=(tgβ)-1
以上个式中,c为浓度;T为绝对温度(K);σ为表面张力;Γ为吉布斯吸附量;M为溶质摩尔质量;ρ为溶质密度;S为分子截面积;δ为分子长;α为吸附系数;NA为阿伏伽德罗数(6.02×1023/mol);R为气体常数。为了求以上参数,关键是测σ。
2. 表面张力及界面张力,矢量。源于凝聚相界面分子受力不平衡,意为表面的单位长度收缩力。σ也是在个条件下凝聚系表面相得热力学强度性质,如果恒温、恒压下扩大单位表面积所需的可逆功,故亦称为表面自由焓。
σ与凝聚相和表面共存接触相种类有关,还与T,P有关,与凝聚相纯度和杂志种类有关。浓度升高,溶液的σ有增有减,随溶质、溶剂而异,表面活性剂是两亲分子,他们的水溶液σ随浓度升高先剧降,后微升,在渐趋稳定。σ随c而变化的本质是溶液表面浓度对体相浓度的偏离,此现象称为表面吸附。表面吸附量Γ与浓度有关,用吉布斯等温方程求出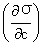 为σ-c曲线在指定浓度的斜率。
为σ-c曲线在指定浓度的斜率。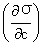 <0, Γ>0为正吸附,表面浓度较体浓度高,达饱和吸附时,Γ趋于饱和吸附量
<0, Γ>0为正吸附,表面浓度较体浓度高,达饱和吸附时,Γ趋于饱和吸附量 ,此时两亲分子在溶液表面处于高度有序的竖立密集,形成单分子膜。,
,此时两亲分子在溶液表面处于高度有序的竖立密集,形成单分子膜。,
若将兰格缪尔等温吸附式中的吸附量赋予吉布斯吸附量的特定意义,则可从其变形式求出 设分子吸附层厚δ,δ即两亲分子长。依δ*ρ=
设分子吸附层厚δ,δ即两亲分子长。依δ*ρ= *M,由此得出求分子的式子。
*M,由此得出求分子的式子。
3. δ的测定方法有环法、滴重法、毛细管上升法等,其中最大气泡法设备简单,易操作,应用广。此法是将下口齐平的毛细管垂直插入试液,并使管口刚与液面相切,则可看到在毛细管内形成凹液面。凹液面受力一是大气压,二是附加压力,因此凹液面受到的总压是p1=p0+△p=p0+2σ/r.
现对管外减压,随管外压力p2=p0+ρg△h减小,|△h|增大,|r|减小,p1随p2同步减小,故p2=p1,得:
σ=rgρ△h/2
由于减压凹液面不断下降,r为不定值,但当凹液面上形成的小气泡降至毛细管下口,并随时气流的瞬间,|r|降至极小,刚等于毛细管下口内径,此时△h 升至最大。若在微微减压。气泡逸出,△h剧降,r为定值,所以只要测出最大的|△h|,即可用上式求出σ。由于r一定。故rgρ/2为定值,称仪器常数K,可用纯水的σ和同条件下实验测得的△h求出。故:
σ=K*△h=σ0*△h/△h0
溶液浓度c用折射仪测出。
四.仪器与药品
仪器:蓄水瓶,毛细管,试管,烧杯,U型水柱压力计,温度计,分液漏斗表面张力仪一套
药品:乙醇溶液:5%,10%,20%,30%,40%,50%
五.实验步骤
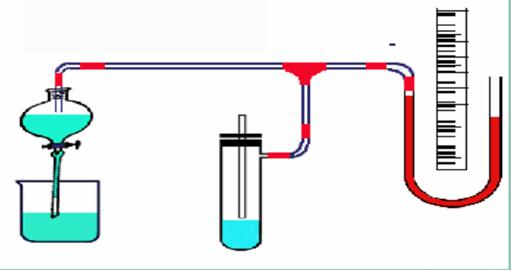
1.按下图安装好实验仪器,检查仪器是否漏气,检查方法如下:由分液往
蓄水瓶中注水,是压力计产生一定的压力差,停止加水,如果压力计维持3~5
分钟不变,可认为不漏气。
2.仔细用热的铬酸洗液洗涤毛细管。
3.毛细管常数的测定:
在清洁的试管中加入约1/4体积的蒸馏水,装上清洁的毛细管,是端面
恰好与液面相接,打开分液漏斗,使水缓缓滴出,以增加毛细管内压力,使气泡
冒出,观察冒出的速度与压力的关系,调节气泡逸出速度不超过每分钟20个,
如此三次,若每次得△h,差别在2mm以内,取平均值,求K。否则重复步骤2,
然后再测。
4.乙醇溶液表面张力的测定:
将试管中的水倒出,用待测溶液洗涤试管和沾洗毛细管(尖端沾取待测
液,然后用耳洗球吹掉内溶液)3次,在试管中装入待测溶液,用上述方法快速
测定浓度为5%,10%,20%,30%,40%,50%的乙醇溶液压力差△h,都测三次取平均
值。
六.数据处理和结果
原始数据表
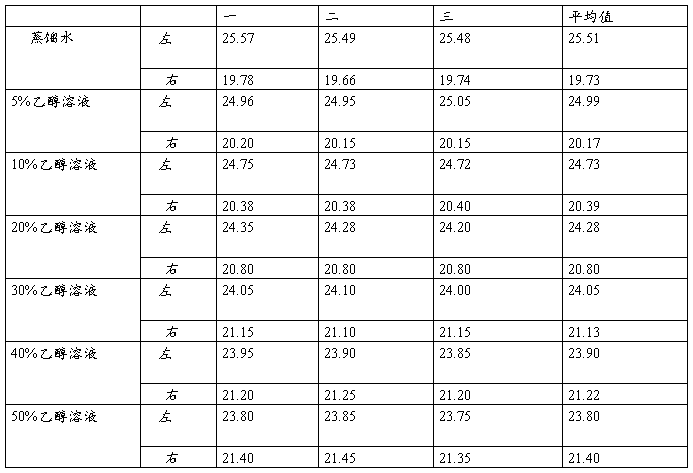
1.将实验记录的数据用表格列出
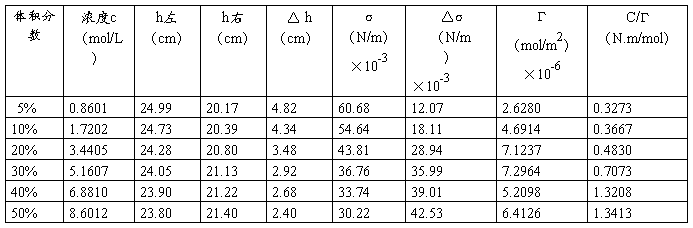
2.利用水的表面张力球毛细管常数k。
由上表知蒸馏水:△h=5.78cm 温度20℃,查表得:б水=72.75×10-3N/m
所以: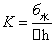 =(72.75/0.0578)×10-3=1.259N/m2
=(72.75/0.0578)×10-3=1.259N/m2
3.计算各浓度乙醇溶液的表面张力。
计算举例:5%的乙醇溶液
б=K×△h=1.259×0.0482=60.68×10-3N/m
其余结果见上表。
4. 作σ-c图。
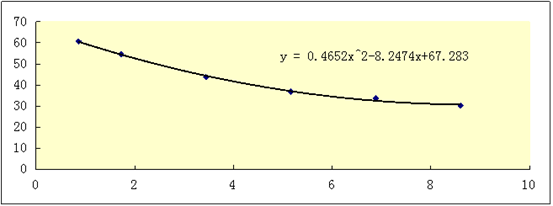
对上曲线方程求导得:y=0.9304×10-3x-8.2474×10-3
所以:5%的乙醇溶液 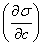 T=0.00054×0.8601-0.0064=-7.4470×10-3
T=0.00054×0.8601-0.0064=-7.4470×10-3
同理得:10%的乙醇溶液 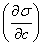 T=-6.6469×10-3
T=-6.6469×10-3
20 %的乙醇溶液 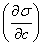 T=-5.0464×10-3
T=-5.0464×10-3
30%的乙醇溶液 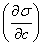 T=-3.4459×10-3
T=-3.4459×10-3
40%的乙醇溶液 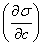 T=-1.8453×10-3
T=-1.8453×10-3
50%的乙醇溶液 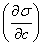 T=-1.8171×10-3
T=-1.8171×10-3
5计算各浓度的Γ和C/Γ。
5%的乙醇溶液:
Γ=﹣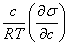 T= 0.8601*7.447/(8.314*293.15)×10-3=2.6280×10-6mol/ m2
T= 0.8601*7.447/(8.314*293.15)×10-3=2.6280×10-6mol/ m2
C/Γ= 0.8601/2.6280×106=0.3273×106
10%的乙醇溶液:
Γ=﹣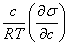 T= 1.7202*6.6469(8.314*293.15)×10-3=4.6914×10-6mol/ m2
T= 1.7202*6.6469(8.314*293.15)×10-3=4.6914×10-6mol/ m2
C/Γ= 1.7202/4.6914×106=0.3667×106
20%的乙醇溶液:
Γ=﹣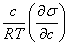 T= 3.4405*5.0464/(8.314*293.15)×10-3=7.1237×10-6mol/ m2
T= 3.4405*5.0464/(8.314*293.15)×10-3=7.1237×10-6mol/ m2
C/Γ= 3.4405/7.1237×106=0.4830×106
30%的乙醇溶液:
Γ=﹣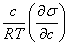 T=5.1607*3.4459/(8.314*293.15)×10-3=7.2964×10-6mol/ m2
T=5.1607*3.4459/(8.314*293.15)×10-3=7.2964×10-6mol/ m2
C/Γ= 05.1607/7.2964×106=0.7073×106
40%的乙醇溶液:
Γ=﹣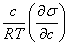 T= 6.8810*1.8453/(8.314*293.15)×10-3=5.2098×10-6mol/ m2
T= 6.8810*1.8453/(8.314*293.15)×10-3=5.2098×10-6mol/ m2
C/Γ= 6.8810/5.2098×106=1.3208×106
50%的乙醇溶液:
Γ=﹣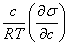 T= 8.6012*1.8171/(8.314*293.15)×10-3=6.4126×10-6mol/ m2
T= 8.6012*1.8171/(8.314*293.15)×10-3=6.4126×10-6mol/ m2
C/Γ= 8.6012/6.4126×106=1.3413×106
6.作C/Γ—C图,求

由图知直线的斜率为:tgβ=0.1479×106
所以  =(tgβ)-1=1/0.1479*10-6=6.7613×10-6
=(tgβ)-1=1/0.1479*10-6=6.7613×10-6
七.思考题
1为什么液体的表面张力随温度升高而减小?
答:同一种物质的表面张力因温度不同而异,当温度升高时物质的体积膨胀,分子间的距离增加,分子之间的相互作用减弱,所以表面张力一般随温度的升高而减小。
2仪器的清洁与否对所测数据有无影响?
答:有影响。毛细管如果不清洁会影响气泡逸出的速度。
八.误差分析
1.实验装置气密性不好,影响压差计的读数。
2.毛细管没有用热的铬酸洗涤干净,这是实验的关键。
3.没有调节好气泡逸出的速度,气泡逸出速度太快每分钟超过30个,气泡逸出速度不均匀。
4.一次测量后没有用待测液洗试管和沾洗毛细管。
5.实验温度,溶液浓度对实验结果的影响。
九.心得体会
本次试验作为最后测试的实验,老师没有给予任何讲解,从实验器材的组装到最终完成,全部由自己摸索完成,我们事先对本实验进行了较为全面的预习,熟知实验原理并熟悉了实验器材,在做实验时才会比较顺利。这次试验结束后,所有的物化实验也就结束了,虽然试验次数不多,但感觉收获不少,特别是在运用计算机软件处理实验数据的方面,学到了很多,我们也不再是用手绘图,而是用计算机处理数据,所得结果更准确也更省时。
第二篇:石工12-11班+120xx523+赵润达最大压差法测表面张力+27

实验二最大压差法测表面张力
一.实验目的
1.掌握最大压差法测定表面张力的原理及方法;
2.测定正丁醇水溶液的表面张力,了解表面张力的概念及影响因素;
3.学习 Gibbs 公式及其应用。
二.实验原理
由于净吸引力的作用,处于液体表面的分子倾向于到液体内部来,因此液体表面倾 向于收缩。要扩大面积,就要把内部分子移到表面来,这就要克服净吸引力作功,所作 的功转变为表面分子的位能。单位表面具有的表面能叫表面张力。
在一定温度、压力下纯液体的表面张力是定值。但在纯液体中加入溶质,表面张力 就会发生变化。若溶质使液体的表面张力升高,则溶质在溶液相表面层的浓度小于在溶 液相内部的浓度;若溶质使液体的表面张力降低,则溶质在溶液相表面层的浓度大于在 溶液相内部的浓度。这种溶质在溶液相表面的浓度和相内部的浓度不同的现象叫吸附。 在一定的温度、压力下,溶质的表面吸附量与溶液的浓度、溶液的表面张力之间的
关系,可用吉布斯(Gibbs)吸附等温式表示:
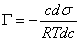
式中 Γ -吸附量(mol/L);
c-吸附质在溶液内部的浓度(mol/L);
σ -表面张力(N/m);
R-通用气体常数(N.m/K.mol);
T-绝对温度(K)。
若 dσ /dc<0,溶质为正吸附;若 dσ /dc>0,溶质为负吸附。通过实验若能测出表 面张力与溶质浓度的关系,则可作出σ -c 曲线,并在此曲线上任取若干个点作曲线的 切线,这些曲线的斜率即为浓度对应的 dσ /dc,将此值代入 2-1 式可求出在此浓度时 的溶质吸附量。
测定液体表面张力的方法有许多种。本实验采用最大压差法,测定装置如图所示。
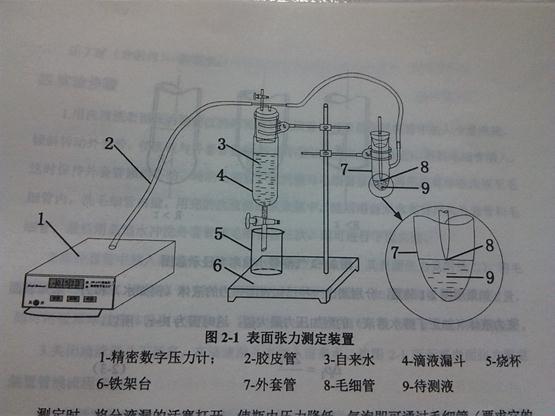
图2-1 表面张力测定装置
测定时,将分液漏的活塞打开,使瓶内压力增加,气泡即可通过毛细管(要求它的尖嘴刚刚与液面接触)。从浸入液面的毛细管端鼓出空气炮时,需要高出外部大气压的 附加压力,以克服气泡表面张力。如果毛细管半径很小,则形成的气泡基本上是球形的(图 2-2)。此时附加压力与表面张力成正比,与气泡的曲率半径成反比,其关系式如下:
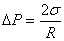
式中 Δ P-广口瓶内滴水形成的附加压力;
R-气泡的曲率半径;
σ-表面张力(N/m)。
当气泡开始形成时 ,表面几乎是平的,这是曲率半径最大,随着气泡的形成,曲 率半径逐渐变小,直到形成半球形,这是曲率半径与毛细管半径 r 相等,曲率半径达最 小值,根据 2-2 式,这时附加压力达最大值。气泡进一步长大,R 变大,附加压力则变 小,直到气泡溢出。
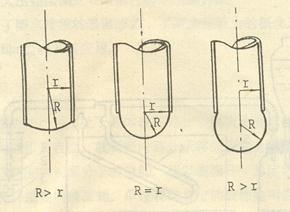
图 2-2 气泡最小曲率半径示意图
如果用图 2-1 装置,分别测出一种已知表面张力的液体(例如水)和另一未知表面 张力液体(如正丁醇水溶液)的附加压力最大值,这时因为 R=r,所以,
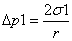
式中:
Δp1 -已知表面张力液体的最大附加压力;
σ1- 已知液体的表面张力。
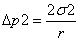
式中:
Δp2 -未知表面张力液体的最大附加压力;
σ2- 未知液体的表面张力。
因为两种液体的最大附加压力(即最大压差)是在同一仪器的同一毛细管测的。所以,上两式的 r 是相同的,若将 r 消去即得:
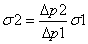
因此,在同一温度下,只要测得ΔP1、ΔP2,再由温度查出已知表面张力液体(水)的表面张力;即可由公式(2-5)求出未知液体的表面张力。
三.仪器与药品
1.仪器
最大压差法测表面张力装置一套,洗瓶,吸耳球。
2.药品
正丁醇(分析纯),蒸馏水。
四.步骤
1.用洗液洗表面张力测定仪的外套管和毛细管。方法是在外套管中放入少量洗液, 倾斜转动外套管,使洗液与外套管接触( 注意不要让洗液从侧管流出 ).再将毛细管插入, 这时保持外套管倾斜不动,转动毛细管,使洗液与毛细管接触,再用洗耳球吸洗液至毛细 管内,洗毛细管内壁.用完的洗液倒回原来瓶中,然后用自来水充分冲洗外套管和毛细管, 最后用蒸馏水冲洗外套管和毛细管各三次,即可进行下面实验;
2.在外套管中放入蒸馏水(作为已知表面张力的液体,其表面张力见附录二),将毛 细管插入外套管,塞紧塞子,并使毛细管尖端刚碰到液面。读出斜管压差计下面一根管内 的零点液位 h0(此时斜管压力计两端都通大气);
3.关闭漏斗下活塞,分液漏斗中装满自来水。按图 2-1 所示装好仪器;
4.打开精密数字压力计电源,然后打开分液漏斗的活塞,将管线内压力放空。按精密数字压力器的采零按钮,使精密数字压力器的示数置零。
5.关闭滴液漏斗上活塞,缓缓打开滴液漏斗下活塞,使分液漏斗中的水慢慢滴入广口瓶中,这时瓶内压力逐渐增加,气泡将通过毛细管端匀速冒出。从精密数字压力计上读出最大压差,重复读取三次,将数据记录在实验记录纸上,取平均值。
6.测完蒸馏水的最大压差后,倒掉蒸馏水,用 0.02mon/L 的正丁醇洗一次外套管 和毛细管,然后再加入该溶液,象测蒸馏水的最大压差一样,测定该溶液的最大压差。 依次侧得 0.05、0.10、0.15、0.20、0.25、0.30、0.35mom/L 的正丁醇溶液的最大压差。
(注意:每更换一次溶液,都应用待定液洗外管套管和毛细管)。
7.记录实验温度.
五.结果处理
1.由附录-查出实验温度下蒸馏水的表面张力。
由公式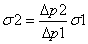 计算出不同浓度正丁醇溶液的表面张力,用表格的形式列出计算结果,并取一组数据附-计算实例。
计算出不同浓度正丁醇溶液的表面张力,用表格的形式列出计算结果,并取一组数据附-计算实例。
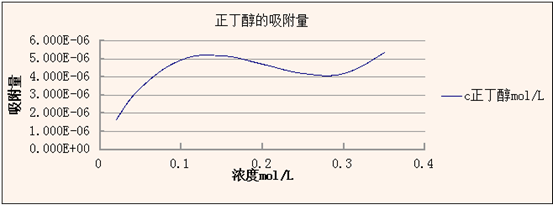
3.以表面张力为纵坐标,以浓度为横坐标,在坐标纸上画出正丁醇溶液的σ-c 图。
4.在σ-c 图上选若干点,作不同浓度曲线时切线,依 Gibbs 公式(2-1)求出相应 的表面吸附量;并在坐标纸上画出正丁醇溶液的吸附等温线。

表1.原始数据表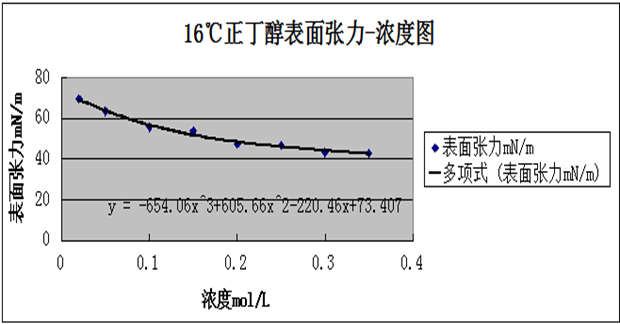

表2. 289K正丁醇的表面张力-吸附量表
误差分析:因为我们的分液漏斗的活塞稍微有点点漏液,所以造成了一定误差。
六.思考题
1.实验中,如果毛细管深入液面 1mm 会造成多大误差?
答:会使最大附加压力增大很多。从而使表面张力增大很多。
按第一组数据分析1mm液体产生压强P=ρgh=9.8Pa
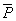 (H
(H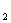 O)=0.351Kp
O)=0.351Kp  (正丁醇)=0.3428Kp
(正丁醇)=0.3428Kp
δ2=0.3428/0.351*73.34=71.62 相对误差=(71.62-69.70)/69.70=2.8%
.实验中会额外造成误差。
2.实验中,为什么要尽量放慢鼓泡速度?
答:为了让气泡逐渐形成,使曲率半径逐渐变小最后达到与毛细管半径相等,曲率半径达最小。鼓泡过快气泡来不及形成,达不到曲率半径最小,会造成实验测量误差。
3.实验中,为什么要求从稀到浓逐个测定不同浓度溶液的表面张力?
答:减少由于残留正丁醇对于浓度的影响而造成的实验误差,使实验更加的精确。
4.解释σ-c 曲线的变化趋势。
答:开始时,曲线变化速率很快,随浓度增加,变化速率逐渐变慢。因为,①当溶液极稀时,表面活性剂分子在溶液中的分布只有一种动平衡。由于浓度极稀,表面上表面活性剂分子彼此不影响,所以可平铺于液面。因此,表面活性剂对表面张力有显著影响。②由于表面活性剂分子在表面浓度增加,所以他们不能像极稀溶液情况下平铺,而是倾斜于液面,因此对表面张力的影响就减小,表现为表面张力随浓度增加而下降减小。③当浓度增至某一数值,表面活性剂在溶液表面吸附达到饱和,并紧密排列,活性分子开始向溶液内部分布。开始形成胶束。④在浓溶液中,表面活性剂动平衡关系不变,但胶束数量不断增加。变化趋势表现为十分平缓。
5.实验中,影响表面张力测定准确性的因素有哪些?
答:影响准确性的因素主要有仪器的气密性,毛细管与液面的接触距离,以及气泡是否缓慢的鼓出。
