\
《实验化学》校本课程实验报告9
姓名 同组学生姓名
实验题目: 树叶上镀铜 实验日期: 年 月 日
【实验目的】
1. 用简单的方法在树叶上镀铜。
2. 体验应用化学知识和技能应用于艺术创作的乐趣。
【实验用品】
氢氧化钠、碳酸钠、酒精、PdCl2 、SnCl2、盐酸、2%硝酸银、2%氨水、10%葡萄糖溶液、稀盐酸、 硫酸铜、稀硫酸、蒸馏水 、新鲜树叶
1000ml的烧杯、250ml的烧杯、小刷子(用来刷去叶肉)、pH试纸、玻璃棒、量筒、学生电源、若干导线。
【实验原理】
由于经前期处理后的树叶是非导体,因此电镀前树叶表面必须进行金属化。本实验采用如下流程:敏化——活化——化学镀——电镀,现将相关原理表述如下:
敏化:
树叶经过敏化处理,表面吸附有一层薄的敏化液,进入清洗水槽时,由于清洗水PH值高于敏化液,发生两价锡的水解作用。
SnCl2+H2O ==Sn(OH)Cl+HCl 同时 SnCl2+2H2O==Sn(OH)2+2HCl
液膜中存在的部分SnCl42-也会随之发生水解。
SnCl42-+ H2O== Sn(OH)++H++4Cl- SnCl42-+2H2O== Sn(OH)2+ 2H++4Cl-
生成的Sn(OH)Cl与Sn(OH)2还可以聚合,形成微溶于水的凝胶状物质Sn2(OH)3Cl。其反应为:Sn(OH)Cl+ Sn(OH)2==Sn2(OH)3Cl
活化:
经过敏化后的树叶,表面吸附了一层还原剂,需要在含有氧化剂的溶液中进行反应,使贵金属离子还原为单质,在树叶表面形成“催化中心”,以便在化学沉积中加速反应。
Sn2+-2e-==Sn4+ Pd2++2e-==Pd Sn2++ Pd2+== Sn4++Pd↓
化学镀银:
C6H12O6+2Ag(NH3)2OH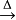 C5H11O5COONH4+3NH3+2Ag↓+H2O
C5H11O5COONH4+3NH3+2Ag↓+H2O
【实验方案】
(一)脱叶绿素处理
选取质硬、完好、带柄的新鲜叶片适量在1000 ml的烧杯中加入5g 氢氧化钠固体和5g 碳酸钠固体,加入500ml水溶液,放在酒精灯上加热至沸腾,将树叶放入煮15分钟,取出树叶放在清水中漂洗2-3分钟。然后用刷子小心把树叶上的叶肉去除,晾干待用。
(二)敏化
称取5gSnCl2溶于部分盐酸水溶液中,然后用蒸馏水稀释到500mL。并控制PH值在0-2之间,为防止二价锡离子氧化成四价锡离子,在敏化槽中应放一些金属锡粒,加入约50ml酒精,并将步骤一的树叶放入敏化液中浸泡约5分钟,然后用蒸馏水漂洗1min,取出待用。
(三)活化
称取0.25g PdCl2放入1000ml烧杯中,加入2mlHCl,用酒精稀释至1L。并控制PH值在1-3间,然后将步骤二中的树叶放入该液中约两分钟,然后取出,蒸馏水洗净。
(四)化学镀银
取一只500毫升的烧杯,放入200毫升2%的硝酸银溶液,再逐滴滴入2%的氨水,直到最初产生的沉淀恰好溶解为止,这就是银氨溶液。把树叶放入银氨溶液中,并滴入10%的葡萄糖溶液约20 mL,2分钟后即取出,用清水漂洗,这时叶片已经银光闪闪。
(五)电镀Cu,装置如图1:
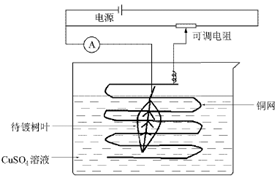
图 1树叶上镀铜
在烧杯内放入硫酸铜浓溶液,再加少量稀硫酸。叶柄用裸铜丝缠绕后放入电解液内作为阴极,取铜网为阳极,12V电压进行电镀。
【实验关键】
1. 叶片一定要质硬而完整,带柄,并洗净。
2. 浸泡叶片的酒精,最好用无水酒精,有利于叶绿素的溶解,使析出的银附牢在叶片的毛孔中。
【实验记录】

【问题与讨论】
每一步完成后用蒸馏水洗过后为什么一定要吸干?
为何有时电压调至6~8V时叶片仍会冒烟?
【实验反思】
因为嫌麻烦电镀铜时未用铜丝绑住叶柄,从而叶柄没有完全浸入硫酸铜溶液中,导致一开始小夹子上镀满了铜,而叶子上有一些地方没有镀满,有点可惜。
第二篇:化学镀铜液的配方
化学镀铜液的配方:
硫酸铜 5g/L
酒石酸甲钠 25g/L
氢氧化钠 7g/L
甲醛 10g/L
稳定剂 0.1g/L

