实验二共沸精馏
一、实验目的:
1.通过实验加深对共沸精馏过程的理解。
2.熟悉精馏设备的构造,掌握精馏操作方法。
3.能够对精馏过程做全塔物料衡算。
4.学会使用气相色谱分析气、液两相组成。
二、实验原理:
精馏是利用不同组份在气一液两相间的分配,通过多次气液两相间的传质和传热来达到 分离的目的。对于不同的分离对象,精馏方法也会有所差异。例如,分离乙醇和水的二元物 系。由于乙醇和水可以形成共沸物,而且常压下的共沸温度和乙醇的沸点温度极为相近,所 以采用普通精馏方法只能得到乙醇和水的混合物,而无法得到无水乙醇。为此,在乙醇一水 系统中加入第三种物质,该物质被称为共沸剂。共沸剂具有能和被分离系统中的一种或几种 物质形成最低共沸物的特性。在精馏过程中共沸剂将以共沸物的形式从塔顶蒸出,塔釜则得 到无水乙醇。这种方法就称作共沸精馏。
乙醇—水系统加入共沸剂苯以后可以形成四种共沸物。现将它们在常压下的共沸温度、 共沸组成列于表1。
为了便于比较,再将乙醇、水、苯三种纯物质常压下的沸点列于表2。
表1 乙醇水一苯三元共沸物性质
共沸物(简记) 共沸点℃
共沸物组成,t%
乙醇 水 苯
乙醇—水一苯(T) 64.85 18.5 7.4 74.1
乙醇一苯(ABZ) 68.24 32.7 0.0 67.63
苯一水(BWZ) 69.25 0.0 8.83 91.17
乙醇一水(AWz) 78.15 95.57 4.43 0.0
2
表2 乙醇、水、苯的常压沸点
从表1和表2列出沸点看,除乙醇一水二元共沸
物的共沸点与乙醇沸点相近之外,其余三种共沸物
的沸点与乙醇沸点均有10℃左右的温度差。因此,
可以设法使水和苯以共沸物的方式从塔顶分离出
来,塔釜则得到无水乙醇。
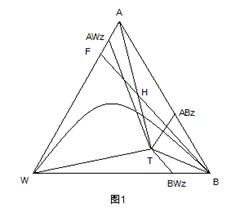
整个精馏过程可以用图1来说明。图中A、B、
W分别为乙醇、苯和水的英文字头;AB
Z、AW
Z、
BW
Z代表三个二元共沸物,T表示三元共沸物。图中
的曲线为25℃下乙醇、水、苯三元混合物的溶解度曲线。该曲线下方为两相区,上方为均 相区。图中标出的三元共沸组成点T是处在两相区内。
以T为中心,连接三种纯物质A、B、w及三个二元共沸点组成点AB
Z、AW
Z、BW
Z,将
该图分为六个小三角形。如果原料液的组成点落在某个小三角形内。当塔顶采用混相回流时 精馏的最终结果只能得到这个小三角形三个顶点所代表的物质。故要想得到无水乙醇,就应 该保证原料液的组成落在包含顶点A的小三角形内,即在ΔATABz或ΔATAWz内。从沸点 看,乙醇—水的共沸点和乙醇的沸点仅差0.15℃,就本实验的技术条件无法将其分开。而乙 醇一苯的共沸点与乙醇的沸点相差10.06℃,很容易将它们分离开来。所以分析的最终结果 是将原料液的组成控制在ΔATABz中。
图1中F代表未加共沸物时原料乙醇、水混合物的组成。随着共沸剂苯的加入,原料液 的总组成将沿着FB连线变化,并与AT线交于H点,这时共沸剂苯的加入量称作理论共沸剂
用量,它是达到分离目的所需最少的共沸剂量。
上述分析只限于混相回流的情况,即回流液的组成等于塔顶上升蒸汽组成的情况。而塔 顶采用分相回流时,由于富苯相中苯的含量很高,可以循环使用,因而苯的用量可以低于理 论共沸剂的用量。分相回流也是实际生产中普遍采用的方法。它的突出优点是共沸剂的用量 少,共沸剂提纯的费用低。
三、装置、流程及试剂
1.装置
物质名称(简记) 乙醇(A) 水(W) 苯(B)
沸点温度(℃) 78.3 100 80.2
图1
3
本实验所用的精馏塔为内径Ф20×200mm的玻璃塔。内装?网环型Ф2×2mm的高效 散装填料。填料层高度1.2m。
塔釜为一只结构特殊的三口烧瓶。上口与塔身相连:侧口用于投料和采样;下口为出料 口;釜侧玻璃套管插入一只测温热电阻,用于测量塔釜液相温度,釜底玻璃套管装有电加热 棒,采用电加热,加热釜料,并通过一台自动控温仪控制加热温度,使塔釜的传热量基本保 持不变。塔釜加热沸腾后产生的蒸汽经填料层到达塔顶全凝器。为了满足各种不同操作方式 的需要,在全凝器与回流管之间设置了一个特殊构造的容器。在进行分相回流时,它可以用 作分相器兼回流比调节器;当进行混相回流时,它又可以单纯地作为回流比调节器使用。这 样的设计既实现了连续精馏操作,又可进行间歇精馏操作。
此外,需要特别说明的是在进行分相回流时,分相器中会出现两层液体。上层为富苯相、 下层为富水相。实验中,富苯相由溢流口回流入塔,富水相则采出。当间歇操作时,为了保 证有足够高的溢流液位,富水相可在实验结束后取出。
2.流程
具体的实验流程见图2。
3.试剂
实验试剂有乙醇(化学纯),含量95%:苯(分析纯),含量99.5%。
四、实验步骤
方法一:间歇精馏
1.称取80克95%的乙醇和一定量的苯(通过共沸物的组成计算,参考量为40克),加入 塔釜中,并分别对原料乙醇和苯进行色谱分析,确定其组成。
2.向全凝器中通入冷却水,并开启釜电加热系统,调节加热电流慢慢升至0.4A(注意 不要使电流过大,以免设备突然受热而损坏)。待釜液沸腾,开启塔身保温电源,调节保温 电流,上段为0~0.4A,下段为0.05~0.2A,以使填料层具有均匀的温度梯度,保证全塔处 在正常的操作范围内。
3.当塔头有液体出现,全回流20分钟稳定后,调节回流比进行混相回流操作,回流比为 5:1~3:1条件下运行20分钟后,将回流比调至1:3。
4.每隔20分钟记录一次塔顶、塔釜温度。
5.待分相器内液体开始溢流,并分成两相,上层为苯相,下层为水相,且能观察到三元 共沸物在苯相苯中以水珠形态穿过,溶于水相中,此时,关闭回流比控制器,开始每隔10 4
分钟取塔釜气项试样进行纯度分析。
6.待塔釜中乙醇含量大于99.6%时,停止加热,让塔内持液全部流至塔釜,取出釜液。
7.将塔顶馏出液用分液漏斗分离。并依次用气相色谱仪分析富水相、富苯相以及釜液组 成,并分别称重。
8.切断设备的供电电源,关闭冷却水,结束实验。
图2共沸精馏流程
方法二:连续精馏:
1.称取40~50克95%的乙醇和一定量的苯(参考量为20~25克)加入塔釜中。
2.开启塔釜电加热系统,慢慢调节加热电流为0.3~0.5A,并向全凝器中通冷却水。当 5
塔头开始出现液滴时,全回流20分钟。
3.将95%的乙醇和苯(按三元共沸物的配比)从塔加料口加入塔中。乙醇的进料流量 (参考值为50~100ml/h),苯的加人量应根据塔顶水相和塔釜乙醇的纯度确定。当塔顶 分相器内液体开始回流时,停止加入原料苯,保持适宜的回流比(参考值为3:1~5:1)。
4.用气相色谱分析塔釜出料乙醇和塔顶排出水的组成,计算单位时间内共沸剂苯的损 失量,以确定连续补加苯的量。
5.在精馏完一定量的有水乙醇后,停止加料。待塔内无原料后,取出精制后乙醇。
6.将塔顶馏出液用分液漏斗分离。并依次用气相色谱仪分析富水相、富苯相以及产品 组成,并分别称重。
7.切断电源,关闭冷却水,结束实验。
五、数据处理
1.作全塔物料衡算,并对共沸物形成的富水相和富苯相进行分析和衡算,求出塔顶三 元共沸物的组成。
2.画出25℃下乙醇一水一苯三元物系的溶解度曲线。在图上标明共沸物的组成点,画 出加料线,并对精馏过程作简要的说明。
六、思考题
1.如何计算共沸剂的加入量?
2.需要测出哪些量才可以作全塔的物料衡算?具体的衡算方法是什么?
3.将计算出的三元共沸物组成与文献值比较,求出其相对误差,并分析实验过程中产 生误差的原因。
七、参考文献
[1]EACoulson,etal.LaboratoryDistillation Practice,L.GeorgeNewsLtd.1958
[2]ErichKrell.HandbookofLaboratoryDistillation,Amsterdam,Elsevier,1982
[3] 陈洪钫. 基本有机化工分离工程.北京:化学工业出版社,1985
[4]FGShinskey.DistillationContol forProductivity andEnergyConservatlon2nded.NewYork, McGraw-HillBookco,19842nd
[5]HoanhNPham,etal.ChemicalEngineeringScience1990,45(7),1823
第二篇:天津大学化工学院:共沸精馏实验报告docx
化工专业实验报告
实验名称: 共沸精馏
实验人员: 同组人:
实验地点:天大化工技术实验中心624室
实验时间: 2012年9月25日
班级/学号: 09 级分子科学与工程专业一班
学号: 实验组号:01
指导教师:
实验成绩:
共沸精馏
一、 实验目的
1. 通过实验加深对共沸精馏过程的理解;
2. 熟悉精馏设备的构造,掌握精馏操作方法;
3. 能够对精馏过程做全塔物料衡算;
4. 学会使用气相色谱分析气、液两相组成。
二、 实验原理
精馏是利用不同组份在气-液两相间的分配,通过多次气液两相间的传质和传热来达到分离的目的。对于不同的分离对象,精馏方法也会有所差异。例如,分离乙醇和水的二元物系。由于乙醇和水可以形成共沸物,而且常压下的共沸温度和乙醇的沸点温度极为相近,所以采用普通精馏方法只能得到乙醇和水的混合物,而无法得到无水乙醇。为此,在乙醇-水系统中加入第三种物质,该物质被称为共沸剂。共沸剂具有能和被分离系统中的一种或几种物质形成最低共沸物的特性。在精馏过程中共沸剂将以共沸物的形式从塔顶蒸出,塔釜则得到无水乙醇。这种方法就称作共沸精馏。
乙醇-水系统加入共沸剂苯以后可以形成四种共沸物。现将它们在常压下的共沸温度、共沸组成列于表1。为了便于比较,再将乙醇、水、苯三种纯物质常压下的沸点列于表2。
表1 乙醇水-苯三元共沸物性质
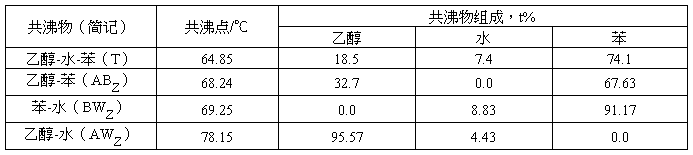
表2 乙醇、水、苯的常压沸点

 从表1和表2列出沸点看,除乙醇-水二元共沸物的共沸物与乙醇沸点相近之外,其余三种共沸物的沸点与乙醇沸点均有10℃左右的温度差。因此,可以设法使水和苯以共沸物的方式从塔顶分离出来,塔釜则得到无水乙醇。
从表1和表2列出沸点看,除乙醇-水二元共沸物的共沸物与乙醇沸点相近之外,其余三种共沸物的沸点与乙醇沸点均有10℃左右的温度差。因此,可以设法使水和苯以共沸物的方式从塔顶分离出来,塔釜则得到无水乙醇。
整个精馏过程可以用图1来说明。图中A、B、W分别为乙醇、苯和水的英文字头;ABZ,AWZ,BWZ代表三个二元共沸物,T表示三元共沸物。图中的曲线为25℃下的乙醇、水、苯三元共沸物的溶解度曲线。该曲线的下方为两相区,上方为均相区。图中标出的三元共沸组成点T是处在两相区内。
以T为中心,连接三种纯物质A、B、W及三个二元共沸点组成点ABZ、AWZ、BWZ,将该图分为六个小三角形。如果原料液的组成点落在某个小三角形内。当塔顶采用混相回流时精馏的最终结果只能得到这个小三角形三个顶点所代表的物质。故要想得到无水乙醇,就应该保证原料液的组成落在包含顶点A的小三角形内,即在ΔATABZ或ΔATAWZ内。从沸点看,乙醇-水的共沸点和乙醇的沸点仅差0.15℃,就本实验的技术条件无法将其分开。而乙醇-苯的共沸点与乙醇的沸点相差10.06℃,很容易将它们分离开来。所以分析的最终结果是将原料液的组成控制在ΔATABZ中。
图1中F代表未加共沸物时原料乙醇、水混合物的组成。随着共沸剂苯的加入,原料液的总组成将沿着FB连线变化,并与AT线交于H点,这时共沸剂苯的加入量称作理论共沸剂用量,它是达到分离目的所需最少的共沸剂量。
上述分析只限于混相回流的情况,即回流液的组成等于塔顶上升蒸汽组成的情况。而塔顶采用分相回流时,由于富苯相中苯的含量很高,可以循环使用,因而苯的用量可以低于理论共沸剂的用量。分相回流也是实际生产中普遍采用的方法。它的突出优点是共沸剂的用量少,共沸剂提纯的费用低。
三、 装置、流程及试剂
1. 装置
本实验所用的精馏塔为内径Ф20×200mm的玻璃塔。内部上层装有Θ网环型Ф2×2 mm的高效散装填料,下部装有三角网环型的高效散装填料。填料塔高度略高于1.2m。
塔釜为一只结构特殊的三口烧瓶。上口与塔身相连:侧口用于投料和采样;下口为出料口;釜侧玻璃套管插入一只测温热电阻,用于测量塔釜液相温度,釜底玻璃套管装有电加热棒,采用电加热,加热釜料,并通过一台自动控温仪控制加热温度,使塔釜的传热量基本保持不变。塔釜加热沸腾后产生的蒸汽经填料层到达塔顶全凝器。为了满足各种不同操作方式的需要,在全凝器与回流管之间设置了一个特殊构造的容器。在进行分相回流时,它可以用作分相器兼回流比调节器;当进行混相回流时,它又可以单纯地作为回流比调节器使用。这样的设计既实现了连续精馏操作,又可进行间歇精馏操作。
此外,需要特别说明的是在进行分相回流时,分相器中会出现两层液体。上层为富苯相、下层为富水相。实验中,富苯相由溢流口回流入塔,富水相则采出。当间歇操作时,为了保证有足够高的溢流液位,富水相可在实验结束后取出。
2. 流程
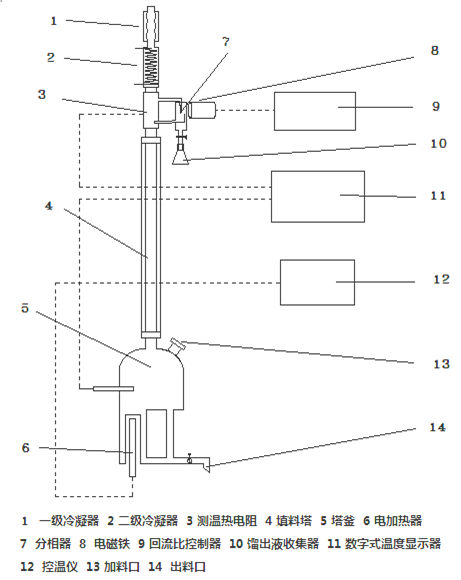
3. 试剂
实验试剂有80g乙醇(化学纯),含量95%;苯(分析纯)34.6g,含量99.5%。
四、 实验步骤
1. 将原料乙醇80g,苯34.6g,依次加入塔釜,打开电源,记录时间、塔釜及塔顶的初始温度和加热电流;
2. 30分钟后打开回流比,调至5:1,20分钟后调至3:1;
3. 溢流开始后,在溢流管仍有水珠连续流出的条件下,将回流比调至1:1,再过10分钟后调至1:3至结束;
4. 3小时后开始蒸出过量的苯,根据色谱分析结果,分次放出若干量蒸出液,直至将塔釜内苯内苯蒸净;
5. 将所有蒸出液放入分液漏斗内,静置5分钟,将分离后的富苯相和富水相分别称重,并分别分析。
五、 实验原始数据
设备编号:01
原始数据记录表见附页预习报告五、实验记录。
备注:1. 气相色谱操作条件:压力为0.075MPa,汽化室温度为110℃,柱箱温度为135℃,检测室温度为110℃。
2. 各物质校正因子:f(Water)=0.742,f(Alcohol)=1.000,f(Benzene)=1.170。
六、 实验数据处理
1. 数据处理表格
1.1 表1:色谱分析条件
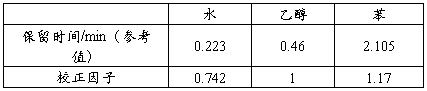
1.2 表2:各阶段塔底组份分析表
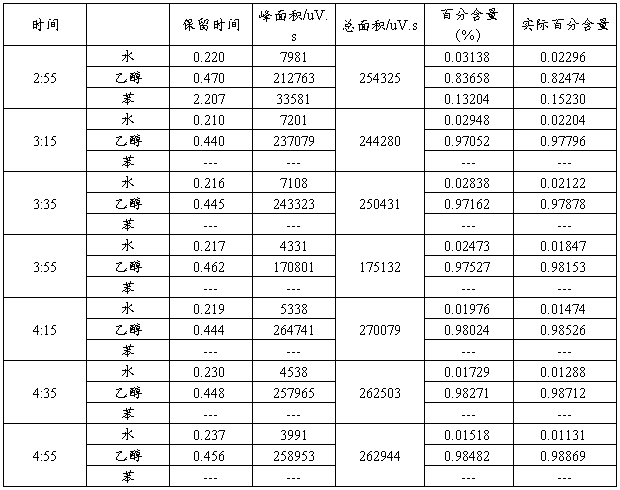
1.3表3:富水相、富苯相及釜液的色谱分析结果表(反应结束后)
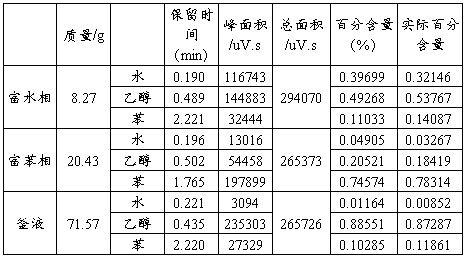
1.4原料乙醇和苯的色谱分析表

实际百分含量用公式 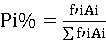 进行计算
进行计算
计算举例:
以反应富苯相中的各组分实际百分含量为例进行计算:
P水%= 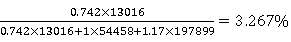
P乙醇%= 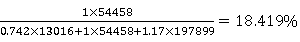
P苯%= 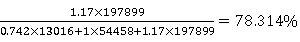
2. 数据处理计算
2.1做全塔物料衡算,并对共沸物形成的富水相和富苯相进行分析和衡算,求出塔顶三元共沸物的组成。
1) 对塔内乙醇进行物料衡算
原料液中乙醇含量百分比:(0.952344153+0.952930162)/2=0.9526
原料液中乙醇含量:80*0.9526=76.21g
由上表所得:富水相中乙醇质量分数:
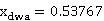
富水相中乙醇含量:8.27*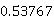 =4.4465g
=4.4465g
富苯相中乙醇质量分数:
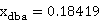
富苯相中乙醇含量:20.43*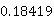 =3.7630g
=3.7630g
塔釜中乙醇含量:
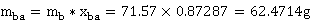
则塔内残余乙醇的含量为:La=76.21-4.4465-3.7630-62.4714=5.5291g
2) 对塔内苯进行物料衡算
原料液中苯含量34.6g
由上面表格中计算得到的实际百分比得:
富水相中苯含量:
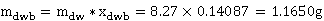
富苯相中苯含量:
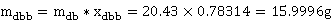
塔釜液中苯的含量:
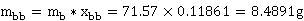
则塔内残余苯的含量为:Lb=34.6-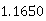 -
-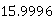 -
- =8.9463g
=8.9463g
3) 对塔内水进行物料衡算
原料液中水含量为80*(1-0.9526)=3.792
富苯相中水含量:
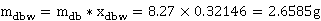
富水相中水含量:
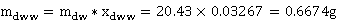
釜液中的水含量:mbw=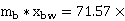 0.00852=0.6095g
0.00852=0.6095g
塔内残余水含量:3.792-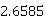 -
-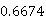 -0.6095=-0.1434g
-0.6095=-0.1434g
4) 塔内总持液量为:80+34.6-8.27-20.43-71.57=14.33g≈5.5291+8.9463-0.1434=14.3320g
5) 对物料衡算结果的分析:
塔内总持液比例:
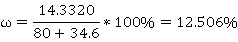
从上述计算可以看出,塔内持液占了不小的比例,其中既包括了乙醇,也包括了苯和水。当然除了塔内残留一部分外,可能还有一些乙醇通过各种可能途径挥发了。
对于塔内水的衡算结果为负值这一事实,经过分析,我们认为这是由于在进行塔釜产品衡算时,对气相色谱的分辨率设置过低,导致水的色谱峰没有被识别所造成。
6) 塔顶三元共沸物组成计算
组分水所占比例:
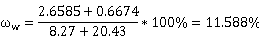
相对误差:
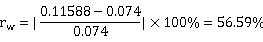
组分乙醇所占比例:
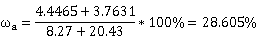
相对误差:
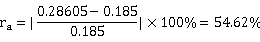
组分苯所占比例:
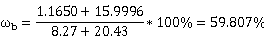
相对误差:
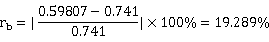
总结上述结果得到下表:
表5 塔顶三元共沸物组成
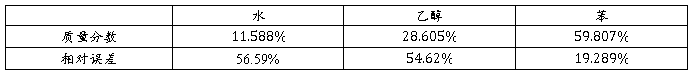
误差结果分析:从上表可以看出,实验的测出的相对误差比较大,之所以会引起误差,主要是因为该求算方法计算的只是塔顶馏出液的组成,而塔顶馏出液实际上是三元共沸物与二元共沸物的混合液。该实验过程并没有很好地对三元共沸物蒸尽的临界点进行控制,因而没法按照精确方法计算。而且由于苯有很强的挥发性,在那么长的时间内挥发了,造成苯的质量分数减小,从而引起其他质量分数的上升,从实验数据也可以看出这一点。今后实验前,一定要仔细,认真检查实验仪器的工作状态。
2.2画出25℃下乙醇—水—苯三元物系的溶解度曲线。在图上表明共沸物的组成点,画出加料线。
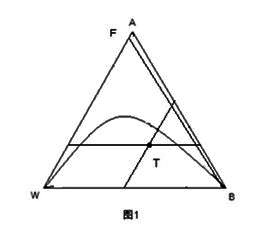
如图所示,BF为加料线,T为共沸点。图中曲线为溶解度曲线。
七、 思考题
1. 如何计算共沸剂的加入量?
1) 在指定的压力下,做水-乙醇-苯的三角相图;
2) 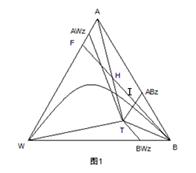 根据相关文献在图上确定共沸物组成点(自由度为1,所以务必确定是该压力下的共沸点组成),包括三元共沸物,所有可能的二元共沸物。按照实验原理中的说明做出下面的连线。由沸点参数可知,原料液组成应控制在ΔATABZ中;
根据相关文献在图上确定共沸物组成点(自由度为1,所以务必确定是该压力下的共沸点组成),包括三元共沸物,所有可能的二元共沸物。按照实验原理中的说明做出下面的连线。由沸点参数可知,原料液组成应控制在ΔATABZ中;
3) 连接F,B两点,交ΔATABZ于H和I,这两点分别是加入共沸剂的最小量和最大量。
4) 从图上可以读出各线段长度。利用杠杆规则,若混合液的组成为I, 则mB=mF*|IF|/|BI|;若混合液组成为H,则mB=mF*|HF|/|BH|。I和H之间的组成点所用到的共沸剂量应在这两个值之间。
2. 需要测出哪些量才可以作全塔的物料衡算?具体的衡算方法是什么?
总共需要六个数据才能对全塔进行物料衡算,具体分别是:1、塔釜液质量mb;2、塔顶富水相质量mdw;3、塔顶富苯相质量mdb;4、塔釜残液各组分质量分数xbi;5、塔顶富水相各组分质量分数xdwi;6、塔顶富苯相各组分质量分数xdbi;7、原料液质量mf;8、原料液各组分的质量分数xfi。
具体衡算方法如下:忽略塔内总持液量的影响,对塔内各个组分列算式:mf*xfi-mdw*xdwi-mdbi*xdbi-mb*xbi,如果结果近似等于0,则认为该组分在全塔范围内守恒。否则需要将塔内损失考虑在内。
3. 将计算出的三元共沸物组成与文献值比较,求出其相对误差,并分析实验过程中产生误差的原因。
相对误差见表5。之所以会引起误差,主要是因为该求算方法计算的只是塔顶馏出液的组成,而塔顶馏出液实际上是三元共沸物与二元共沸物的混合液。该实验过程并没有很好地对三元共沸物蒸尽的临界点进行控制,因而没法按照精确方法计算。而且由于苯有很强的挥发性,在那么长的时间内挥发了,造成苯的质量分数减小,从而引起其他质量分数的上升,从实验数据也可以看出这一点。今后实验前,一定要仔细,认真检查实验仪器的工作状态。
八、 参考文献
[1]. E A Coulson, etal ,Laboratory Distillation Practice, L.George News Ltd,1958
[2]. Erich Krel, Handbook of Laboratory Distillation, Amsterdam, Elsevier, 1982
[3]. 陈洪钫,基本有机化工分离工程,北京:化学工业出版社1985
[4]. F G Shinskey, Distillation Control for Productivity and Energy Conservation 2nd ed, New York, Mc Graw-Hill Book co, 1984 2nd
[5]. Hoanh N Pham,et al. Chemical Engineering Science 1990,45(7):1823
