课题2:化学是一门以实验为基础的科学
一,教学目标:
1、知识与技能:认识实验是化学学习的重要途径,学会细致、准确、客观地观察、描述和记录实验现象。
2、过程与方法:能有意识地发现生活中值得探究的问题,并能进行实验,通过对实验现象的观察和分析得出有价值的结论。
3、情感与价值观:体会化学与人类进步以及社会发展的密切关系,关注与化学有关的社会问题,认识学习化学的价值。 二,实验准备:
1、澄清石灰水,水
2、蜡烛、小刀、火柴、烧杯(干燥、洁净)、集气瓶、玻璃片、水槽。
三,课时安排:二课时
四,教学过程:
第一课时:
实验探究:
探究1:观察和描述——对蜡烛及其燃烧的探究
探究指导:
观察方法:运用味觉以外的感觉器官对蜡烛燃烧前、燃烧时和
熄灭后进行详细的、客观的观察、描述和记录。
记录方法:课本第九页探究实验报告。
探究观察提示:
1、点燃前:观察色、味、状态,形状,硬度,溶于水的性质,
是否浮在水面,水里或沉入水底。
2、点燃时:发生了哪些变化?火焰的层次怎样,亮度怎能样,
温度高低怎样?怎样证明它的生成物是什么?
3、熄灭时:有何现象?迅速用火柴点刚熄灭的白烟,蜡烛能否
重新燃烧?
探究参考:
1、点燃前:蜡烛为圆柱形,白色固体,半透明,有轻微的气味,
质地柔软。用小刀可切割,指甲可划出痕迹,中心
由细线拧成的烛芯,把切下的小块蜡烛放入水中,
不溶于水且浮在水面上,说明密度比水小。
2、点燃时:蜡烛能被点燃,燃烧时较安静,并能持续燃烧,有
火焰产生,火焰会随气流闪烁、摇晃,火焰上有黑
烟向上冲,火焰分层次,上层火焰黄色且明亮,中
层较暗,内层底部淡蓝色,把火柴梗放入烛火中,
外层火焰处最先碳化,说明外焰温度最高。加热物
体时应用外焰。
3、熄灭时:有白烟从烛芯飘出,迅速用火柴点燃白烟,火会顺
白烟将蜡烛重新点燃。
实验中注意的问题:
1、点燃蜡烛时要仔细观察前、中、后的所有现象。
2、火柴梗放入火焰中时间为2S左右。
3、点燃蜡烛熄灭后的白烟时,最好选粗蜡烛且速度要快。 小结:略
作业:探究实验报告。
教后:
第二课时:对人体吸入的空气和呼出的气体的探究
回顾旧识:
人的呼吸过程是一个什么样的过程?
思维猜想:
人每时每刻都在进行呼吸,人吸进的气体和呼出的气体是否一样?
作出猜想
1、呼出的气体中二氧化碳的含量比空气多。
2、呼出的气体中氧气的含量比空气少。
3、呼出的气体中水蒸气的含量比空气多。
制定计划收集实证:查阅资料,设计实验,验证自己的假设。
探究提示:
1、二氧化碳能使澄清石灰水变浑浊。
2、氧气能使带火星的木条复燃。
3、二氧化碳能使燃着的木条熄灭。
探究指导:
1、收集两瓶空气做对照实验(如何收集?)
2、收集两瓶呼出的气体做实验。
提问:如何收集呼出的气体?
演示:用排水集气法收集气体。
3、收集一瓶呼出的气体,用澄清的石灰水检验。
同时做空气的对比实验。
4、收集一瓶呼出的气体,用燃着的小木条检验。同时做空气的对比实验。
5、对着干燥的玻璃片呼气。同时做空气的对比实验。 由以上实验得出的初步结论是:
1、呼出的气体中二氧化碳的含量比空气多。
2、呼出的气体中氧气的含量比空气少。
3、呼出的气体中水蒸气的含量比空气多。
探究参考:
步骤1:瓶内无水且瓶口向外冒气泡
步骤2、两个干燥的集气瓶中就有空气。
步骤3、呼出气体中浑浊多此,说明探究参考
步骤1:瓶内无水且瓶口向外冒气泡。
步骤2、两个干燥的集气瓶中就有空气。
步骤3、呼出气体中浑浊更多些,说明呼出的气体中二氧化碳的
含量比空气多。
步骤4、呼出气体中燃着的木条熄灭,说明呼出的气体中二氧化
碳浓度大,不利于燃烧。
步骤5、呵气的玻璃片上有较多的水珠,说明呼出的气体中水蒸
气的含量比空气中高。
结论:跟空气相比,人呼出的气体中氧气含量减少,二氧化碳和
水的含量增加。步骤4、呼出气体中燃着的木条熄灭,说明二氧化碳浓度大,不利于燃烧。
步骤5、呵气的玻璃片上有较多水珠,说明呼出的气体中水蒸气
的含量比空气高。
结论:跟空气相比,人呼出的气体中氧气含量减少,二氧化碳和
水的含量增加
实验中应注意的问题:
1、 呼气导管应用饮料吸管,不要用实验室中的玻璃管。
2、 呼气换气时不要把集气瓶中的水吸入口中。
3、 实验中倒入瓶中的石灰水应相同(同体积同浓度),且量
要足。
4、 伸入瓶中的木条燃烧的情况应相同。
5、 探究参考
步骤1:瓶内无水且瓶口向外冒气泡。
步骤2、两个干燥的集气瓶中就有空气。
交流讨论:
1、与其他组的实验结论是否相同?分析其他可能的结论,并再讨论如何证明你的推断。
2、从生物的角度,分析吸入和呼出的气体不同的原因。
四,教学反思评价:
1、学完本课题你的收获是什么?受到哪些启发?
2、你明白了什么是科学探究?
五,作业安排:科学探究报告册
第二篇:九年级化学上册 2.3制取氧气教案1.

上教考资源网 助您教考无忧
课题3 制取氧气
教学目的:
1、使学生掌握实验室制取氧气的方法和反应原理
2、了解工业上从空气中提取氧气的基本原理
3、了解分解反应的定义及其与化合反应的区别
4、使学生对催化剂的概念有一个大致印象
教学重点:实验室制取氧气和收集气体的操作方法的示范
教学难点:催化剂
教学过程:一、氧气的实验室制法(化学变化)
1、双氧水(无色液体)制氧气
[演示实验]:课本P34 图2—P34表格)
2)、加热MnO2MnO2
2MnO2的化学性质
二氧化锰 水 + 氧气
2H2O + O2
[板书]:催化剂——在化学反应中能改变其它物质的化学反应速率,而本身的质量和化学性质在反应前后没有改变的物质叫催化剂。
[讲解]:催化剂:1)、催化剂只改变化学反应的速率,不改变化学反应的性质和产量。
2)、催化剂改变化学反应速率,可能是“加快”,可能是“减慢”。
版权所有@中国教育考试资源网

上教考资源网 助您教考无忧
3)、一个化学反应可能有几种物质能做它的催化剂。 4)、没有万能催化剂
5)、催化剂在化学反应前后质量和化学性质不改变,在反应的过程中可能改变。
2、高锰酸钾(紫黑色晶体)制氧气
[板书]:
KMnO4 2MnO4 + MnO2 + O2
3、氯酸钾(白色晶体)和二氧化锰制氧气
[板书]:(要掌握各物质的化学式)
氯酸钾 二氧化锰 氯化钾 + 氧气 KClO3 2KCl+ 02
[板书]:分解反应----
铜绿受热分解
[、组装仪器;2、检查装置的气密性;3、装药品,连接仪器;
,再对药品处加热;5、气泡连续均匀冒出时再收集;
6时,先把导管移出水面,再熄灭酒精灯。
[收集方法]:密度比空气大------向上排气法(干而不纯)
不易溶于水-------排水集气法(湿而纯)
[验满]:带火星的木条放在集气瓶口,复
燃则满
版权所有@中国教育考试资源网

上教考资源网 助您教考无忧
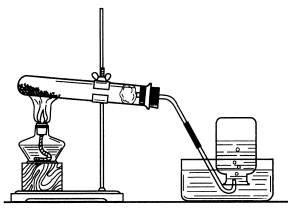
[演示实验]:说处每处仪器的名称及其注意点是为什么(为什么靠近管口要放团棉花?
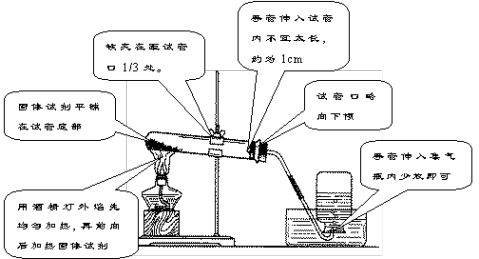
)
[指导阅读]:请同学们阅读P17
[板书]:

氧气的沸点不同,用蒸馏法,分离液态空气。
( )
A.
B.在分解氯酸钾制氧气时,可用二氧化锰作催化剂
C.二氧化锰在氯酸钾受热分解反应中,起着是否有氧气放出的决定性作用
D.只有二氧化锰才能加快氯酸钾分解的速度,起催化作用
版权所有@中国教育考试资源网

上教考资源网 助您教考无忧
2、在高锰酸钾分解制氧气的反应中,二氧化锰是 物;而在氯酸钾与二氧化锰混合加热制氧气时,二氧化锰是 、氯酸钾是 ;若不加二氧化锰,则氯酸钾受热 (填“能”与“不能”)分解产生氧气。如果将高锰酸钾与氯酸钾混合加热,其反应速度与单独加热氯酸钾制取氧气的速度相比
要 (填“快”与“慢”)。
3、高锰酸钾 (填“是”与“不是”)氯酸钾加热制取氧气反应的催化剂。
版权所有@中国教育考试资源网
